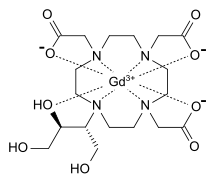
Гадобутрол - Gadobutrol
 | |
| Клинические данные | |
|---|---|
| AHFS /Drugs.com | Международные названия лекарств |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | IV |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Химические и физические данные | |
| Формула | C18ЧАС31Б-гN4О9 |
| Молярная масса | 604.72 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Гадобутрол (ГОСТИНИЦА ) (Gd-DO3A-бутрол) является контрастный агент для МРТ на основе гадолиния (GBCA).
Он получил маркетинговое одобрение в Канаде и США.[1][2][3][4]
По состоянию на 2007 год это был единственный GBCA утвержден при 1,0 молярных концентрациях.[5]
Гадобутрол продается Bayer AG так как Гадовист, и Bayer HealthCare Pharmaceuticals as Гадавист.[6]
Медицинское использование
Гадобутрол - лекарственный препарат, используемый в диагностической магнитно-резонансной томографии (МРТ) у взрослых и детей. Он обеспечивает усиление контраста во время исследований черепа, позвоночника, груди или других исследований. В центральной нервной системе гадобутрол воздействует на любые области с нарушенным гематоэнцефалическим барьером (ГЭБ) и / или аномальной васкуляризацией. В тканях груди гадобутрол выявляет наличие и степень злокачественного заболевания груди. Точно так же гадобутрол также используется в магнитно-резонансной ангиографии с контрастированием (CE-MRA) для диагностики инсульта, обнаружения перфузии опухоли и наличия очаговой церебральной ишемии.[6][7]
Гадобутрол следует вводить внутривенно только медицинским работникам. При приготовлении и проведении инъекции всегда необходимо использовать стерильные методы. По сравнению с другими GBCA, гадобутрол доступен в более концентрированной форме (1 ммоль / мл) для облегчения приема большого объема. Рекомендуемая доза составляет 0,1 мл / кг массы тела.[6]
Побочные эффекты
Безопасность гадобутрола оценивалась в ходе клинических испытаний и постмаркетингового периода, для многократного применения, в различных группах населения и при многократных дозах.[6][7]
Наиболее тяжелой реакцией на гадобутрол является фиброз нефрогенной системы (NSF) у пациентов с нарушением выведения препарата. Риск наиболее высок среди пациентов с хроническим нарушением функции почек и пациентов с острым повреждением почек. NSF может привести к смерти или серьезному повреждению кожи, мышц и внутренних органов.[6]
Пациенты, у которых ранее была неблагоприятная реакция на другой контрастный агент, у которых есть бронхиальная астма и / или аллергические расстройства, повышен риск реакции гиперчувствительности на гадобутрол. Реакции гиперчувствительности могут включать анафилактоидные и анафилактические реакции от легкой до тяжелой. Эти реакции нечасты, однако необходимо наблюдение за пациентом на предмет признаков и симптомов во время и после приема гадобутрола.[6][7]
Другие, более легкие побочные реакции наблюдались у небольшой части пациентов после приема. Эти реакции могут включать, но не ограничиваются следующим:[6]
- Головная боль
- Тошнота и / или рвота
- Реакции в месте инъекции (ощущение холода, тепла, боли или жжения)
- Дисгевзия (неприятный привкус во рту)
- Жарко
- Головокружение
- Сыпь
- Эритема (покраснение кожи)
- Одышка (затрудненное дыхание)
- Парестезия (чувство жжения)
Использование в определенных группах населения
Беременность
FDA отнесло гадобутрол к категории C при беременности. Достаточных исследований гадобутрола у беременных женщин не проводилось. Однако было показано, что другие GBCA проникают через плаценту у людей и вызывают заражение плода, но не оказывают неблагоприятного воздействия на плод.[6]
Были проведены исследования на животных, в которых беременные крысы и кролики получали дозу, в 12 и 8 раз превышающую человеческий эквивалент, исходя из площади поверхности тела, соответственно. Эти воздействия часто приводили к задержке развития эмбриона и смерть эмбриона. Задержка эмбриона не наблюдалось у обезьян, которым вводили дозу в 8 раз больше рекомендуемой для человека, но приводило к гибели эмбрионов. Животным вводили многократные дозы повторно в течение нескольких дней, поэтому уровни их воздействия были намного выше, чем у людей.[6]
Гадобутрол следует назначать беременным женщинам только в том случае, если потенциальная польза превышает риск для плода.[6][7]
Кормление грудью
Неизвестно, сколько гадобутрола попадает в молоко у человека. Имеются ограниченные данные об экскреции других GBCA с грудным молоком человека, но предполагают, что скорость переноса в грудное молоко составляет от 0,01% до 0,04% введенного материала. Доклинические данные по гадробутролу позволяют предположить, что менее 0,01% выделяется в грудное молоко при внутривенном введении рекомендованной дозы. Дальнейшие данные показывают, что всасывание через желудочно-кишечный тракт очень низкое (примерно 5%). Для обеспечения максимальной безопасности грудное вскармливание следует прекратить на 24 часа после приема гадобутрола и надлежащей утилизации любого молока.[6][7]
Педиатрия
Безопасность, эффективность и фармакокинетика хорошо изучены у детей в возрасте 2-17 лет. Было обнаружено, что корректировки рекомендованной дозы 0,1 мл / кг массы тела не требуется.[6][7]
Данные по безопасности и эффективности для детей в возрасте до 2 лет ограничены, но продемонстрировали, что в этой популяции можно использовать дозу 0,1 мл / кг массы тела. Тем не менее, рекомендуется использовать минимально возможную дозу и дать промежуток не менее 7 дней между дозами для выведения агента из организма.[7]
Гериатрия
Клинические данные показали, что нет никакой разницы в безопасности или эффективности гадобутрола у субъектов в возрасте 65 лет и старше по сравнению с лицами в возрасте до 65 лет. Нет никаких требуемых специальных мер предосторожности и / или корректировки дозы для людей без почечной недостаточности.[6][7]
Население с почечной недостаточностью
Перед приемом гадобутрола рекомендуется оценить почечную недостаточность у всех пациентов. В этих группах населения нет необходимости корректировать дозу, однако гадобутрол необходимо будет удалить из организма с помощью гемодиализа.[6]
Взаимодействия
Нет данных о лекарственном взаимодействии с гадобутролом. Однако его не следует смешивать с другими препаратами.[6]
Механизм действия
Гадобутрол - это парамагнитный макроциклический контрастный агент, вводимый внутривенно для использования в магнитно-резонансной томографии. Эффект усиления контраста является результатом нейтрального комплекса гадолиния и дигидроксигидроксиметилпропил-тетраазациклододекан-триуксусной кислоты (бутрол), который работает для уменьшения различий в временах продольной релаксации (T1) и различий во временах спин-спиновой или поперечной релаксации ( Т2). Эти времена релаксации в сочетании с различиями в плотности протонов ответственны за изменение интенсивности радиочастотных сигналов, которые способствуют визуализации тканей МРТ. Большее усиление сигнала и, следовательно, лучшая визуализация тканей достигается за счет увеличения укорочения T1 и T2.[7][8]
История
Коммерциализация
Гадобутрол был впервые одобрен в Швейцарии в 1998 году для использования в МРТ головного и спинного мозга с контрастным усилением. С тех пор он был одобрен и продан в 65 других странах, включая все страны Европейского Союза, США, Канаду, Мексику, Австралию, Новую Зеландию, Китай, Южную Корею, Россию и Бразилию, для множества применений.[9] Гадобутрол был впервые одобрен для использования в МРТ центральной нервной системы в США в 2011 году. В настоящее время он производится Bayer Healthcare Pharmaceuticals Inc. и продается под торговой маркой Gadavist.[9][10] В 2015 году Гадавист был одобрен FDA в качестве первого контрастного вещества, безопасного для использования у детей в возрасте до 2 лет. Совсем недавно, в начале 2016 года, Гадавист был одобрен в США для использования в магнитно-резонансной ангиографии с контрастным усилением.[10]
Исследования и клинические испытания
Гадавист был одобрен в Соединенных Штатах в 2011 году после представления результатов 43 клинических исследований, которые в основном проводились в Азии и Европейском Союзе, в дополнение к одному этапу 2 и двум клиническим испытаниям фазы 3, проведенным в Соединенных Штатах.[9] Многоцентровые рандомизированные двойные слепые клинические испытания фазы 3 (одно завершено без активной группы сравнения)[11] набрано 402 пациента старше 18 лет, направленных на МРТ ЦНС с контрастным усилением.[12] Каждый пациент получил однократную дозу гадобутрола (0,1 ммоль / кг массы тела) посредством внутривенной инъекции, а затем однократную дозу гадотеридола (ProHance) в утвержденной дозе (0,1 ммоль / кг массы тела) посредством внутривенной инъекции или наоборот. В исследовании оценивалась безопасность и эффективность гадобутрола. На основании этих клинических испытаний фазы 3 были сделаны следующие выводы:[9]
- Комбинированные изображения с улучшенным содержанием гадобутрола и без улучшения по сравнению с изображениями без улучшения:
- Превосходные диагностические характеристики
- Превосходно подходит для визуализации поражений: контрастное усиление, определение границ и внутренняя морфология
- Не уступает по количеству обнаруженных повреждений
- Было показано, что гадобутрол не уступает ProHance по параметрам визуализации: контрастному усилению, разграничению границ и внутренней морфологии, а также количеству обнаруженных повреждений.
- Гадобутрол показал более высокую чувствительность, чем ProHance, для определения злокачественности поражения.
- Все 3 слепых считывателя неизменно предпочитали изображения, усиленные гадобутролом, по сравнению с изображениями, улучшенными ProHance.
Перед одобрением для использования у детей в возрасте до 2 лет в 2015 году была проведена фаза 1 клинических испытаний. В исследование могут быть включены педиатрические пациенты, которым назначено плановое МРТ-исследование с контрастным усилением любой области тела, как мужчин, так и женщин, в возрасте до 2 лет. Открытый многоцентровый фармакокинетический тест и тест на безопасность изучали, как гадобутрол попадает, перемещается и выводится из организма младенцев. В исследовании также оценивалась безопасность, переносимость и эффективность стандартной дозы гадобутрола, 0,1 ммоль / кг (0,1 мл / кг) массы тела. Клиническое испытание спонсировалось Bayer Healthcare Pharmaceuticals Inc.[13]
Перед утверждением для использования в магнитно-резонансной ангиографии (МРА) в начале 2006 г. была проведена фаза 3 клинических испытаний. В исследование могут быть включены пациенты, направленные на обычную магнитно-резонансную ангиографию (МРА), как мужчины, так и женщины, в возрасте старше 18 лет. В открытом многоцентровом слепом исследовании безопасности и эффективности чтения сравнивались диагностические результаты МРА-изображений, усиленных гадобутролом, с неконтрастными МРА-изображениями. Перед сканированием пациенты получили однократную внутривенную инъекцию гадобутрола 0,1 ммоль / кг. Затем квалифицированный персонал вслепую прочитал результаты МРА-изображения. Клиническое испытание спонсировалось Bayer Healthcare Pharmaceuticals Inc.[14]
Нормативный
Единственный патент США на гадобутрол - US5980864A, выданный 9 ноября 1999 г. компании Schering AG.[15] Патент на процесс с использованием 1,4,7,10-тетраазациклододекана бутилтриолов для получения гадолиниевого (III) комплекса 10- (1-гидроксиметил-2,3-дигидроксипропил) -1,4,7-трискарбоксиметил-1, 4,7,10-тетраазациклододекан (гадобутрол). Патент защищает использование этого металлического комплекса в качестве превосходной диагностической среды. В 2006 году Bayer Healthcare Pharmaceuticals Inc. поглотила Schering AG, а в ноябре 2007 года патент был передан компании Bayer Schering Pharma. После одобрения FDA в 2011 году срок действия патента был продлен на 1470 дней, и торговое название Gadavist стало ассоциироваться с патентом. В феврале 2016 года патент был продлен на второй срок, но истек в ноябре 2016 года.[16]
Упаковка и покупка
Контрастное средство гадобутрол представляет собой прозрачный раствор от бесцветного до бледно-желтого цвета с концентрацией 1 ммоль / мл, доступный во флаконах с разовой дозой (2 мл, 7,5 мл, 10 мл и 15 мл), предварительно заполненные однократные дозы (7,5 мл, 10 мл, 15 мл) и аптечные оптовые упаковки (30 мл и 65 мл), содержащие несколько флаконов.[17] Гадобутрол в настоящее время продается в Соединенных Штатах под названием Гадавист, а в большинстве других стран - под названием Гадовист или Гадовист 1.0.[9]
Гадобутрол не отпускается по рецепту и может вводиться только обученным персоналом. В 2016 году компания Bayer-UK опубликовала цены на продукт.[18]
использованная литература
- ^ Ченг К.Т. (2007). «Гадобутрол» (PDF). База данных молекулярной визуализации и контрастного вещества (MICAD). Национальный центр биотехнологической информации (NCBI). PMID 20641787. NBK23589.
- ^ «Байер в радиологии - Гадавист® (гадобутрол) для инъекций 1 ммоль / мл». bayerimaging.com. Получено 20 мая 2015.
- ^ «FDA одобряет визуализирующий агент для сканирования центральной нервной системы» (Пресс-релиз). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA). 15 марта 2011 г.. Получено 31 марта, 2011.
- ^ «FDA США одобряет инъекцию гадависта (гадобутрола) компании Bayer для МРТ центральной нервной системы» (Пресс-релиз). Bayer HealthCare Pharmaceuticals. 14 марта 2011 г. Архивировано с оригинал 2 мая 2011 г.. Получено 31 марта, 2011.
- ^ «Образование для специалистов в области кардиологии» (PDF). touchcardiology.com. Radcliffecardiology. Получено 20 мая 2015.
- ^ а б c d е ж грамм час я j k л м п о «Полная информация о назначении препарата Гадавист» (PDF). Получено 2011-03-14.
- ^ а б c d е ж грамм час я «Монография ГадовистПродукт» (PDF). Bayer Inc., 12 августа 2016 г.. Получено 11 ноября, 2016.
- ^ «Гадобутрол». DrugBank. 2016-11-19.
- ^ а б c d е «Информационный документ для инъекций гадобутрола, NDA 201 277» (PDF). FDA.Gov. Управление по контролю за продуктами и лекарствами. 21 января 2011 г.. Получено 11 ноября, 2016.
- ^ а б «История одобрения Gadavist (гадобутрол) FDA». www.drugs.com. Получено 2016-11-19.
- ^ Стинсон Б. (6 марта 2009 г.). «Клиническое обозрение» (PDF). FDA.Gov. FDA. Получено 11 ноября, 2016.
- ^ «Безопасность и эффективность Gadobutrol 1.0 Molar (Gadavist) у пациентов для визуализации центральной нервной системы (ЦНС)». ClinicalTrials.gov. Получено 2016-11-19.
- ^ "Исследование фармакокинетики и безопасности гадобутрола у детей в возрасте <2 лет". ClinicalTrials.gov. Получено 2016-11-19.
- ^ «МРА супрааортальных сосудов с усилением гадобутролом». ClinicalTrials.gov. Получено 2016-11-19.
- ^ Платцек Дж., Грис Х., Вайнманн Х., Шуман-Джампьери Дж., Press W (9 ноября 1999 г.), 1,4,7,10-тетраазациклододеканбутилтриолы, способы их получения и фармацевтические агенты, содержащие их, получено 2016-11-19
- ^ «Патент US5980864A». Патенты Google. Получено 4 марта, 2019.
- ^ «Байер в радиологии | Гадавист® (гадобутрол) для инъекций 1 ммоль / мл». www.radiologysolutions.bayer.com. Получено 2016-11-20.
- ^ «Прейскурант на 2016 год» (PDF). Байер-Великобритания. 16 июня 2016 г.. Получено 19 ноября, 2016.
