Флуоресцентный микроскоп - Fluorescence microscope

А флуоресцентный микроскоп является оптический микроскоп который использует флуоресценция вместо или в дополнение к рассеяние, отражение, и затухание или же поглощение, чтобы изучить свойства органических или неорганический вещества.[1][2] «Флуоресцентный микроскоп» относится к любому микроскопу, который использует флуоресценцию для создания изображения, будь то более простая установка, такая как эпифлуоресцентный микроскоп, или более сложная конструкция, такая как конфокальный микроскоп, который использует оптическое сечение для получения лучшего разрешения флуоресцентного изображения.[3]
Принцип
Образец освещается светом определенного длина волны (или длины волн), который поглощается флуорофоры, заставляя их излучать свет с большей длиной волны (т. е. другого цвета, чем поглощенный свет). Освещающий свет отделяется от гораздо более слабой излучаемой флуоресценции с помощью спектрального эмиссионного фильтра. Типичными компонентами флуоресцентного микроскопа являются источник света (ксеноновая дуговая лампа или же ртутная лампа общие; более продвинутые формы обладают высокой мощностью Светодиоды и лазеры ), фильтр возбуждения, то дихроичное зеркало (или же дихроичный светоделитель ), а эмиссионный фильтр (см. рисунок ниже). Фильтры и дихроичный светоделитель выбираются в соответствии со спектральными характеристиками возбуждения и излучения флуорофора, используемого для маркировки образца.[1] Таким образом, одновременно отображается распределение одного флуорофора (цвета). Многоцветные изображения нескольких типов флуорофоров необходимо составлять путем объединения нескольких одноцветных изображений.[1]
Большинство используемых флуоресцентных микроскопов представляют собой эпифлуоресцентные микроскопы, в которых возбуждение флуорофора и обнаружение флуоресценции осуществляются через один и тот же световой путь (то есть через объектив). Эти микроскопы широко используются в биологии и являются основой для более совершенных конструкций микроскопов, таких как конфокальный микроскоп и флуоресцентный микроскоп полного внутреннего отражения (TIRF).
Эпифлуоресцентная микроскопия

Большинство флуоресцентных микроскопов, особенно используемых в Науки о жизни, имеют схему эпифлуоресценции, показанную на диаграмме. Свет с длиной волны возбуждения освещает образец через цель линза. В флуоресценция испускаемый образцом фокусируется на детекторе тем же объективом, который используется для возбуждения, что для большего разрешения потребует линзы объектива с более высоким разрешением. числовая апертура. Поскольку большая часть возбуждающего света проходит через образец, только отраженный возбуждающий свет достигает объектива вместе с испускаемым светом, и поэтому метод эпифлуоресценции дает высокое отношение сигнал / шум. Дихроичный светоделитель действует как фильтр для определенной длины волны, пропускающий флуоресцентный свет через окуляр или детектор, но отражающий оставшийся возбуждающий свет обратно к источнику.
Источники света
Флуоресцентная микроскопия требует интенсивного, почти монохроматического освещения, которое некоторые широко распространенные источники света, такие как галогенные лампы не могу предоставить.[4] Используются четыре основных типа источников света, в том числе ксеноновые дуговые лампы или же ртутные лампы с фильтр возбуждения, лазеры, суперконтинуум источники и мощные Светодиоды. Лазеры наиболее широко используются для более сложных методов флуоресцентной микроскопии, таких как конфокальная микроскопия и флуоресцентная микроскопия полного внутреннего отражения и ксеноновые лампы, и ртутные лампы, и светодиоды с дихроичный возбуждающий фильтр обычно используется для широкопольных эпифлуоресцентных микроскопов. Поместив два микролинза решетки в световой тракт широкоугольного эпифлуоресцентного микроскопа,[5] очень равномерное освещение с коэффициент вариации 1-2% может быть достигнуто.
Базовые приготовления
Отображает наложения с четырех флуоресцентных каналов
(b) Голубой: [флуоресценция PLL-A546] - общий контраст для визуализации поверхностей эукариотических клеток.
(c) Синий: [флуоресценция Hoechst] - окрашивает ДНК, идентифицирует ядра.
(d) Красный: [автофлуоресценция хлорофилла] - рассасывает хлоропласты.[6]

Чтобы образец подходил для флуоресцентной микроскопии, он должен быть флуоресцентным. Есть несколько методов создания флуоресцентного образца; основные методы - это маркировка флуоресцентными красителями или, в случае биологических образцов, выражение из флуоресцентный белок. В качестве альтернативы собственная флуоресценция образца (т. Е. автофлуоресценция ) может быть использован.[1] В биологических науках флуоресцентная микроскопия является мощным инструментом, позволяющим специфическое и чувствительное окрашивание образца для определения распределения белки или другие представляющие интерес молекулы. В результате существует широкий спектр методов флуоресцентного окрашивания биологических образцов.
Биологические флуоресцентные пятна
Многие флуоресцентные красители были разработаны для ряда биологических молекул. Некоторые из них представляют собой небольшие молекулы, которые по своей природе флуоресцентны и связывают интересующую биологическую молекулу. Основные примеры из них: нуклеиновая кислота пятна, такие как DAPI и Hoechst (возбуждаемые ультрафиолетовым светом) и DRAQ5 и DRAQ7 (оптимально возбуждаемые красным светом), которые связывают малую бороздку ДНК, таким образом маркируя ядра ячеек. Другие - лекарства, токсины или пептиды, которые связывают определенные клеточные структуры и были модифицированы с помощью флуоресцентного репортера. Основным примером этого класса флуоресцентных красителей является фаллоидин, который используется для окрашивания актин волокна в млекопитающее клетки. Новый пептид, известный как Коллагеновый гибридизующий пептид, также может быть сопряжен с флуорофоры и использовался для окрашивания денатурированный коллагеновые волокна. Окрашивание растения клеточные стенки выполняется с использованием морилки или красителей, связывающих целлюлоза или же пектин. Поиски флуоресцентных зондов с высокой специфичностью, которые также позволяют получать изображения растительных клеток в реальном времени, продолжаются.[7]
Есть много флуоресцентных молекул, называемых флуорофоры или же флуорохромы Такие как флуоресцеин, Алекса Флуорс, или же DyLight 488, который может быть химически связан с другой молекулой, которая связывает интересующую мишень в образце.
Иммунофлуоресценция
Иммунофлуоресценция - это метод, в котором используется высокоспецифичное связывание антитело к его антиген чтобы маркировать определенные белки или другие молекулы внутри клетки. Образец обрабатывают первичным антителом, специфичным для интересующей молекулы. Флуорофор можно напрямую конъюгировать с первичным антителом. В качестве альтернативы вторичное антитело, конъюгированный с флуорофором, который специфически связывается с первым антителом. Например, первичное антитело мыши, которое распознает тубулин в сочетании со вторичным антимышиным антителом, дериватизированным с флуорофором, можно использовать для мечения микротрубочки в камере.
Флуоресцентные белки
Современное понимание генетика а методы, доступные для модификации ДНК, позволяют ученым генетически модифицировать белки, чтобы они также несли флуоресцентный белковый репортер. В биологических образцах это позволяет ученому непосредственно сделать интересующий белок флуоресцентным. Затем можно напрямую отслеживать местоположение белка, в том числе в живых клетках.
Ограничения
Флуорофоры теряют способность к флуоресценции, когда они освещаются в процессе, называемом фотообесцвечивание. Фотообесцвечивание происходит, когда флуоресцентные молекулы накапливают химические повреждения от электронов, возбужденных во время флуоресценции. Фотообесцвечивание может сильно ограничить время, в течение которого образец можно наблюдать с помощью флуоресцентной микроскопии. Существует несколько методов уменьшения фотообесцвечивания, таких как использование более надежных флуорофоров, минимизация освещения или использование фотозащитных материалов. мусорщик химикаты.
Флуоресцентная микроскопия с использованием флуоресцентных репортерных белков позволила анализировать живые клетки с помощью флуоресцентной микроскопии, однако клетки чувствительны к фототоксичности, особенно при использовании коротковолнового света. Кроме того, флуоресцентные молекулы имеют тенденцию генерировать химически активные химические вещества при освещении, что усиливает фототоксический эффект.
В отличие от методов микроскопии в проходящем и отраженном свете, флуоресцентная микроскопия позволяет наблюдать только определенные структуры, помеченные как флуоресцентные. Например, наблюдение за образцом ткани, приготовленным с использованием флуоресцентного окрашивания ДНК, с помощью флуоресцентной микроскопии показывает только организацию ДНК внутри клеток и ничего больше не показывает о морфологии клеток.
Субдифракционные методы
Волновая природа света ограничивает размер пятна, на которое он может быть сфокусирован из-за предел дифракции. Это ограничение было описано в XIX веке Эрнст Аббе и «ограничивает разрешение оптического микроскопа примерно половиной длины волны используемого света». Флуоресцентная микроскопия занимает центральное место во многих методах, которые стремятся преодолеть этот предел с помощью специализированных оптических конфигураций.
В 20-м веке были изобретены несколько усовершенствований в методах микроскопии, которые в некоторой степени привели к увеличению разрешения и контрастности. Однако они не преодолели дифракционный предел. В 1978 году были разработаны первые теоретические идеи по преодолению этого барьера путем использования 4Pi микроскопа в качестве конфокального лазерного сканирующего флуоресцентного микроскопа, в котором свет фокусируется идеально со всех сторон в общий фокус, который используется для сканирования объекта «точка за точкой». точечное возбуждение в сочетании с обнаружением «точка за точкой».[8]Однако первая экспериментальная демонстрация микроскопа 4pi состоялась в 1994 году.[9] 4Pi микроскопия максимизирует количество доступных направлений фокусировки за счет использования двух противоположных линз объектива или микроскопия с двухфотонным возбуждением с использованием красного смещения света и многофотонного возбуждения.
Интегрированный корреляционная микроскопия объединяет флуоресцентный микроскоп с электронным микроскопом. Это позволяет визуализировать ультраструктуру и контекстную информацию с помощью электронного микроскопа, используя данные флуоресцентного микроскопа в качестве инструмента маркировки.[10]
Первым методом, действительно позволившим достичь субдифракционного разрешения, было STED-микроскопия, предложенный в 1994 году. Этот метод и все техники, следующие за RESOLFT Концепция основана на сильном нелинейном взаимодействии между светом и флуоресцентными молекулами. Молекулы сильно движутся между различимыми молекулярными состояниями в каждом конкретном месте, так что, наконец, свет может испускаться только в небольшой части пространства, следовательно, повышенное разрешение.
Также в 1990-х годах был разработан другой метод микроскопии сверхвысокого разрешения, основанный на широко-полевой микроскопии. Значительно улучшенное разрешение сотовой связи по размеру наноструктуры окрашивание флуоресцентным маркером было достигнуто за счет развития микроскопии локализации SPDM и структурированного лазерного освещения (пространственно-модулированное освещение, SMI).[11] Сочетание принципа SPDM с SMI привело к развитию Вертико СМИ микроскоп.[12][13] Обнаружение одной молекулы нормального мигает флуоресцентные красители, подобные зеленый флуоресцентный белок (GFP) может быть достигнута за счет дальнейшего развития SPDM, так называемой технологии SPDMphymod, которая позволяет обнаруживать и подсчитывать два разных типа флуоресцентных молекул на молекулярном уровне (эта технология называется двухцветной микроскопией локализации или 2CLM. ).[14]
Как вариант, появление фотоактивированная локализационная микроскопия может достичь аналогичных результатов, полагаясь на мигание или переключение одиночных молекул, где доля флуоресцирующих молекул в каждый момент времени очень мала. Этот стохастический отклик молекул на приложенный свет также соответствует сильно нелинейному взаимодействию, ведущему к субдифракционному разрешению.
Галерея флуоресцентных микрофотографий

Z-проекция клетки остеосаркомы, окрашенная фаллоидином для визуализации актиновых нитей. Изображение было снято на конфокальном микроскопе, а последующая деконволюция была выполнена с использованием экспериментально полученной функции рассеяния точки.
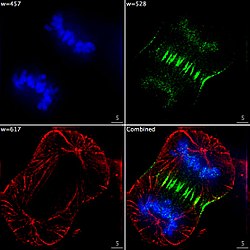
Эпифлуоресцентное изображение трех компонентов делящейся раковой клетки человека. ДНК окрашен в синий цвет, а белок называется INCENP зеленый, а микротрубочки красные. Каждый флуорофор отображается отдельно с использованием другой комбинации фильтров возбуждения и излучения, и изображения снимаются последовательно с помощью цифрового CCD камера, затем наложили, чтобы получить полное изображение.

Эндотелиальные клетки под микроскопом. Ядра окрашены в синий цвет с помощью DAPI, микротрубочки помечены зеленым цветом по антителу, связанному с FITC, а филаменты актина помечены красным цветом с фаллоидином, связанным с TRITC. Эндотелиальные клетки легочной артерии крупного рогатого скота (BPAE)
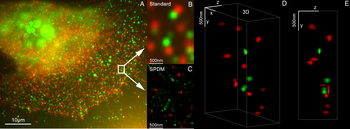
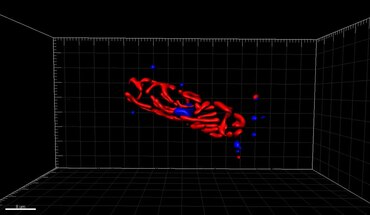
Двухцветная трехмерная микроскопия сверхвысокого разрешения с Her2 и Her3 в клетках молочной железы, стандартные красители: Alexa 488, Alexa 568. Микроскопия LIMON

Ядро лимфоцитов человека, окрашенное DAPI, с гибридизированными зондами хромосомы 13 (зеленый) и 21 (красный) центромеры (Флуоресцентная гибридизация in situ (РЫБЫ))

Мембрана дрожжевых клеток визуализируется некоторыми мембранными белками, слитыми с флуоресцентными маркерами RFP и GFP. Наложение света от обоих маркеров приводит к желтому цвету.

Микроскопия сверхвысокого разрешения: обнаружение одной молекулы YFP в раковой клетке человека. Типичные измерения расстояний в диапазоне 15 нм измерено с помощью микроскопа Vertico-SMI / SPDMphymod
Микроскопия сверхвысокого разрешения: Совместная локализационная микроскопия (2CLM) с белками слияния GFP и RFP (ядро клетки рака кости) 120 000 локализованных молекул в широкой области (470 мкм2) измерено с помощью микроскопа Vertico-SMI / SPDMphymod

Флуоресцентная микроскопия экспрессии ДНК у человека дикого типа и мутанта P239S Палладин.

На изображениях флуоресцентной микроскопии патологии солнечных вспышек в клетке крови пораженные участки показаны красным цветом.
Смотрите также
- Флуоресцентная визуализация
- Флуоресценция в науках о жизни
- Корреляционная свето-электронная микроскопия
- Элизабет Гарри, пионер методов флуоресцентной микроскопии для визуализации бактериальных субклеточных белков
- Зеленый флуоресцентный белок (GFP)
- Лампа ртутно-паровая
- Микроскоп
- Сканирующий электронный микроскоп # Катодолюминесценция
- Стоксов сдвиг
- Ксеноновая дуговая лампа
Рекомендации
- ^ а б c d Весна KR, Дэвидсон MW. «Введение в флуоресцентную микроскопию». Nikon MicroscopyU. Получено 28 сентября 2008.
- ^ «Флуоресцентный микроскоп». Микроскопы - помогите ученым исследовать скрытые миры. Нобелевский фонд. Получено 28 сентября 2008.
- ^ Хуан Карлос Штокерт, Альфонсо Бласкес-Кастро (2017). Флуоресцентная микроскопия в науках о жизни. Издательство Bentham Science. ISBN 978-1-68108-519-7. Получено 17 декабря 2017.
- ^ Хуан Б. (март 2010 г.). «Флуоресцентная микроскопия сверхвысокого разрешения». Ежегодный обзор биохимии. Дои:10.1146 / annurev.biochem.77.061906.092014. PMID 19489737. Получено 29 сентября 2020. Цитировать журнал требует
| журнал =(помощь) - ^ F.A.W. Coumans; Э. ван дер Поль; L.W.M.M. Терстаппен (2012). «Профиль освещения с плоским верхом в эпифлуоресцентном микроскопе с помощью двух массивов микролинз». Цитометрия Часть А. 81 (4): 324–331. Дои:10.1002 / cyto.a.22029. PMID 22392641. S2CID 13812696.
- ^ Колин, С., Коэльо, Л.П., Сунагава, С., Боулер, К., Карсенти, Э., Борк, П., Пепперкок, Р. и Де Варгас, К. (2017) «Количественная 3D-визуализация для клеточной биологии. и экология экологических микробных эукариот ». eLife, 6: e26066. Дои:10.7554 / eLife.26066.002.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Бидхенди, AJ; Chebli, Y; Гайтманн, А (май 2020 г.). «Визуализация флуоресценции целлюлозы и пектина в первичной клеточной стенке растений». Журнал микроскопии. 278 (3): 164–181. Дои:10.1111 / jmi.12895. PMID 32270489.
- ^ Cremer, C; Кремер, Т. (1978). «Соображения по поводу лазерного сканирующего микроскопа с высоким разрешением и глубиной резкости» (PDF). Microscopica Acta. 81 (1): 31–44. PMID 713859.
- ^ С.В. Ад, E.H.K. Стельцер, С. Линдек, К. Кремер; Штельцер; Линдек; Кремер (1994). «Конфокальная микроскопия с увеличенной апертурой обнаружения: конфокальная микроскопия типа B 4Pi». Письма об оптике. 19 (3): 222–224. Bibcode:1994OptL ... 19..222H. CiteSeerX 10.1.1.501.598. Дои:10.1364 / OL.19.000222. PMID 19829598.CS1 maint: несколько имен: список авторов (связь)
- ^ Баарле, Кейтлин ван. «Корреляционная микроскопия: открытие мира информации с помощью флуоресценции». Получено 16 февраля 2017.
- ^ Хаусманн, Майкл; Шнайдер, Бернхард; Брадл, Иоахим; Кремер, Кристоф Г. (1997), «Высокоточная дистанционная микроскопия 3D наноструктур с помощью флуоресцентного микроскопа с пространственно модулированным возбуждением» (PDF), в Бигио, Ирвинг Дж; Шнекенбургер, Герберт; Славик, Ян; и другие. (ред.), Оптическая биопсия и микроскопические методы II, Оптическая биопсия и микроскопические методы II, 3197, п. 217, Дои:10.1117/12.297969, S2CID 49339042
- ^ Рейманн, Дж; Баддели, Д.; Гункель, М; Lemmer, P; Стадтер, Вт; Jegou, T; Риппе, К; Cremer, C; Бирк, У (2008). «Высокоточный структурный анализ субядерных комплексов в фиксированных и живых клетках с помощью микроскопии с пространственно-модулированным освещением (SMI)» (PDF). Хромосомные исследования: международный журнал по молекулярным, супрамолекулярным и эволюционным аспектам хромосомной биологии. 16 (3): 367–82. Дои:10.1007 / s10577-008-1238-2. PMID 18461478. S2CID 22811346.
- ^ Баддели, Д.; Батрам, C; Вейланд, Y; Cremer, C; Бирк, UJ (2003). «Анализ наноструктур с использованием микроскопии с пространственно-модулированным освещением» (PDF). Протоколы природы. 2 (10): 2640–6. Дои:10.1038 / nprot.2007.399. PMID 17948007. S2CID 22042676.[мертвая ссылка ]
- ^ Гункель, М; Erdel, F; Риппе, К; Lemmer, P; Кауфманн, Р. Hörmann, C; Amberger, R; Кремер, С. (2009). «Двухцветная локализационная микроскопия клеточных наноструктур» (PDF). Биотехнологический журнал. 4 (6): 927–38. Дои:10.1002 / biot.200900005. PMID 19548231. S2CID 18162278.
внешняя ссылка
| Библиотечные ресурсы о Флуоресцентная микроскопия |
- Fluorophores.org[постоянная мертвая ссылка ], база данных флуоресцентных красителей
- Ресурсный центр по микроскопии
- анимации и пояснения к различным типам микроскопов, включая флуоресцентные и конфокальные микроскопы (Université Paris Sud)