Клеточная активность - Cell potency
Клеточная активность это клетки способность к различать в другие типы клеток.[1][2][3]Чем в большее количество типов клеток может дифференцироваться клетка, тем выше ее эффективность. Сила также описывается как потенциал активации гена внутри клетки, который, как континуум, начинается с тотипотентность для обозначения клетки с наибольшим потенциалом дифференцировки, плюрипотентность, мультипотентность, олигопотентность, и наконец униженность.

Тотипотентность
Тотипотентность (лат. тотипотенция, "способность ко всему [вещам]") - это способность одного клетка делить и производить все дифференцированные клетки в организм. Споры и зиготы являются примерами тотипотентных клеток.[4]В спектре активности клеток тотипотентность представляет собой клетку с наибольшим дифференциация потенциал, способность дифференцировать в любой эмбриональный клетка, а также внеэмбриональные клетки. Напротив, плюрипотентные клетки могут дифференцироваться только в эмбриональные клетки.[5][6]
Полностью дифференцированная клетка может вернуться в состояние тотипотентности.[7] Это преобразование в тотипотентность сложно, не до конца изучено и является предметом недавних исследований. Исследования 2011 года показали, что клетки могут дифференцироваться не в полностью тотипотентную клетку, а вместо этого в «сложную клеточную вариацию» тотипотентности.[8] Стволовые клетки, напоминающие тотипотент бластомеры из эмбрионов на двухклеточной стадии могут возникать спонтанно в культурах эмбриональных стволовых клеток мыши[9][10] а также могут возникать чаще in vitro через понижающее регулирование хроматин монтажная деятельность CAF-1.[11]
Модель развития человека может быть использована для описания того, как возникают тотипотентные клетки.[12] Человеческое развитие начинается, когда сперма оплодотворяет яйцеклетку, и в результате оплодотворенной яйцеклетки образуется единственная тотипотентная клетка, зигота.[13] В первые часы после оплодотворения эта зигота делится на идентичные тотипотентные клетки, которые впоследствии могут развиться в любой из трех зародышевых листков человека (энтодерма, мезодерма, или же эктодерма ), либо в ячейки плацента (цитотрофобласт или же синцитиотрофобласт ). Достигнув стадии 16 клеток, тотипотентные клетки морула дифференцируются в клетки, которые в конечном итоге станут бластоциста с Внутренняя клеточная масса или внешний трофобласты. Примерно через четыре дня после оплодотворения и после нескольких циклов клеточного деления эти тотипотентные клетки начинают специализироваться. Внутренняя клеточная масса, источник эмбриональные стволовые клетки, становится плюрипотентным.
Исследования по Caenorhabditis elegans предполагает, что несколько механизмов, включая Регулирование РНК может играть роль в поддержании тотипотенции на разных этапах развития у некоторых видов.[14] Работать с данио и млекопитающие предполагают дальнейшее взаимодействие между miRNA и РНК-связывающие белки (ОДП) в определении различий в развитии.[15]
Первичные половые клетки
В исконной мыши стволовые клетки, геном - широкое перепрограммирование, ведущее к тотипотентности, включает стирание эпигенетический отпечатки. Перепрограммированию способствует активная Деметилирование ДНК с участием ДНК базовая эксцизионная пластика ферментативный путь.[16] Этот путь влечет за собой стирание CpG метилирование (5mC) в первичных половых клетках через начальное превращение 5mC в 5-гидроксиметилцитозин (5hmC), реакция, вызванная высокими уровнями энзимов диоксигеназы десять-одиннадцать. ТЭЦ-1 и ТЭЦ-2.[17]
Плюрипотентность
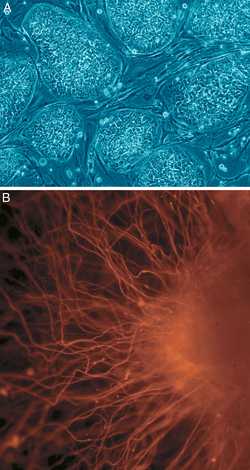
В клеточной биологии плюрипотентность (лат. плюрипотенция, "способность ко многим [вещам]")[18] относится к стволовым клеткам, которые могут различать в любой из трех ростковые отростки: энтодерма (внутренняя оболочка желудка, желудочно-кишечный тракт, легкие), мезодерма (мышцы, кости, кровь, мочеполовые органы) или эктодерма (эпидермальные ткани и нервная система), но не во внеэмбриональные ткани, такие как плацента.[19] Однако плюрипотентность клеток - это континуум, начиная от полностью плюрипотентной клетки, которая может образовывать каждую клетку собственно эмбриона, например, эмбриональные стволовые клетки и ИПСК (см. Ниже), до частично или частично плюрипотентной клетки, которая может формировать клетки всех трех зародышевые листки, но они могут не обладать всеми характеристиками полностью плюрипотентных клеток.
Индуцированная плюрипотентность
Индуцированные плюрипотентные стволовые клетки, обычно обозначаемые как iPS-клетки или iPSCs, представляют собой тип плюрипотентных стволовая клетка искусственно полученный из не плюрипотентной клетки, обычно взрослого Соматическая клетка, вызывая "принудительное" выражение определенных гены и факторы транскрипции.[20] Эти факторы транскрипции играют ключевую роль в определении состояния этих клеток, а также подчеркивают тот факт, что эти соматические клетки действительно сохраняют ту же генетическую информацию, что и ранние эмбриональные клетки.[21] Способность приводить клетки в плюрипотентное состояние была впервые обнаружена в 2006 году с использованием мышей. фибробласты и четыре фактора транскрипции, 4 октября, Sox2, Klf4 и c-Мой с;[22] этот метод, называемый перепрограммирование, позже заработал Шинья Яманака и Джон Гэрдон Нобелевская премия по физиологии и медицине.[23] Затем в 2007 году последовала успешная индукция ИПСК человека, полученных из фибробластов кожи человека, с использованием методов, аналогичных тем, которые используются для индукции клеток мыши.[24] Эти индуцированные клетки обладают сходными чертами с эмбриональными стволовыми клетками (ЭСК), но не требуют использования эмбрионов. Некоторые из сходств между ESC и iPSC включают: плюрипотентность, морфология, способность к самообновлению, черта, которая подразумевает, что они могут делиться и воспроизводиться бесконечно, и экспрессия гена.[25]
Эпигенетический Также считается, что факторы участвуют в фактическом перепрограммировании соматических клеток, чтобы вызвать плюрипотентность. Было высказано предположение, что некоторые эпигенетический факторы могут действительно работать, чтобы очистить исходное соматическое эпигенетический меток, чтобы получить новые эпигенетические метки, которые являются частью достижения плюрипотентный государственный. Хроматин также реорганизуется в ИПСК и становится таким же, как в ЭСК, в том смысле, что он менее конденсирован и, следовательно, более доступен. Эухроматин модификации также распространены, что также согласуется с состоянием эухроматин найдено в ESC.[25]
Из-за большого сходства с ESC, ИПСК вызывают большой интерес у медицинского и исследовательского сообщества. ИПСК потенциально могут иметь такое же терапевтическое значение и применение, что и ЭСК, но без неоднозначного использования эмбрионов в процессе, что является предметом больших биоэтических дебатов. Фактически, индуцированный плюрипотентность из соматические клетки в недифференцированный iPS клетки первоначально был провозглашен концом спорно использование из эмбриональные стволовые клетки. Однако было обнаружено, что ИПСК потенциально онкогенный, и, несмотря на успехи,[20] никогда не были одобрены для клинических исследований в США. При создании ИПСК также встречались такие неудачи, как низкая скорость репликации и раннее старение.[26] препятствуя их использованию в качестве замены ESC.
Кроме того, было установлено, что соматическая экспрессия комбинированного факторы транскрипции может напрямую вызывать судьбу других определенных соматических клеток (трансдифференциация ); исследователи определили три фактора транскрипции, специфичных для нейронального происхождения, которые могут напрямую преобразовывать мышиные фибробласты (клетки кожи) в полностью функциональные нейроны.[27] Этот результат ставит под сомнение терминальную природу клеточная дифференциация и целостность преданности родословной; и подразумевает, что с соответствующими инструментами, все клетки тотипотент и может образовывать все виды тканей.
Некоторые из возможных медицинских и терапевтических применений ИПСК, полученных от пациентов, включают их использование при трансплантации клеток и тканей без риска отторжения, с которым обычно сталкиваются. ИПСК потенциально могут заменить неподходящие модели животных, а также in vitro модели, используемые для исследования болезней.[28]

Наивные и праймированные состояния плюрипотентности
Недавние открытия в отношении эпибласты до и после имплантации предложили разделить плюрипотентность на две отдельные фазы: «наивную» и «подготовленную».[29] Базовые стволовые клетки, обычно используемые в науке, которые называются эмбриональными стволовыми клетками (ЭСК), происходят из предимплантационного эпибласта; такой эпибласт способен генерировать весь плод, и одна клетка эпибласта может вносить вклад во все клеточные клоны при введении в другую бластоцисту. С другой стороны, можно наблюдать несколько заметных различий между до- и постимплантационными эпибластами, например, их различие в морфологии, при которой эпибласт после имплантации меняет свою морфологию на чашевидную форму, называемую «яйцевидным цилиндром», поскольку а также хромосомное изменение, при котором одна из Х-хромосом подвергается случайной инактивации на ранней стадии цилиндра яйца, известное как X-инактивация.[30] Во время этого развития клетки эпибласта цилиндра яйца систематически становятся мишенью для Факторы роста фибробластов, Wnt передача сигналов и другие индуктивные факторы через окружающий желточный мешок и ткань трофобласта,[31] так что они становятся поучительно конкретными в соответствии с пространственной организацией.[32]
Другое важное различие, которое наблюдалось в отношении активности клеток, заключается в том, что стволовые клетки эпибласта после имплантации не могут вносить вклад в образование бластоцисты. химеры,[33] что отличает их от других известных плюрипотентных стволовых клеток. Клеточные линии, полученные из таких постимплантационных эпибластов, называются стволовые клетки, полученные из эпибласта которые впервые были получены в лаборатории в 2007 году; несмотря на их номенклатуру, как ESC, так и EpiSC происходят из эпибластов, как раз на разных фазах развития, и что плюрипотентность в постимплантационном эпибласте все еще не нарушена, что демонстрируется консервативной экспрессией Наног, Fut4, и Октябрь-4 в EpiSCs,[34] до того как сомитогенез и может быть отменен на полпути путем индуцированной экспрессии Октябрь-4.[35]
Мультипотентность

Мультипотентность описывает клетки-предшественники которые обладают потенциалом активации генов для дифференциации на отдельные типы клеток. Например, мультипотентный кровь стволовые клетки - и этот тип клеток может дифференцироваться в несколько типов клеток крови, таких как лимфоциты, моноциты, нейтрофилы и т. д., но вопрос о том, HSC обладают способностью дифференцировать клетки мозга, костные клетки или другие типы клеток, не относящиеся к крови.[нужна цитата ]
Новое исследование, связанное с мультипотентными клетками, предполагает, что мультипотентные клетки могут превращаться в неродственные типы клеток. В другом случае стволовые клетки пуповинной крови человека были преобразованы в нейроны человека.[36] Исследования также сосредоточены на превращении мультипотентных клеток в плюрипотентный клетки.[37]
Мультипотентные клетки обнаруживаются во многих, но не во всех типах клеток человека. Мультипотентные клетки были обнаружены в пуповинная кровь,[38] жировая ткань,[39] сердечные клетки,[40] костный мозг и мезенхимальные стволовые клетки (МСК), которые находятся в третий моляр.[41]
МСК могут оказаться ценным источником стволовых клеток моляров в возрасте 8–10 лет, до кальцификации зубов у взрослых. МСК могут дифференцироваться на остеобласты, хондроциты и адипоциты.[42]
Олигопотентность
В биологии олигопотентность - это способность клетки-предшественники разделить на несколько типы клеток. Это степень потенция. Примерами олигопотентных стволовых клеток являются лимфоидные или миелоидные стволовые клетки.[2]В частности, лимфоидная клетка может давать начало различным клеткам крови, таким как В- и Т-клетки, но не к другому типу клеток крови, например к эритроцитам.[43] Примерами клеток-предшественников являются сосудистые стволовые клетки, способные одновременно становиться эндотелиальный или гладкомышечные клетки.
Унипотентность
В клеточная биология, унипотентная клетка - это концепция, согласно которой одна стволовая клетка способна дифференцироваться только в один тип клеток. В настоящее время неясно, существуют ли истинные унипотентные стволовые клетки. Гепатобласты, которые дифференцируются на гепатоциты (которые составляют большую часть печень ) или же холангиоциты (эпителиальные клетки желчного протока), бипотентны.[44] Близкий синоним слова унипотентная клетка является клетка-предшественник.
Смотрите также
Рекомендации
- ^ Тотипотентность клеток была открыта Хабертландом, а термин был придуман Томасом Хандом Морганом.Махла RS (2016). «Применение стволовых клеток в регенеративной медицине и трепевтике болезней». Международный журнал клеточной биологии. 2016 (7): 19. Дои:10.1155/2016/6940283. ЧВК 4969512. PMID 27516776.
- ^ а б Ханс Р. Шелер (2007). «Возможности стволовых клеток: перечень». В Николаусе Кнёпффлере; Дагмар Шипански; Стефан Лоренц Зоргнер (ред.). Биотехнология человека как социальный вызов. ООО "Ашгейт Паблишинг" с. 28. ISBN 978-0-7546-5755-2.
- ^ «Школа стволовых клеток: глоссарий».[мертвая ссылка ]
- ^ Миталипов С, Вольф Д. (2009). «Тотипотентность, плюрипотентность и ядерное репрограммирование». Инженерия стволовых клеток. Достижения в области биохимической инженерии / биотехнологии. 114. С. 185–199. Bibcode:2009esc..book..185M. Дои:10.1007/10_2008_45. ISBN 978-3-540-88805-5. ЧВК 2752493. PMID 19343304.
- ^ Лодиш, Харви (2016). Молекулярная клеточная биология, 8-е изд.. В. Х. Фриман. С. 975–977. ISBN 978-1319067748.
- ^ «В чем разница между тотипотентным, плюрипотентным и мультипотентным?».
- ^ Вестерн П (2009). «Половые клетки плода: баланс между плюрипотентностью и дифференцировкой». Int. J. Dev. Биол. 53 (2–3): 393–409. Дои:10.1387 / ijdb.082671pw. PMID 19412894.
- ^ Сугимото К., Гордон С.П., Мейеровиц Е.М. (апрель 2011 г.). «Регенерация у растений и животных: дедифференцировка, трансдифференцировка или просто дифференциация?». Тенденции Cell Biol. 21 (4): 212–218. Дои:10.1016 / j.tcb.2010.12.004. PMID 21236679.
- ^ Макфарлан Т.С.; Gifford W.D .; Driscoll S .; Lettieri K .; Rowe H.M .; Bonanomi D .; Ферт А .; Певица О .; Троно Д. и Пфафф С.Л. (2012). «Эффективность эмбриональных стволовых клеток колеблется в зависимости от активности эндогенного ретровируса». Природа. 487 (7405): 57–63. Bibcode:2012Натура 487 ... 57M. Дои:10.1038 / природа11244. ЧВК 3395470. PMID 22722858.
- ^ Моргани С.М .; Canham M.A .; Николс Дж .; Шаров А.А .; Migueles R.P .; Ко М.С. И Брикман Дж. М. (2013). «Тотипотентные эмбриональные стволовые клетки возникают в условиях наземной культуры». Сотовый представитель. 3 (6): 1945–1957. Дои:10.1016 / j.celrep.2013.04.034. ЧВК 3701323. PMID 23746443.
- ^ Ishiuchi T .; Enriquez-Gasca R .; Mizutani E .; Boskovic A .; Ziegler-Birling C .; Родригес-Терронес Д .; Вакаяма Т .; Вакерисас Дж. М. и Торрес-Падилья М. Э. (2015). «Ранние эмбрионоподобные клетки индуцируются подавлением репликационно-зависимой сборки хроматина». Нат Структ Мол Биол. 22 (9): 662–671. Дои:10.1038 / nsmb.3066. PMID 26237512. S2CID 837230.
- ^ Seydoux G, Braun RE (декабрь 2006 г.). «Путь к тотипотенции: уроки половых клеток». Клетка. 127 (5): 891–904. Дои:10.1016 / j.cell.2006.11.016. PMID 17129777. S2CID 16988032.
- ^ Asch R, Simerly C, Ord T, Ord VA, Schatten G (июль 1995 г.). «Этапы остановки оплодотворения человека: конфигурации микротрубочек и хромосом в осемененных ооцитах, которые не смогли завершить оплодотворение и развитие у людей». Гм. Репрод. 10 (7): 1897–1906. Дои:10.1093 / oxfordjournals.humrep.a136204. PMID 8583008.
- ^ Ciosk, R .; Депалма, Майкл; Присс, Джеймс Р. (10 февраля 2006 г.). «Трансляционные регуляторы поддерживают тотипотентность в зародышевой линии Caenorhabditis elegans». Наука. 311 (5762): 851–853. Bibcode:2006Научный ... 311..851C. Дои:10.1126 / science.1122491. PMID 16469927. S2CID 130017.
- ^ Кедде М., Агами Р. (апрель 2008 г.). «Взаимодействие между микроРНК и РНК-связывающими белками определяет процессы развития». Клеточный цикл. 7 (7): 899–903. Дои:10.4161 / cc.7.7.5644. PMID 18414021.
- ^ Хайкова П., Джеффрис С.Дж., Ли К., Миллер Н., Джексон С.П., Сурани М.А. (июль 2010 г.). «Полногеномное перепрограммирование в зародышевой линии мыши влечет за собой основной путь эксцизионной репарации». Наука. 329 (5987): 78–82. Bibcode:2010Sci ... 329 ... 78H. Дои:10.1126 / science.1187945. ЧВК 3863715. PMID 20595612.
- ^ Hackett JA, Sengupta R, Zylicz JJ, Murakami K, Lee C, Down TA, Surani MA (январь 2013 г.). «Динамика деметилирования ДНК зародышевой линии и стирание отпечатка с помощью 5-гидроксиметилцитозина». Наука. 339 (6118): 448–52. Bibcode:2013Наука ... 339..448H. Дои:10.1126 / science.1229277. ЧВК 3847602. PMID 23223451.
- ^ «Биология онлайн». Biology-Online.org. Получено 25 апреля 2013.
- ^ Binder, Marc D .; Хирокава, Нобутака; Уве Виндхорст, ред. (2009). Энциклопедия неврологии. Берлин: Springer. ISBN 978-3540237358.
- ^ а б Бейкер, Моня (2007-12-06). «Взрослые клетки перепрограммированы до плюрипотентности, без опухолей». Природа сообщает о стволовых клетках. Дои:10.1038 / stemcells.2007.124.
- ^ Stadtfeld, M .; Хохедлингер, К. (15 октября 2010 г.). «Индуцированная плюрипотентность: история, механизмы и приложения». Гены и развитие. 24 (20): 2239–2263. Дои:10.1101 / gad.1963910. ЧВК 2956203. PMID 20952534.
- ^ Такахаши, Кадзутоши; Яманака, Шинья (август 2006 г.). «Индукция плюрипотентных стволовых клеток из эмбриональных и взрослых культур фибробластов мышей с помощью определенных факторов». Клетка. 126 (4): 663–676. Дои:10.1016 / j.cell.2006.07.024. HDL:2433/159777. PMID 16904174. S2CID 1565219.
- ^ "Нобелевская премия по физиологии и медицине 2012 г. ". Nobelprize.org. Nobel Media AB 2013. Интернет. 28 ноября 2013 г.
- ^ Такахаши, Кадзутоши; Танабэ, Кодзи; Охнуки, Мари; Нарита, Мегуми; Ичисака, Томоко; Томода, Киичиро; Яманака, Шинья (1 ноября 2007 г.). «Индукция плюрипотентных стволовых клеток из фибробластов взрослого человека с помощью определенных факторов». Клетка. 131 (5): 861–872. Дои:10.1016 / j.cell.2007.11.019. HDL:2433/49782. PMID 18035408. S2CID 8531539.
- ^ а б Лян, Гаоян; Чжан, И (18 декабря 2012 г.). «Эмбриональные стволовые клетки и индуцированные плюрипотентные стволовые клетки: эпигенетическая перспектива». Клеточные исследования. 23 (1): 49–69. Дои:10.1038 / cr.2012.175. ЧВК 3541668. PMID 23247625.
- ^ Чой, Чарльз. «Отключение клеток: индуцированные плюрипотентные стволовые клетки не соответствуют потенциалу, обнаруженному в эмбриональной версии». Scientific American. Получено 25 апреля 2013.
- ^ Vierbuchen T, Ostermeier A, Pang ZP, Kokubu Y, Südhof TC, Wernig M (2010). «Прямое преобразование фибробластов в функциональные нейроны определенными факторами». Природа. 463 (7284): 1035–1041. Bibcode:2010Натура 463.1035В. Дои:10.1038 / природа08797. ЧВК 2829121. PMID 20107439.
- ^ Park, IH; Леру, PH; Чжао, Р. Хо, Н; Дейли, GQ (2008). «Генерация индуцированных человеком плюрипотентных стволовых клеток». Протоколы природы. 3 (7): 1180–1186. Дои:10.1038 / нпрот.2008.92. PMID 18600223. S2CID 13321484.
- ^ Николс Дж, Смит А (2009). «Наивные и готовые плюрипотентные государства». Стволовая клетка. 4 (6): 487–492. Дои:10.1016 / j.stem.2009.05.015. PMID 19497275.
- ^ Слышал E (2004). «Последние достижения в инактивации Х-хромосомы». Curr. Мнение. Cell Biol. 16 (3): 247–255. Дои:10.1016 / j.ceb.2004.03.005. PMID 15145348.
- ^ Беддингтон RS, Робертсон EJ (1999). «Развитие оси и ранняя асимметрия у млекопитающих». Клетка. 96 (2): 195–209. Дои:10.1016 / s0092-8674 (00) 80560-7. PMID 9988215. S2CID 16264083.
- ^ Лоусон К.А., Менесес Дж.Дж., Педерсен Р.А. (1991). «Клональный анализ судьбы эпибластов во время формирования зародышевого листка у эмбриона мыши». Разработка. 113 (3): 891–911. PMID 1821858.
- ^ Россант Дж (2008). «Стволовые клетки и раннее развитие линии». Клетка. 132 (4): 527–531. Дои:10.1016 / j.cell.2008.01.039. PMID 18295568. S2CID 14128314.
- ^ Бронс И.Г., Смитерс Л.Е., Троттер М.В., Рагг-Ганн П., Сан Б., Чува де Соуза Лопес С.М., Хоулетт С.К., Кларксон А., Арлунд-Рихтер Л., Педерсен Р.А., Валлиер Л. (2007). «Получение плюрипотентных стволовых клеток эпибласта из эмбрионов млекопитающих». Природа. 448 (7150): 191–195. Bibcode:2007Натура.448..191Б. Дои:10.1038 / природа05950. PMID 17597762. S2CID 4365390.
- ^ Осорно Р., Цакиридис А., Вонг Ф., Камбрей Н., Эконому С., Уилки Р., Блин Дж., Скоттинг П. Дж., Чемберс I, Уилсон В. (2012). «Разрушение плюрипотентности в процессе развития обращено эктопическим выражением Oct4». Разработка. 139 (13): 2288–2298. Дои:10.1242 / dev.078071. ЧВК 3367440. PMID 22669820.
- ^ Джорджетти А., Маркетто М.С., Ли М., Ю Д., Фаззина Р., Мю И, Адамо А., Парамонов И., Кардосо Дж. К., Монастерио М.Б., Барди С., Кассиани-Ингони Р., Лю Г. Х., Гейдж Ф. Х., Изписуа Бельмонте Дж. К. (2012) . «Нейрональные клетки, полученные из пуповинной крови путем эктопической экспрессии Sox2 и c-Myc». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 109 (31): 12556–61. Bibcode:2012PNAS..10912556G. Дои:10.1073 / pnas.1209523109. ЧВК 3412010. PMID 22814375.
- ^ Гуан К., Найерния К., Майер Л.С., Вагнер С., Дрессел Р., Ли Дж. Х., Нолте Дж., Вольф Ф., Ли М., Энгель В., Хазенфусс Г. (2006). «Плюрипотентность сперматогониальных стволовых клеток из семенников взрослых мышей». Природа. 440 (7088): 1199–203. Bibcode:2006 Натур.440.1199G. Дои:10.1038 / природа04697. PMID 16565704. S2CID 4350560.
- ^ Юн Чжао; Теодор Маццоне (декабрь 2010 г.). «Стволовые клетки пуповинной крови человека и путь к лекарству от диабета 1 типа». Аутоиммунный Rev. 10 (2): 103–107. Дои:10.1016 / j.autrev.2010.08.011. PMID 20728583.
- ^ Tallone T; Realini C; Böhmler A; и другие. (Апрель 2011 г.). «Жировая ткань взрослого человека содержит несколько типов мультипотентных клеток». J Cardiovasc Transl Res. 4 (2): 200–10. Дои:10.1007 / s12265-011-9257-3. PMID 21327755. S2CID 36604144.
- ^ Бельтрами AP; Barlucchi L; Торелла Д; и другие. (Сентябрь 2003 г.). «Взрослые кардиальные стволовые клетки мультипотентны и поддерживают регенерацию миокарда». Клетка. 114 (6): 763–76. Дои:10.1016 / S0092-8674 (03) 00687-1. PMID 14505575. S2CID 15588806.
- ^ Огуши Х., Арима Н., Такетани Т. (декабрь 2011 г.). «[Регенеративная терапия с использованием аллогенных мезенхимальных стволовых клеток]». Ниппон Риншо (на японском языке). 69 (12): 2121–7. PMID 22242308.
- ^ Уччелли, Антонио; Моретта, Пистойя (сентябрь 2008 г.). «Мезенхимальные стволовые клетки в здоровье и болезни». Nature Reviews Иммунология. 8 (9): 726–36. Дои:10.1038 / nri2395. PMID 19172693. S2CID 3347616.
- ^ Ibelgaufts, Horst. "Интернет-энциклопедия следопытов Cytokines & Cells". Получено 25 апреля 2013.
- ^ «дифференциация гепатобластов». СХОДИТЬ С УМА. Архивировано из оригинал на 2016-03-03. Получено 2012-08-31.
