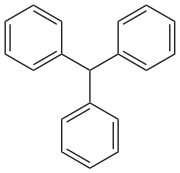
Трифенилметан - Triphenylmethane
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC 1,1 ′, 1 ′ ′ - Метантриилтрибензол | |
| Другие имена Трифенилметан 1,1 ′, 1 ′ ′ - Метилидинетрисбензол | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.007.524 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C19ЧАС16 | |
| Молярная масса | 244.337 г · моль−1 |
| Внешность | Бесцветное твердое вещество |
| Плотность | 1.014 г / см3 |
| Температура плавления | От 92 до 94 ° C (от 198 до 201 ° F, от 365 до 367 K) |
| Точка кипения | 359 ° С (678 ° F, 632 К) |
| Нерастворимый | |
| Растворимость | Растворим в диоксан[1] и гексан |
| Кислотность (пKа) | 33.3 |
| −165.6×10−6 см3/ моль | |
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материалов |
| R-фразы (устарело) | R36 R37 R38 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Трифенилметан, или же трифенилметан, это углеводород с формула (C6ЧАС5)3CH. Это бесцветное твердое вещество растворимо в неполярных органических растворителях, но не в воде. Трифенилметан - основной скелет многих синтетических красители называется триарилметановые красители, многие из них индикаторы pH, и некоторый дисплей флуоресценция. А тритил группа в органической химии - это трифенилметильная группа Ph3C, например трифенилметилхлорид (тритилхлорид) и трифенилметильный радикал (тритильный радикал).
Подготовка
Трифенилметан был впервые синтезирован в 1872 году немецким химиком. Август Кекуле и его бельгийский студент Антуан Поль Николя Франшимон (1844–1919) путем нагрева дифенилртуть (Hg (C6ЧАС5)2, Квексилбердифенил) с бензал хлорид (C6ЧАС5CHCl2, Бензиленхлорид).[2]
Трифенилметан может быть синтезирован Реакция Фриделя – Крафтса из бензол и хлороформ с хлорид алюминия катализатор:
- 3 С6ЧАС6 + CHCl3 → Ph3CH + 3 HCl
В качестве альтернативы бензол может реагировать с четыреххлористый углерод используя тот же катализатор для получения трифенилметилхлорид –хлорид алюминия аддукт, который гидролизуется разбавленной кислотой:[3]
- 3 С6ЧАС6 + CCl4 + AlCl3 → Ph3CCl · AlCl3
- Ph3CCl · AlCl3 + HCl → Ph3CH
Синтез из бензилиденхлорид, приготовленный из бензальдегид и пентахлорид фосфора, также используется.
Кислотность
В пKа составляет 33,3.[4] Трифенилметан значительно более кислый, чем большинство других углеводородов, поскольку его заряд делокализованный над тремя фенильными кольцами. Однако стерические эффекты не позволяют всем трем фенильным кольцам одновременно достичь компланарности. как следствие дифенилметан еще более кислый, потому что в его анионе заряд распределяется по двум фенильным кольцам одновременно. В тритил-анион красный. Этот цвет можно использовать как индикатор в кислотно-основное титрование.
Натриевую соль можно также получить из хлорид:[5]
- (C6ЧАС5)3CCl + 2 Na → (С6ЧАС5)3CNa + NaCl
Использование тритилсатрия как сильного, ненуклеофильное основание затмила популяризация бутиллитий и связанные с ними сильные основания.
Триарилметановые красители
Примеры триарилметановых красителей: бромкрезоловый зеленый:
И азот -несущий малахитовый зеленый:
Смотрите также
- Тетрафенилметан
- Трифенилметанол
- Трифенилметилхлорид
- Трифенилметил гексафторфосфат
- Трифенилметильный радикал
Рекомендации
- ^ «Трифенилметан | 519-73-3».
- ^ Август Кекуле и А. Франшимон (1872) «Убер дас трифенилметан» (По трифенилметану), Berichte der deutschen chemischen Gesellschaft, 5 : 906–908.
- ^ Дж. Ф. Норрис (1925). «Трифенилметан». Органический синтез. 4: 81. Дои:10.15227 / orgsyn.004.0081.
- ^ Рональд Бреслоу и Уильям Чу (1969). «Электрохимические определения pKас. Трифенилметаны и циклогептатриен ». Журнал Американского химического общества. 92 (7): 2165. Дои:10.1021 / ja00710a077.
- ^ У. Б. Ренфроу-младший и К. Р. Хаузер (1943). «Трифенилметилнатрий». Органический синтез.; Коллективный объем, 2, п. 607


