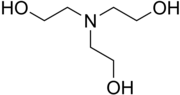
Триэтаноламин - Triethanolamine
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC 2,2 ', 2' '- нитрилотри (этан-1-ол)[1] | |
Другие имена
| |
| Идентификаторы | |
3D модель (JSmol ) | |
| 3DMet | |
| 1699263 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.002.773 |
| Номер ЕС |
|
| КЕГГ | |
| MeSH | Биафин |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C6ЧАС15NО3 | |
| Молярная масса | 149.190 г · моль−1 |
| Внешность | Бесцветная жидкость |
| Запах | Аммиачный |
| Плотность | 1,124 г мл−1 |
| Температура плавления | 21,60 ° С; 70,88 ° F; 294,75 К |
| Точка кипения | 335,40 ° С; 635,72 ° F; 608,55 К |
| смешивающийся | |
| бревно п | −0.988 |
| Давление газа | 1 Па (при 20 ° C) |
| Кислотность (пKа) | 7.74[2] |
| УФ-видимый (λМаксимум) | 280 нм |
| 1.485 | |
| Термохимия | |
Теплоемкость (C) | 389 Дж К−1 моль−1 |
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −665,7 - −662,7 кДж моль−1 |
Станд. Энтальпия горение (ΔcЧАС⦵298) | −3,8421 - −3,8391 МДж моль−1 |
| Фармакология | |
| D03AX12 (ВОЗ) | |
| Опасности | |
| Паспорт безопасности | hazar.com |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H319 | |
| P305 + 351 + 338 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 179 ° С (354 ° F, 452 К) |
| 325 ° С (617 ° F, 598 К) | |
| Пределы взрываемости | 1.3–8.5% |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) |
|
| Родственные соединения | |
Родственные алканолы | |
Родственные соединения | Диэтилгидроксиламин |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триэтаноламин, или TEA - это вязкий органическое соединение это и высшее амин и триол. Триол - это молекула с тремя алкоголь группы. Приблизительно 150 000 тонны были произведены в 1999 году.[3] Это бесцветное соединение, хотя образцы могут казаться желтыми из-за примесей.
Производство
Триэтаноламин получают по реакции окись этилена с водным аммиак, также производятся этаноламин и диэтаноламин. Соотношение продуктов можно контролировать, изменяя стехиометрия реагентов.[4]
Приложения
Триэтаноламин используется в основном при производстве поверхностно-активные вещества, например, для эмульгатор. Это обычный ингредиент в рецептурах, используемых как в промышленных, так и в потребительских товарах. Триэтаноламин нейтрализует жирные кислоты, регулирует и буферы то pH, и солюбилизирует масла и другие ингредиенты, которые не полностью растворимый в воде. Соли триэтаноламмония в некоторых случаях более растворимы, чем соли щелочных металлов которые можно было бы использовать иначе, и в результате образуется меньше щелочных продуктов, чем при использовании гидроксидов щелочных металлов для образования соли. Некоторые распространенные продукты, в которых содержится триэтаноламин: солнцезащитные лосьоны, жидкость стиральные порошки, жидкости для мытья посуды, общие чистящие средства, дезинфицирующие средства для рук, полирует, металлообработка жидкости, краски, крем для бритья и печатные краски.[5]
Производство цемента
Триэтаноламин также используется в качестве органической добавки (0,1 мас.%) При измельчении цементный клинкер. Это облегчает процесс измельчения, предотвращая агломерацию и покрытие порошка на поверхности шаров и стенок мельницы.[6]
Косметика и медицина
Разные ушные заболевания и инфекции лечат ушными каплями, содержащими олеат-конденсат полипептида триэтаноламина, такими как Cerumenex в США. В фармацевтике триэтаноламин является активным ингредиентом некоторых ушных капель, используемых для лечения пораженных участков. ушная сера. Он также служит pH балансир во многих косметических продуктах, начиная от очищающих кремов и молочка, лосьоны для кожи, гели для глаз, увлажняющие средства, шампуни, пена для бритья, и так далее. TEOA - довольно сильное основание: 1% раствор имеет pH приблизительно 10, тогда как pH кожи меньше pH 7, приблизительно 5,5-6,0. Очищающие молочно-кремовые эмульсии на основе TEOA особенно хорошо удаляют макияж.
Производные
В лаборатории и в любительской фотографии
Другое распространенное использование TEOA - это комплексообразователь за алюминий ионы в водных растворах. Эта реакция часто используется для маскировки таких ионов перед комплексометрическое титрование с другим хелатирующий агент, такой как EDTA. TEOA также использовался в фотографический (галогенид серебра ) обработка. Фотографы-любители рекламировали его как полезную щелочь.
В голографии
TEOA используется для повышения чувствительности к галогенидам серебра. голограммы, а также как агент набухания для изменения цвета голограмм. Можно добиться повышения чувствительности без изменения цвета, промыв ЧАЙ перед нанесением ракеля и сушкой.[7]
В химическом покрытии
TEOA сейчас широко и очень эффективно используется в качестве комплексообразователя в химическое нанесение покрытия.
В ультразвуковом контроле
2-3% в воде TEOA используется в качестве ингибитора коррозии (антикоррозийного) при ультразвуковых испытаниях погружением.
При пайке алюминия
Триэтаноламин, диэтаноламин и аминоэтилэтаноламин являются основными компонентами обычных жидких органических флюсов для пайки алюминиевых сплавов с использованием оловянно-цинковых и других мягких припоев на основе олова или свинца.[8][9][10]
Безопасность и регулирование
Аллергические реакции
Исследование 1996 года показало, что триэтаноламин (TEOA) иногда вызывает контакт аллергия.[11] Исследование 2001 г. показало, что TEOA в солнцезащитный крем вызвал аллергический контакт дерматит.[12] Исследование 2007 года показало, что TEOA в ушные капли вызвал контактную аллергию.[13] Системную токсичность и токсичность для дыхательных путей (RT) анализировали в течение 28 дней в исследовании 2008 г. при вдыхании через нос на крысах Wistar; TEOA, по-видимому, менее эффективен в отношении системной токсичности и раздражения при ЛТ, чем диэтаноламин (ДЭА). Воздействие TEOA приводило к очаговому воспалению, начиная с 20 мг / м3 у одиночных самцов животных.3 концентрации.[14]
Исследование 2009 года показало, что патч-тест реакции выявляют незначительный раздражающий потенциал вместо истинной аллергической реакции в нескольких случаях, а также указывают на риск поражения кожи сенсибилизация до TEOA кажется очень низким.[15]
Опухоли
Отчеты показали, что TEOA вызывает повышенную заболеваемость рост опухоли в печени самок мышей B6C3F1, но не самцов мышей или крыс Fischer 344.[16] Исследование 2004 г. пришло к выводу, что «TEOA может вызывать опухоли печени у мышей за счет истощения холина, и что этот эффект, вероятно, вызван ингибированием поглощения холина клетками».[16]
Экологическая токсичность
Исследование 2009 года показало, что TEOA обладает потенциально острой, субхронической и хронической токсичностью в отношении водных видов.[17]
Регулирование
TEOA внесен в список Приложение 3, часть B из Конвенция о химическом оружии поскольку его можно использовать при изготовлении Азотный горчица HN3.
Смотрите также
Рекомендации
- ^ «Переднее дело». Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. С. P001 – P004. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Симонд, М. Р. (2012). «Константы диссоциации протонированных аминов в воде при температурах от 293,15 К до 343,15 К». Журнал химии растворов. 41: 130. Дои:10.1007 / s10953-011-9790-3.
- ^ Фрауенкрон, Матиас; Мельдер, Иоганн-Петер; Руидер, Гюнтер; Россбахер, Роланд; Хёке, Хартмут. «Этаноламины и пропаноламины». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a10_001.
- ^ Вайссермель, Клаус; Арпе, Ханс-Юрген; Lindley, Charlet R .; Хокинс, Стивен (2003). «Глава 7. Продукты окисления этилена». Промышленная органическая химия. Вайли-ВЧ. С. 159–161. ISBN 978-3-527-30578-0.
- ^ Эшфорд, Роберт Д. (2011). Словарь промышленных химикатов Эшфорда (3-е изд.). Солташ, Корнуолл: публикации о длине волны. п. 9252. ISBN 978-0-9522674-3-0.
- ^ Sohoni, S .; Sridhar, R .; Мандал, Г. (1991). «Влияние шлифовальных добавок на тонкое измельчение известняка, кварца и портландцементного клинкера». Порошковая технология. 67 (3): 277–286. Дои:10.1016 / 0032-5910 (91) 80109-В.
- ^ "Holoforum.org". Holoforum.org. Получено 2016-07-16.
- ^ «Капп Жидкий флюс SDS» (PDF). kappalloy.com. Получено 9 апреля 2019.
- ^ "Harris Stay-Clean Aluminium Flux SDS" (PDF). lincolnelectric.com. Получено 9 апреля 2019.
- ^ "Superior # 1260 Flux SDS" (PDF). superiorflux.com. Получено 9 апреля 2019.
- ^ Гамильтон, Т. К .; Цуг, К. А. (1996). «Аллергия на триэтаноламин, непреднамеренно обнаруженная флуоресцентным маркером». Являюсь. J. Связаться с Dermat. 7 (3): 164–5. Дои:10.1016 / S1046-199X (96) 90006-8. PMID 8957332.
- ^ Chu, C.Y .; Солнце, К. С. (2001). «Аллергический контактный дерматит от триэтаноламина в солнцезащитном креме». Контактный дерматит. 44 (1): 41–2. Дои:10.1034 / j.1600-0536.2001.440107-8.x. PMID 11156016.
- ^ Schmutz, J. L .; Barbaud, A .; Трехо, П. (2007). «Контактная аллергия на триэтаноламин в ушных каплях и шампунях». Анна. Дерматол. Венереол. 134 (1): 105. Дои:10.1016 / S0151-9638 (07) 89009-0. PMID 17384563.
- ^ Геймер, А.О .; Россбахер, Р .; Kaufmann, W .; ван Равенцвай, Б. (2008). «Ингаляционная токсичность ди- и триэтаноламинов при многократном воздействии». Food Chem. Токсикол. 46 (6): 2173–2183. Дои:10.1016 / j.fct.2008.02.020. PMID 18420328.
- ^ Lessmann, H .; Uter, W .; Schnuch, A .; Гейер, Дж. (2009). «Кожные сенсибилизирующие свойства этаноламинов моно-, ди- и триэтаноламинов. Анализ данных многоцентровой сети эпиднадзора (IVDK *) и обзор литературы». Контактный дерматит. 60 (5): 243–255. Дои:10.1111 / j.1600-0536.2009.01506.x. PMID 19397616.
- ^ а б Stott, W. T .; Radtke, B.J .; Линскомб, В. А .; Mar, M. H .; Цейсель, С. Х. (2004). «Оценка способности триэтаноламина изменять уровни холина в печени у самок мышей B6C3F1». Toxicol. Наука. 79 (2): 242–7. Дои:10.1093 / toxsci / kfh115. ЧВК 1592523. PMID 15056812.
- ^ Libralato, G .; Volpi Ghirardini, A .; Авеццо, Ф. (2009). «Экотоксичность моноэтаноламина, диэтаноламина и триэтаноламина в морской воде». J. Hazard. Матер. 176 (1–3): 535–9. Дои:10.1016 / j.jhazmat.2009.11.062. PMID 20022426.


