Тетраиодид титана - Titanium tetraiodide
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Иодид титана (IV) | |
| Другие имена Тетраиодид титана | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.868 |
| Номер ЕС |
|
PubChem CID | |
| |
| |
| Характеристики | |
| TiI4 | |
| Молярная масса | 555,485 г / моль |
| Внешность | красно-коричневые кристаллы |
| Плотность | 4,3 г / см3 |
| Температура плавления | 150 ° С (302 ° F, 423 К) |
| Точка кипения | 377 ° С (711 ° F, 650 К) |
| гидролиз | |
| Растворимость в других растворителях | растворим в CH2Cl2 CHCl3 CS2 |
| Структура | |
| кубический (а = 12,21 Å) | |
| четырехгранный | |
| 0 D | |
| Опасности | |
| Главный опасности | бурный гидролиз разъедающий |
| R-фразы (устарело) | 34-37 |
| S-фразы (устарело) | 26-36/37/39-45 |
| Родственные соединения | |
Другой анионы | Бромид титана (IV) Хлорид титана (IV) Фторид титана (IV) |
Родственные соединения | Иодид титана (III) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Тетраиодид титана является неорганическое соединение с формула TiI4. Это черное летучее твердое вещество, о котором впервые сообщил Рудольф Вебер в 1863 году.[1] Это промежуточное звено в Процесс Ван Аркеля для очистки титана.
Физические свойства
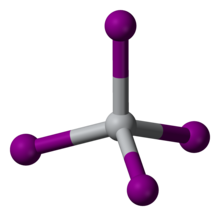
TiI4 представляет собой редкий молекулярный иодид бинарного металла, состоящий из изолированных молекул тетраэдрических центров Ti (IV). Расстояние Ti-I составляет 261 вечера.[2] Отражая его молекулярный характер, TiI4 можно перегонять без разложения при одной атмосфере; это свойство является основой его использования в Процесс Ван Аркеля. Разница в температуре плавления TiCl4 (т.пл. -24 ° C) и TiI4 (т.пл.150 ° C) сопоставима с разницей между температурами плавления CCl4 (т.пл. -23 ° C) и CI4 (т.пл.168 ° C), что отражает более сильную межмолекулярную ван-дер-ваальсовую связь в иодидах.
Два полиморфы TiI4 существуют, один из которых хорошо растворяется в органических растворителях. В менее растворимой кубической форме расстояния Ti-I равны 261 вечера.[2]
Производство
Хорошо известны три метода: 1) Из элементов, обычно с использованием трубчатой печи при 425 ° C:[3]
- Ti + 2 I2 → TiI4
Эту реакцию можно обратить, чтобы получить пленки металлического Ti высокой чистоты.[4]
2) Обменная реакция от тетрахлорид титана и привет.
- TiCl4 + 4 HI → TiI4 + 4 HCl
3) Оксидно-йодидный обмен от йодид алюминия.
- 3 TiO2 + 4 Али3 → 3 TiI4 + 2 Al2О3
Реакции
Как TiCl4 и TiBr4, TiI4 образует аддукты с основаниями Льюиса, а также может быть восстановлен. Когда восстановление проводят в присутствии металлического Ti, получают полимерные производные Ti (III) и Ti (II), такие как CsTi.2я7 и цепочка CsTiI3, соответственно.[5]
TiI4 проявляет обширную реакционную способность по отношению к алкенам и алкинам, что приводит к образованию йодорганических производных. Это также влияет муфты pinacol и другие реакции образования связи C-C.[6]
Рекомендации
- ^ Вебер, Р. (1863). "Ueber die isomeren Modificationen der Titansäure und über einige Titanverbindungen". Annalen der Physik. 120 (10): 287–294. Bibcode:1863AnP ... 196..287Вт. Дои:10.1002 / andp.18631961003.
- ^ а б Торнквист, Э. Г. М .; Либби, У. Ф. (1979). «Кристаллическая структура, растворимость и электронный спектр тетраиодида титана». Неорганическая химия. 18 (7): 1792–1796. Дои:10.1021 / ic50197a013.
- ^ Lowry, R. N .; Фэй Р.С. (1967). Иодид титана (IV). Неорганические синтезы. 10. п. 1. Дои:10.1002 / 9780470132418.ch1. ISBN 9780470132418.
- ^ Blumenthal, W. B .; Смит, Х. (1950). «Тетраиодид титана, получение и очистка». Промышленная и инженерная химия. 42 (2): 249. Дои:10.1021 / ie50482a016.
- ^ Jongen, L .; Gloger, T .; Beekhuizen, J .; Мейер, Г. (2005). "Двухвалентный титан: галогениды ATiX3 (A = K, Rb, Cs; X = Cl, Br, I) ". Zeitschrift für anorganische und allgemeine Chemie. 631 (2–3): 582. Дои:10.1002 / zaac.200400464.
- ^ Shimizu, M .; Хачия, И. (2014). «Хемоселективное восстановление и йодирование с использованием тетраиодида титана». Буквы Тетраэдра. 55 (17): 2781–2788. Дои:10.1016 / j.tetlet.2014.03.052.
