Ротаксан - Rotaxane
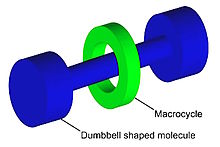

А ротаксан это механически взаимосвязанная молекулярная архитектура состоящий из "молекулы в форме гантели", продетой через "макроцикл "(см. графическое изображение). Название происходит от латинского слова" колесо "(вращение) и ось (ось). Два компонента ротаксана захватываются кинетически, поскольку концы гантели (часто называемые стопорами) больше, чем внутренние диаметр кольца и предотвратить диссоциация (распаковка) компонентов, поскольку это потребует значительного искажения ковалентных связей.
Большая часть исследований ротаксанов и других механически взаимосвязанных молекулярных архитектур, таких как катенаны, был сосредоточен на их эффективном синтезе или их использовании в качестве искусственных молекулярные машины. Однако примеры субструктуры ротаксана были обнаружены в природных пептидах, в том числе: цистиновый узел пептиды, циклотиды или лассо-пептиды, такие как микроцин J25.
Синтез
Самый ранний синтез ротаксана в 1967 году основывался на статистическая вероятность что если две половинки молекулы в форме гантели прореагируют в присутствии макроцикл что небольшой процент будет подключаться через кольцо.[2] Чтобы получить разумное количество ротаксана, макроцикл был прикреплен к твердофазная поддержка и обрабатывали обеими половинами гантели 70 раз, а затем отделяли от опоры с выходом 6%. Однако синтез ротаксанов значительно продвинулся вперед, и эффективные выходы могут быть достигнуты путем предварительной организации компонентов с использованием водородная связь, металлическое согласование, гидрофобные силы, ковалентные связи, или же кулоновские взаимодействия. Три наиболее распространенных стратегии синтеза ротаксана - это «укупоривание», «отсечение» и «скольжение».[3] хотя другие существуют.[4][5] Недавно Ли и соавторы описали новый путь к механически взаимосвязанным архитектурам с участием центра переходного металла, который может катализировать реакцию через полость макроцикла.[6]

Укупорка

Синтез методом укупорки сильно зависит от термодинамически обусловленного эффекта шаблона; то есть «нить» удерживается внутри «макроцикла» нековалентными взаимодействиями, например вращение с циклодекстриновыми макроциклами связано с использованием гидрофобного эффекта. Этот динамический комплекс или псевдоротаксан затем превращается в ротаксан, реагируя на концах связанного гостя с большими группами, предотвращая диссоциацию.[8]
Вырезка
Метод отсечения аналогичен реакции кэппинга, за исключением того, что в этом случае молекула в форме гантели является полной и связана с частичным макроциклом. Затем частичный макроцикл подвергается реакция замыкания кольца вокруг молекулы в форме гантели, образуя ротаксан.[9]
Скольжение
Метод скольжения основан на термодинамическом[10] стабильность ротаксана. Если концевые группы гантели имеют соответствующий размер, она сможет обратимо проходить через макроцикл при более высоких температурах. При охлаждении динамического комплекса он становится кинетически захваченным в виде ротаксана при более низкой температуре.
Методика «активного шаблона»
Ли и соавторы недавно начали исследовать стратегию, в которой ионы-матрицы могут также играть активную роль в стимулировании решающей последней реакции образования ковалентной связи, которая захватывает заблокированную структуру (т. Е. Металл выполняет двойную функцию, действуя как шаблон для связывание предшественников и катализирование образования ковалентной связи между реагентами).
Возможные приложения

Молекулярные машины
Молекулярные машины на основе ротаксана изначально представляли интерес из-за их потенциального использования в молекулярная электроника как логика молекулярное переключение элементы и как молекулярные челноки.[12][13] Эти молекулярные машины обычно основаны на движении макроцикл на гантели. В макроцикл может вращаться вокруг оси гантели, как колесо и ось, или может скользить вдоль своей оси от одного места к другому. Контроль положения макроцикл позволяет ротаксану функционировать в качестве молекулярного переключателя, при этом каждое возможное положение макроцикла соответствует разному состоянию. Эти ротаксановые машины можно манипулировать как химическими [14] и фотохимические вводы.[15] Также было показано, что системы на основе ротаксана действуют как молекулярные мышцы.[16][17] В 2009 году было сообщение об «эффекте домино» от одной конечности до другой в молекулярной машине с гликоротаксаном. В этом случае 4C1 или же 1C4 стулообразное строение маннопиранозид стопором можно управлять в зависимости от локализации макроцикла.[18] В 2012 г. в журнале Chem было опубликовано сообщение об уникальных псевдомакроциклах, состоящих из молекулярных машин с двойным лассо (также называемых ротамакроциклами). Sci. Эти структуры можно сжимать или ослаблять в зависимости от pH. В этих новых молекулярных машинах также наблюдалось контролируемое движение скакалки.[19]
Ультрастабильные красители
Возможное применение в качестве красителей длительного действия основано на повышенной стабильности внутренней части молекулы в форме гантели.[20][21] Исследования с циклодекстрин -защищенный ротаксан азокрасители установил эту характеристику. Более реактивный скваринные красители также было показано, что они обладают повышенной стабильностью, предотвращая нуклеофильная атака внутренней площади часть.[22] Повышенная стабильность ротаксановых красителей объясняется изолирующим действием макроцикл, который способен блокировать взаимодействие с другими молекулами.
Нанозапись
В приложении для нано-записи[23] определенный ротаксан откладывается в виде Фильм Ленгмюра – Блоджетт на ITO -мелованное стекло. Когда положительный Напряжение наносится кончиком сканирующий туннельный микроскоп зонд, ротаксановые кольца в области кончика гантели переключаются на другую часть гантели, и в результате получается новый конформация заставляет молекулы торчать 0,3 нанометр с поверхности. Такой разницы в высоте достаточно для точка памяти. Пока не известно, как стереть такую нанозапись.
Номенклатура
Принятая номенклатура заключается в обозначении количества компонентов ротаксана в скобках в качестве префикса.[24] Поэтому ротаксан, состоящий из одной аксиальной молекулы в форме гантели с одним макроциклом вокруг вала, называется [2] ротаксаном, а два цианозвезда молекулы вокруг центральной фосфатной группы диалкилфосфата представляют собой [3] ротаксан.
Смотрите также
- Catenane
- Молекулярная архитектура с механической блокировкой
- Молекулярные кольца Борромео
- Молекулярные узлы
- Полиротаксан
Рекомендации
- ^ Браво, Хосе А .; Raymo, Françisco M .; Стоддарт, Дж. Фрейзер; Уайт, Эндрю Дж. П .; Уильямс, Дэвид Дж. (1998). «Высокоурожайные матричные синтезы [2] ротаксанов». Евро. J. Org. Chem. 1998 (11): 2565–2571. Дои:10.1002 / (SICI) 1099-0690 (199811) 1998: 11 <2565 :: AID-EJOC2565> 3.0.CO; 2-8.
- ^ Харрисон, Ян Томас; Харрисон, Шуен. (1967). «Синтез стабильного комплекса макроцикла и нитевой цепи». Варенье. Chem. Soc. 89 (22): 5723–5724. Дои:10.1021 / ja00998a052.
- ^ Арико, Ф. (2005). Шаблонный синтез взаимосвязанных молекул. Темы современной химии. 249. С. 203–259. Дои:10.1007 / b104330. HDL:10278/33611. ISBN 978-3-540-23087-8.
- ^ Юн, я; Нарита, М; Симидзу, Т; Асакава, М. (2004). «Протокол нарезания нити с последующей усадкой для синтеза [2] ротаксана, включающего фрагмент Pd (II) -салофен». Варенье. Chem. Soc. 126 (51): 16740–16741. Дои:10.1021 / ja0464490. PMID 15612709.
- ^ Камета, Н; Hiratani, K; Нагава, Y (2004). «Новый синтез хиральных ротаксанов посредством образования ковалентной связи». Chem. Commun. (51): 466–467. Дои:10.1039 / b314744d. PMID 14765261.
- ^ Окань, V; Берна, Дж; Crowley, J.D .; Goldup, S.M .; Hänni, K. D .; Leigh, D.A .; Lusby, P.J .; Рональдсон, В. Э .; Славин, А. М .; Витеризи, А; Уокер, Д. Б. (2007). «Каталитический« активный металл »темплатный синтез [2] ротаксанов, [3] ротаксанов и молекулярных челноков, а также некоторые наблюдения о механизме катализируемого Cu (I) азид-алкин-1,3-циклоприсоединения». Варенье. Chem. Soc. 129 (39): 11950–11963. Дои:10.1021 / ja073513f. PMID 17845039.
- ^ Лист, Джонатан; Фальгенгауэр, Элизабет; Коппергер, Энцо; Пардачер, Гюнтер; Зиммель, Фридрих К. (2016). «Движение больших механически связанных наноструктур ДНК на большие расстояния». Nature Communications. 7: 12414. Bibcode:2016НатКо ... 712414L. Дои:10.1038 / ncomms12414. ЧВК 4980458. PMID 27492061.
- ^ «Ротаксан путем укупорки». youtube.com.
- ^ Ромеро, Антонио. "Ротаксан путем укупорки 3d". Ротаксан путем укупорки 3d. 3D видео.
- ^ Карсон Дж. Брунс; Дж. Фрейзер Стоддарт (7 ноября 2016 г.). Природа механической связи: от молекул к машинам. Джон Вили и сыновья. С. 271–. ISBN 978-1-119-04400-0.
- ^ Stanier, Carol A .; о'Коннелл, Майкл Дж .; Андерсон, Гарри Л .; Клегг, Уильям (2001). "Синтез флуоресцентных ротаксанов стильбена и толана сочетанием Сузуки". Chem. Commun. (5): 493–494. Дои:10.1039 / b010015n.
- ^ Schalley, C.A .; Beizai, K; Vögtle, F (2001). «На пути к молекулярным двигателям на основе ротаксана: исследования молекулярной мобильности и топологической хиральности». Соотв. Chem. Res. 34 (6): 465–476. Дои:10.1021 / ar000179i. PMID 11412083.
- ^ Соваж, Дж. П. (1999). «Ротаксаны и катенаны с переходными металлами в движении: к молекулярным машинам и двигателям». ХимИнформ. 30 (4): нет. Дои:10.1002 / подбородок.199904221.
- ^ Coutrot, F .; Буссерон, Э. (2008). «Новая молекулярная машина для гликоротаксана на основе анилиния и триазолиевой станции». Chem. Евро. Дж. 14 (16): 4784–4787. Дои:10.1002 / chem.200800480. PMID 18409178.
- ^ Серрели, V; Lee, C.F .; Kay, E. R .; Ли, Д. А. (2007). "Осуществление демонов: трещотка молекулярной информации". Природа. 445 (7127): 523–527. Bibcode:2007Натура.445..523S. Дои:10.1038 / природа05452. PMID 17268466.
- ^ Coutrot, F; Ромуальд, С; Буссерон, Э (2008). "Новая молекулярная машина диманнозила [c2] гирляндной цепи с переключением pH". Орг. Lett. 10 (17): 3741–3744. Дои:10.1021 / ol801390h. PMID 18666774.
- ^ Радха Кишан, М; Пархэм, А; Schelhase, F; Йонева, А; Сильва, G; Чен, X; Окамото, Y; Фогтле, Ф (2006). «Соединение колес ротаксанов - циклохиральные боннаны». Энгью. Chem. Int. Эд. 45 (43): 7296–7299. Дои:10.1002 / anie.200602002. PMID 17029314.
- ^ Coutrot, F .; Буссерон, Э. (2009). «Управление конформацией кресла маннопиранозы в большой амплитуде [2] ротаксановой молекулярной машины». Chem. Евро. Дж. 15 (21): 5186–5190. Дои:10.1002 / chem.200900076. PMID 19229918.
- ^ Ромуальд, Камилла; Арда, Ана; Клавель, Кэролайн; Хименес-Барберо, Хесус; Котро, Фредерик (2012). «Затягивание или ослабление pH-чувствительной молекулярной машины с двойным лассо, легко синтезируемой из гирляндной цепи, активируемой концами [c2]». Chem. Sci. 3 (6): 1851–1857. Дои:10.1039 / C2SC20072D. HDL:10261/60415.
- ^ Buston, Jonathan E.H .; Янг, Джеймс Р .; Андерсон, Гарри Л. (2000). «Цианиновые красители, инкапсулированные в ротаксане: повышенная эффективность флуоресценции и фотостабильность». Chem. Commun. (11): 905–906. Дои:10.1039 / b001812k.
- ^ Craig, M. R .; Hutchings, M. G .; Claridge, T. D .; Андерсон, Х. Л. (1998). «Ротаксан-инкапсуляция повышает стабильность азокрасителя в растворе и при связывании с целлюлозой». Энгью. Chem. Int. Эд. 40 (6): 1071–1074. Дои:10.1002 / 1521-3773 (20010316) 40: 6 <1071 :: AID-ANIE10710> 3.0.CO; 2-5. PMID 11268077.
- ^ Arunkumar, E; Forbes, C.C .; Noll, B.C .; Смит, Б. Д. (2005). "Ротаксаны, полученные из сквараина: стерически защищенные флуоресцентные красители в ближнем ИК-диапазоне" (PDF). Варенье. Chem. Soc. 127 (10): 3288–3289. Дои:10.1021 / ja042404n. PMID 15755140.
- ^ Фэн, М; Guo, X; Lin, X; Он, Х; Джи, Вт; Ду, С; Zhang, D; Чжу, Д; Гао, Х (2005). «Стабильная, воспроизводимая нанозапись на тонких пленках ротаксана». Варенье. Chem. Soc. 127 (44): 15338–15339. Дои:10.1021 / ja054836j. PMID 16262375.
- ^ Ерин, Андрей; Уилкс, Эдвард С .; Мосс, Джерард П .; Харада, Акира (2008). «Номенклатура ротаксанов и псевдоротаксанов (Рекомендации ИЮПАК 2008 г.)». Чистая и прикладная химия. 80 (9): 2041–2068. Дои:10.1351 / pac200880092041.

