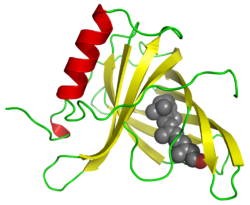
Белок, связывающий ретинол 4 - Retinol binding protein 4
Белок, связывающий ретинол 4, также известный как RBP4, это транспортер белок[5] за ретинол (витамин А, алкоголь). RBP4 имеет молекулярную массу приблизительно 21 кДа и кодируется RBP4 ген в людях.[6][7] Он в основном, но не исключительно, синтезируется в печени и циркулирует в кровотоке, связываясь с ретинолом в комплексе с транстиретин. RBP4 был лекарственной мишенью для офтальмологических исследований из-за его роли в зрении.[8] RBP4 также может быть вовлечен в метаболические заболевания, как показали недавние исследования.
Функция
Этот белок относится к липокалин семья и является специфическим носителем для ретинол (витамин А) в крови. Он доставляет ретинол из запасов печени в периферические ткани. В плазме комплекс RBP-ретинол взаимодействует с транстиретин, что предотвращает его потерю путем фильтрации через почки клубочки. Дефицит витамина А блокирует секрецию связывающего белка посттрансляционно и приводит к нарушению доставки и снабжения эпидермальных клеток.[7]
Структура

RBP4 представляет собой одиночную полипептидную цепь с гидрофобным карманом, в котором связывается ретинол. Комплекс RBP4-ретинол затем связывает транстиретин в кровотоке, чтобы предотвратить почечную фильтрацию RBP4.[9]
В сыворотке TTR и RBP4 связываются от 1 до 1 стехиометрия (две молекулы TTR соединяются с двумя молекулами RBP4 с образованием комплекса с общей молекулярной массой примерно 80000 Дальтон ).[10]
Клиническое значение
Ретинол-связывающий белок 4 является лекарственной мишенью для лечения глазных болезней, поскольку RBP4 является единственным носителем ретинола, который является важным питательным веществом для зрительного цикла. Исследования на животных с использованием антагонистов RBP4 показали, что снижение RBP4 может приводить к уменьшению накопления липофусцин что приводит к потере зрения при глазных заболеваниях, таких как Болезнь Штаргардта и дегенерация желтого пятна.[8][11]Исследование на животных с использованием ABCA4 нокаутирующая мышь доказали, что снижение уровня RBP4 в сыворотке может ингибировать липофусцин без подавления зрительного цикла. [ref] Одно клиническое исследование возрастной дегенерации желтого пятна (AMD) было проведено с использованием Фенретинид. Исследование показало тенденции к снижению скорости роста поражений при AMD и скорости преобразования AMD на ранней стадии (сухой AMD) в позднюю стадию AMD (влажный AMD) без серьезных побочных эффектов.
RBP4 недавно был описан как адипокин что способствует резистентность к инсулину и сахарный диабет в модели мыши AG4KO.[12] Помимо печени, RBP4 также секретируется адипоциты из жировая ткань в меньшей части и действует как сигнал для окружающих клеток, когда происходит снижение концентрации глюкозы в плазме.[13] Предполагается, что повышенный уровень RBP4 привлекает макрофаги к жировой ткани, вызывает местное воспаление и приводит к инсулинорезистентности.[14][15]
Мутации в гене RBP4 недавно были связаны с формой аутосомно-доминантного микрофтальмии, анофтальмии и колобомы (MAC).[16] Уникальной особенностью этого заболевания является эффект материнского наследования, когда плод наследует мутированную копию гена RBP4 от своей матери, но не от отца. Физиологическая основа заключается в беременности, при которой продукт мутировавшего гена, ретинол-связывающий белок (RBP), оказывает негативное влияние на перенос витамина А из мест хранения материнской печени в плаценту, а затем снова на сторону кровообращения плода при доставке витамина А из плаценты. развивающимся тканям плода, особенно развивающемуся глазу. Этот эффект «двойного удара» не существует, когда мутантный ген RBP4 унаследован от отца. Вышеупомянутый механизм отличается от ранее известных типов эффектов материнского наследования, таких как геномный импринтинг, митохондриальное наследование или перенос мРНК материнского ооцита. Авторы вышеупомянутого исследования ссылаются на потенциал добавок витамина А у беременных женщин, которые, как известно, несут мутацию RBP4 с ретиниловым эфиром, который использует RBP-независимый путь для доставки ретиноидов из кишечника матери непосредственно в плаценту и в конечном итоге поглощается плод. Ключевым моментом будет добавление добавок в течение первых нескольких месяцев жизни, когда глаза начинают развиваться, поскольку добавление добавок на более поздних сроках беременности будет слишком поздно, чтобы избежать любого потенциального заболевания MAC.
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000138207 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000024990 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Раск Л., Анунди Х, Фохлман Дж, Петерсон П.А. (1987). «Полная аминокислотная последовательность ретинол-связывающего белка сыворотки человека». Упсальский журнал медицинских наук. 92 (2): 115–46. Дои:10.3109/03009738709178685. PMID 2444024.
- ^ Рокки М., Ковоне А., Ромео Дж., Фараонио Р., Колантуони В. (март 1989 г.). «Региональное сопоставление RBP4 с 10q23 ---- q24 и RBP1 с 3q21 ---- q22 у человека». Соматическая клетка и молекулярная генетика. 15 (2): 185–90. Дои:10.1007 / BF01535081. PMID 2928844. S2CID 37896530.
- ^ а б «Ген Entrez: RBP4, ретинол-связывающий белок 4, плазма».
- ^ а б Cioffi CL, Dobri N, Freeman EE, Conlon MP, Chen P, Stafford DG, Schwarz DM, Golden KC, Zhu L, Kitchen DB, Barnes KD, Racz B, Qin Q, Michelotti E, Cywin CL, Martin WH, Pearson PG , Джонсон Г., Петрухин К. (сентябрь 2014 г.). «Дизайн, синтез и оценка неретиноидных антагонистов ретинол-связывающего белка 4 для потенциального лечения атрофической возрастной дегенерации желтого пятна и болезни Штаргардта». Журнал медицинской химии. 57 (18): 7731–57. Дои:10.1021 / jm5010013. ЧВК 4174998. PMID 25210858.
- ^ Канаи М., Раз А., Гудман Д.С. (сентябрь 1968 г.). «Ретинол-связывающий белок: транспортный белок для витамина А в плазме крови человека». Журнал клинических исследований. 47 (9): 2025–44. Дои:10.1172 / jci105889. ЧВК 297364. PMID 5675424.
- ^ Naylor HM, Newcomer ME (март 1999 г.). «Структура человеческого ретинол-связывающего белка (RBP) с его белком-носителем транстиретином обнаруживает взаимодействие с карбокси-концом RBP». Биохимия. 38 (9): 2647–53. Дои:10.1021 / bi982291i. PMID 10052934.
- ^ Раду Р.А., Хан Й., Буй ТВ, Нусиновиц С., Бок Д., Лихтер Дж., Виддер К., Трэвис Г. Х., Мата Н. Л. (декабрь 2005 г.). «Снижение уровня витамина А в сыворотке крови останавливает накопление токсичных флуорофоров сетчатки: потенциальная терапия для лечения заболеваний сетчатки на основе липофусцина». Исследовательская офтальмология и визуализация. 46 (12): 4393–401. Дои:10.1167 / iovs.05-0820. PMID 16303925.
- ^ Ян К., Грэм Т.Е., Моди Н., Прейтнер Ф., Перони О.Д., Заболотный Дж. М., Котани К., Квадро Л., Кан BB (июль 2005 г.). «Связывающий ретинол белок 4 сыворотки способствует развитию инсулинорезистентности при ожирении и диабете 2 типа». Природа. 436 (7049): 356–62. Дои:10.1038 / природа03711. PMID 16034410. S2CID 4343960.
- ^ Герман М.А., Кан BB (июль 2006 г.). «Транспорт и зондирование глюкозы в поддержании гомеостаза глюкозы и метаболической гармонии». Журнал клинических исследований. 116 (7): 1767–75. Дои:10.1172 / JCI29027. ЧВК 1483149. PMID 16823474.
- ^ Мораес-Виейра П.М., Йоре М.М., Дуайер П.М., Сайед И., Ариал П., Кан BB (март 2014 г.). «RBP4 активирует антигенпрезентирующие клетки, что приводит к воспалению жировой ткани и системной инсулинорезистентности». Клеточный метаболизм. 19 (3): 512–26. Дои:10.1016 / j.cmet.2014.01.018. ЧВК 4078000. PMID 24606904.
- ^ Галич С., Окхилл Дж. С., Стейнберг Г. Р. (март 2010 г.). «Жировая ткань как эндокринный орган». Молекулярная и клеточная эндокринология. 316 (2): 129–39. Дои:10.1016 / j.mce.2009.08.018. PMID 19723556. S2CID 7385199.
- ^ Chou CM, Nelson C, Tarlé SA, Pribila JT, Bardakjian T, Woods S, Schneider A, Glaser T (апрель 2015 г.). «Биохимическая основа доминирующего наследования, переменной проницаемости и материнских эффектов при врожденном заболевании глаз RBP4». Клетка. 161 (3): 634–646. Дои:10.1016 / j.cell.2015.03.006. ЧВК 4409664. PMID 25910211.
дальнейшее чтение
- Quadro L, Hamberger L, Colantuoni V, Gottesman ME, Blaner WS (декабрь 2003 г.). «Понимание физиологической роли ретинол-связывающего белка в метаболизме витамина А с использованием моделей трансгенных и нокаутных мышей». Молекулярные аспекты медицины. 24 (6): 421–30. Дои:10.1016 / S0098-2997 (03) 00038-4. PMID 14585313.
- Newcomer ME, Ong DE (октябрь 2000 г.). «Белок, связывающий ретинол плазмы: структура и функция прототипического липокалина». Biochimica et Biophysica Acta (BBA) - Структура белка и молекулярная энзимология. 1482 (1–2): 57–64. Дои:10.1016 / s0167-4838 (00) 00150-3. PMID 11058747.
- Fex G, Hansson B (февраль 1979 г.). «Ретинол-связывающий белок из мочи человека и его взаимодействие с ретинолом и преальбумином». Европейский журнал биохимии. 94 (1): 307–13. Дои:10.1111 / j.1432-1033.1979.tb12896.x. PMID 571335.
- Раск Л., Анунди Х, Петерсон П.А. (август 1979 г.). «Первичная структура ретинол-связывающего белка человека». Письма FEBS. 104 (1): 55–8. Дои:10.1016/0014-5793(79)81084-4. PMID 573217. S2CID 8540537.
- Fex G, Albertsson PA, Hansson B (сентябрь 1979 г.). «Взаимодействие между преальбумином и ретинол-связывающим белком изучено с помощью аффинной хроматографии, гель-фильтрации и двухфазного разделения». Европейский журнал биохимии. 99 (2): 353–60. Дои:10.1111 / j.1432-1033.1979.tb13263.x. PMID 574085.
- Monaco HL, Zanotti G (апрель 1992 г.). «Трехмерная структура и активный центр трех гидрофобных связывающих молекулы белков со значительным сходством аминокислотной последовательности». Биополимеры. 32 (4): 457–65. Дои:10.1002 / bip.360320425. PMID 1623143. S2CID 34994569.
- Cowan SW, Newcomer ME, Jones TA (1990). «Кристаллографическое уточнение человеческого белка, связывающего ретинол, при разрешении 2А». Белки. 8 (1): 44–61. Дои:10.1002 / prot.340080108. PMID 2217163. S2CID 21613341.
- Д'Онофрио К., Колантуони В., Кортезе Р. (август 1985 г.). «Структура и клеточно-специфическая экспрессия гена клонированного человеческого ретинол-связывающего белка: 5'-фланкирующая область содержит специфические для гепатомы транскрипционные сигналы». Журнал EMBO. 4 (8): 1981–9. Дои:10.1002 / j.1460-2075.1985.tb03881.x. ЧВК 554451. PMID 2998779.
- Пфеффер Б.А., Кларк В.М., Фланнери Дж. Г., Бок Д. (июль 1986 г.). «Мембранные рецепторы ретинол-связывающего белка в культивируемом пигментном эпителии сетчатки человека». Исследовательская офтальмология и визуализация. 27 (7): 1031–40. PMID 3013795.
- Камеко М., Итикава М., Кацуяма Т., Канаи М., Като М., Акамацу Т. (апрель 1986). «Иммуногистохимическая локализация ретинол-связывающего белка плазмы и преальбумина в островках поджелудочной железы человека». Гистохимический журнал. 18 (4): 164–8. Дои:10.1007 / BF01676116. PMID 3525470. S2CID 2959823.
- Siegenthaler G, Saurat JH (апрель 1987 г.). «Потеря ретинол-связывающих свойств для ретинол-связывающего белка плазмы в нормальном эпидермисе человека». Журнал следственной дерматологии. 88 (4): 403–8. Дои:10.1111 / 1523-1747.ep12469731. PMID 3559267.
- Раск Л., Валквист А., Петерсон П.А. (ноябрь 1971 г.). «Исследования двух физиологических форм человеческого ретинол-связывающего белка, различающихся по содержанию витамина А и аргинина». Журнал биологической химии. 246 (21): 6638–46. PMID 5132677.
- Колантуони В., Романо В., Бенси Дж., Санторо К., Костанцо Ф., Раугеи Дж., Кортезе Р. (ноябрь 1983 г.). «Клонирование и секвенирование полноразмерной кДНК, кодирующей человеческий ретинол-связывающий белок». Исследования нуклеиновых кислот. 11 (22): 7769–76. Дои:10.1093 / nar / 11.22.7769. ЧВК 326530. PMID 6316270.
- Newcomer ME, Jones TA, Aqvist J, Sundelin J, Eriksson U, Rask L, Peterson PA (июль 1984 г.). «Трехмерная структура ретинол-связывающего белка». Журнал EMBO. 3 (7): 1451–4. Дои:10.1002 / j.1460-2075.1984.tb01995.x. ЧВК 557543. PMID 6540172.
- Раск Л., Анунди Х., Беме Дж., Эрикссон Ю., Ронне Х., Сеге К., Петерсон П.А. (февраль 1981 г.). «Структурные и функциональные исследования белков, связывающих витамин А». Летопись Нью-Йоркской академии наук. 359: 79–90. Дои:10.1111 / j.1749-6632.1981.tb12739.x. PMID 6942701. S2CID 5781208.
- Jaconi S, Rose K, Hughes GJ, Saurat JH, Siegenthaler G (июнь 1995 г.). «Характеристика двух посттрансляционно процессированных форм человеческого ретинол-связывающего белка: измененные соотношения при хронической почечной недостаточности». Журнал липидных исследований. 36 (6): 1247–53. PMID 7666002.
- Берни Р., Малпели Дж., Фолли С., Муррелл Дж. Р., Лиепниекс Дж. Дж., Бенсон, доктор медицины (сентябрь 1994 г.). «Аминокислотная замена Ile-84 -> Ser в транстиретине препятствует взаимодействию с ретинол-связывающим белком плазмы». Журнал биологической химии. 269 (38): 23395–8. PMID 8089102.
- Зилигер М.В., Бисальский Х.К., Виссинджер Б., Голлник Х., Гилен С., Фрэнк Дж., Бек С., Зреннер Э. (январь 1999 г.). «Фенотип дефицита ретинола из-за наследственного дефекта синтеза ретинол-связывающего белка». Исследовательская офтальмология и визуализация. 40 (1): 3–11. PMID 9888420.
внешняя ссылка
- RBP4 + белок, + человек в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB за UniProt: P02753 (Ретинол-связывающий белок 4) на PDBe-KB.