Металлизация - Metalation
Металлизация (Альтернативное написание: Metallation) - это химическая реакция который включает в себя связь атома металла с тем, что обычно органический молекула с образованием нового соединения. Эта реакция обычно включает замену атома галогена в органической молекуле на атом металла с образованием металлоорганический сложный. В лаборатории обычно используют металлизацию для активировать органические молекулы во время образования связей C — X (где X обычно представляет собой углерод, кислород или азот), которые необходимы для синтеза многих органических молекул.
В синтезе металлизированные реагенты обычно участвуют в нуклеофильное замещение, одноэлектронный перенос (SET) и редокс химия с функциональными группами на других молекулах (включая, но не ограничиваясь, кетоны, альдегиды, и алкилгалогениды ). Металлизированные молекулы также могут участвовать в кислотно-щелочная химия, с одним металлоорганическим реагентом, депротонирующим органическую молекулу для создания нового металлоорганического реагента.
Наиболее распространенными классами металлизированных соединений являются литийорганические реагенты и Реактивы Гриньяра. Однако другие металлоорганические соединения, такие как цинкорганические соединения - также широко используются как в лабораторных, так и в промышленных целях.
История
Впервые металлирование было обнаружено в лаборатории Эдвардом Франкландом во время синтеза диэтилцинка в 1849 году.[1] Хотя это развитие в конечном итоге привело к развитию металлоорганических соединений других металлов,[2] эти соединения не нашли применения в лаборатории из-за их дороговизны и (в случае цинкорганических соединений) их высокой пирофорный природа. Реакции металлирования (особенно в форме трансметалляция ) стали широко использоваться в синтетических лабораториях только после Франсуа Огюст Виктор Гриньяр Синтезируют галогениды магния непосредственно из металлического магния и органических галогенидов.[3] Исключительная универсальность этих недавно обнаруженных магнийорганических реагентов в органическом синтезе привела к тому, что металлирование широко использовалось в лабораторных исследованиях.[4] Литийорганические реагенты были впервые синтезированы в 1917 году Шленком и Хольцем,[5] хотя эти реагенты не получили широкого распространения в качестве металлирующих агентов или реагентов в органическом синтезе до тех пор, пока Карл Циглер, Генри Гилман, и Георг Виттиг - среди прочего - разработали синтетические методы, которые улучшили этот первоначальный синтез.[6] После того, как стало известно об этих улучшениях в синтезе, интерес к соединениям значительно возрос, поскольку они, как правило, более реакционноспособны, чем магнийорганические соединения. Первое использование литийорганического реагента в качестве реагента для металлирования произошло в 1928 году, когда Шленк и Бергманн применили металлирование флуорена этиллитием.[7]
Реакционная способность и приложения
Наиболее простые металлизированные соединения коммерчески доступны как в твердой фазе, так и в фазе раствора, а металлизированные соединения в фазе раствора доступны в широком диапазоне растворителей и концентраций. Эти соединения также могут быть созданы в лаборатории в качестве на месте синтетический промежуточный продукт или отдельно в растворе.
Реакционная способность металлизированных соединений
Большая разница в электроотрицательность между атомом углерода и атомами металла в большинстве металлизированных соединений приводит к тому, что результирующая связь углерод-металл является высокой полярный. Высокая полярность связи - и, как следствие, высокая электронная плотность вокруг металлизированного атома углерода - приводит к тому, что электронный характер связи сильно напоминает характер связи ионный связь. Это делает металлизированные реагенты в целом хорошими. нуклеофилы, и сильный базы.
Металлизированные соединения чаще всего используются в органическом синтезе, где они действуют как нуклеофилы в нуклеофильное замещение реакции, сильные основания в депротонирование реакции, инициаторы в полимеризация реакции и исходные материалы для создания других металлизированных соединений в реакциях трансметаллирования.
Стерически затрудненные металлизированные соединения, такие как н-бутиллитий комплексы, часто используются как супербазы или инициаторы полимеризации, поскольку их стерическая масса препятствует способности соединения приближаться к нуклеофилам на расстояние, достаточно короткое для нуклеофильной атаки. Металлические соединения без высокой стерической пухлости, такие как метиллитий или алкил магний галогениды, чаще используются в качестве нуклеофилов или реагентов трансметаллирования, хотя высокая основность этих соединений часто требует защита основных функциональные группы найдено на органических молекулах.
Механизм
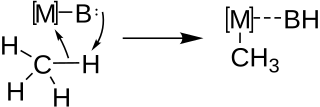
Металлирование обычно используется для синтеза сложных металлоорганических реагентов, таких как реагенты алкинилития, из сложных углеводородных молекул, которые обладают кислыми атомами водорода. Как для межмолекулярных, так и для внутримолекулярный При металлировании реакция происходит через кислотно-основную функционализацию связи C-H парой металл (M) - основание (B) в соответствии с общей схемой, приведенной ниже.
Относительная стабильность конечных продуктов этой реакции определяет, будет ли эта реакция обратимой, в то время как относительная кислотность связей C-H, присутствующих в металлизированной молекуле, будет определять место металлирования вновь образованного металлоорганического реагента.
Впервые металлирование было предложено следовать механизму согласованного металлирования-депротонирования (CMD) Винштейном и Трейлором в 1955 году, постулируя его на основе ртути. электрофильность при ацетолизе дифенилртути в уксусной кислоте.[8] Более поздние механистические исследования подтверждают существование этого механизма как для межмолекулярных, так и для внутримолекулярных реакций металлирования, приводящих к образованию металлоорганических соединений. Общепринятый механизм изображен ниже на примере металлирования первичного водорода.[9]
Трансметалляция
Трансметаллирование включает обмен двух металлов между органическими молекулами по механизму окислительно-восстановительного обмена. Например, трансметаллирование часто приводит к реакции между литийорганическим реагентом и солью металла.
Литийорганический реагент
При синтезе простых литийорганических реагентов восстановление одного эквивалента простого алкил- или арилгалогенида двумя эквивалентами металлического лития дает один эквивалент простого алкил- или ариллития и один эквивалент галогенида лития с хорошим выходом.[10]
Известно, что эта реакция протекает по радикальному пути, который, вероятно, инициируется механизмом одноэлектронного переноса типа, показанного ниже.[11]
Магний аналогичным образом металлирует галогениды с образованием Реактивы Гриньяра.
Рекомендации
- ^ Франкланд, Э. (1849). "Ueber die Isolirung der organischen Radicale". Европейский журнал органической химии. 71 (2): 171–213. Дои:10.1002 / jlac.18490710205.
- ^ Джонсон, W.C. (1939). "Die Chemie der Metall-Organischen Verbindungen (Krause, Erich; Grosse, A.V)". J. Chem. Образовательный. 16 (3): 148. Bibcode:1939JChEd..16..148J. Дои:10.1021 / ed016p148.1.
- ^ Гриньяр, В. (1900). "Sur quelques nouvelles combinaisons organométaliques du magnésium et leur application à des synthèses d'alcools et d'hydrocabures". Компт. Раздирать. 130: 1322–25.
- ^ Эйш, Джон Дж. (2002). «Генри Гилман: американский пионер в области металлоорганической химии в современной науке и технологиях». Металлоорганические соединения. 21 (25): 5439–5463. Дои:10.1021 / om0109408.
- ^ Schlenk, W .; Хольц, Дж. (1917). "Über die einfachsten Metallorganischen Alkaliverbindungen". Европейский журнал неорганической химии. 50 (1): 262–274. Дои:10.1002 / cber.19170500142.
- ^ Гилман, Х.; Zoellner, E. A .; Селби, У. М. (1932). «Улучшенная процедура получения литийорганических соединений». Варенье. Chem. Soc. 54 (5): 1957–1962. Дои:10.1021 / ja01344a033.
- ^ Шленк, Бергманн (1928). "II. Neuartige Erkenntnisse auf dem Gebiete der Stereochemie des Kohlenstoffs". Annalen der Chemie Юстуса Либиха. 463: 192. Дои:10.1002 / jlac.19284630103.
- ^ Винштейн, С .; Трейлор, Т. (1955). «Механизмы реакции ртутьорганических соединений. II. Электрофильное замещение на насыщенном углероде. Ацетолиз соединений диалкилртути». Варенье. Chem. Soc. 77 (14): 3747–3752. Дои:10.1021 / ja01619a021.
- ^ Lapointe, D .; Фагну, К. (2010). "Обзор механистической работы по согласованному пути металлизации-депротонирования". Письма по химии. 39 (11): 1118–1126. Дои:10.1246 / cl.2010.1118.
- ^ «Металлоорганические соединения в органическом синтезе», Шлоссер, М., Эд, Вили: Нью-Йорк, 1994. ISBN 0-471-93637-5
- ^ Бейли, Уильям Ф .; Патрисия, Джеффри Дж. (1988). «Механизм реакции обмена лития и галогена: обзор литературы». Журнал металлоорганической химии. 352 (1–2): 1–46. Дои:10.1016 / 0022-328x (88) 83017-1.