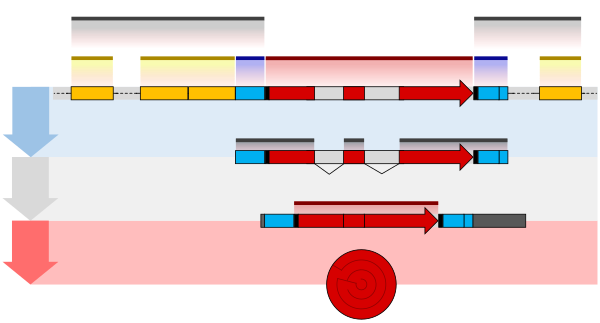
Структура гена - Gene structure
Структура гена это организация специализированных последовательность элементы в ген. Гены содержат информацию, необходимую для жизни клетки выжить и воспроизвести.[1][2] У большинства организмов гены состоят из ДНК, где конкретная последовательность ДНК определяет функцию гена. Ген записано (скопировано) из ДНК в РНК, которые могут быть либо некодирующими (нкРНК ) с прямой функцией или промежуточным мессенджером (мРНК ), который затем переводится в белок. Каждый из этих шагов контролируется конкретными элементами последовательности или участками в гене. Следовательно, каждый ген требует, чтобы несколько элементов последовательности функционировали.[2] Это включает последовательность, которая на самом деле кодирует функционал белок или нкРНК, а также множественные регуляторная последовательность регионы. Эти регионы могут быть всего несколько пар оснований, длиной до многих тысяч пар оснований.
Большая часть генной структуры в целом похожа между эукариоты и прокариоты. Эти общие элементы во многом являются результатом общая родословная из клеточная жизнь в организмах более 2 миллиардов лет назад.[3] Ключевые различия в структуре генов между эукариотами и прокариотами отражают их разные механизмы транскрипции и трансляции.[4][5] Понимание структуры гена - основа понимания гена аннотация, выражение, и функция.[6]
Общие черты
Структуры как эукариотических, так и прокариотических генов включают несколько элементов вложенной последовательности. Каждый элемент выполняет определенную функцию в многоэтапном процессе экспрессия гена. Последовательности и длина этих элементов различаются, но в большинстве генов присутствуют одни и те же общие функции.[2] Несмотря на то что ДНК представляет собой двухцепочечную молекулу, обычно только одна из цепей кодирует информацию, которую РНК-полимераза читает, чтобы произвести кодирование белков мРНК или некодирующая РНК. Эта «смысловая» или «кодирующая» нить проходит от 5 футов до 3 дюймов. направление где числа относятся к атомам углерода основной цепи. рибоза сахар. В открытая рамка чтения (ORF) гена поэтому обычно представляют в виде стрелки, указывающей направление, в котором читается смысловая цепь.[7]
Нормативные последовательности расположены на концах генов. Эти участки последовательности могут быть либо рядом с транскрибируемой областью ( промоутер ) или разделенных множеством килобаз (усилители и глушители ).[8] Промотор расположен на 5'-конце гена и состоит из коровой промоторной последовательности и проксимальной промоторной последовательности. Основной промотор отмечает место начала транскрипции, связывая РНК-полимеразу и другие белки, необходимые для копирования ДНК в РНК. Проксимальная область промотора связывает факторы транскрипции которые модифицируют сродство основного промотора к РНК-полимеразе.[9][10] Гены могут регулироваться множественными последовательностями энхансеров и сайленсеров, которые дополнительно модифицируют активность промоторов путем связывания активатор или же репрессор белки.[11][12] Энхансеры и сайленсеры могут быть расположены далеко от гена, на расстоянии многих тысяч пар оснований. Следовательно, связывание разных факторов транскрипции регулирует скорость инициации транскрипции в разное время и в разных клетках.[13]
Регуляторные элементы могут перекрывать друг друга, при этом участок ДНК может взаимодействовать со многими конкурирующими активаторами и репрессорами, а также с РНК-полимеразой. Например, некоторые репрессорные белки могут связываться с коровым промотором для предотвращения связывания полимеразы.[14] Для генов с множеством регуляторных последовательностей скорость транскрипции является продуктом всех элементов вместе взятых.[15] Связывание активаторов и репрессоров с множеством регуляторных последовательностей оказывает совместное действие на инициацию транскрипции.[16]
Хотя все организмы используют как активаторы транскрипции, так и репрессоры, говорят, что гены эукариот «отключены по умолчанию», тогда как гены прокариот «включены».[5] Для экспрессии корового промотора эукариотических генов обычно требуется дополнительная активация промоторными элементами. Основной промотор прокариотических генов, наоборот, достаточен для сильной экспрессии и регулируется репрессорами.[5]
Дополнительный уровень регуляции возникает для генов, кодирующих белок, после того, как мРНК была обработана для подготовки ее к трансляции в белок. Только область между Начните и остановка кодонов кодирует конечный белковый продукт. Фланговый непереведенные регионы (UTR) содержат дополнительные регуляторные последовательности.[18] В 3 'UTR содержит терминатор последовательность, которая отмечает конечную точку транскрипции и высвобождает РНК-полимеразу.[19] В 5 ’UTR связывает рибосома, что переводит белок-кодирующая область в цепочку аминокислоты который складывать для формирования конечного белкового продукта. В случае генов некодирующих РНК РНК не транслируется, а вместо этого транслируется. складки быть непосредственно функциональным.[20][21]
Эукариоты
В структуру эукариотических генов входят черты, отсутствующие у прокариот. Большинство из них относятся к посттранскрипционная модификация из пре-мРНК производить зрелая мРНК готов к переводу в белок. Эукариотические гены обычно имеют больше регуляторных элементов для контроля экспрессии генов по сравнению с прокариотами.[5] Это особенно верно в многоклеточный эукариоты, например, люди, у которых экспрессия генов широко варьируется среди разных ткани.[11]
Ключевой особенностью структуры эукариотических генов является то, что их транскрипты обычно подразделяются на экзон и интрон регионы. Области экзонов сохраняются в финальном зрелая мРНК молекулы, а интронные области сращен (вырезано) во время пост-транскрипционной обработки.[22] В самом деле, интронные области гена могут быть значительно длиннее, чем экзонные области. После сплайсинга экзоны образуют единые непрерывные области, кодирующие белок, и границы сплайсинга не обнаруживаются. Посттранскрипционный процессинг эукариот также добавляет Крышка 5 футов к началу мРНК и полиаденозиновый хвост до конца мРНК. Эти добавки стабилизируют мРНК и направляют ее транспорт от ядро к цитоплазма, хотя ни одна из этих особенностей непосредственно не кодируется в структуре гена.[18]
Прокариоты
Общая организация прокариотических генов заметно отличается от таковой у эукариот. Наиболее очевидное различие состоит в том, что ОРС прокариот часто сгруппированы в полицистронный оперон под контролем общего набора регуляторных последовательностей. Все ORF транскрибируются на одной и той же мРНК, поэтому они совместно регулируются и часто выполняют связанные функции.[23][24] У каждой ORF обычно свой сайт связывания рибосомы (RBS), так что рибосомы одновременно транслируют ORF на одной и той же мРНК. Некоторые опероны также демонстрируют трансляционную связь, когда скорости трансляции нескольких ORF внутри оперона связаны.[25] Это может происходить, когда рибосома остается прикрепленной к концу ORF и просто перемещается к следующей без необходимости в новом RBS.[26] Трансляционное соединение также наблюдается, когда трансляция ORF влияет на доступность следующей RBS через изменения вторичной структуры РНК.[27] Наличие нескольких ORF на одной мРНК возможно только у прокариот, потому что их транскрипция и трансляция происходят в одно и то же время и в одном и том же субклеточном местоположении.[23][28]
В оператор Последовательность рядом с промотором является основным регуляторным элементом у прокариот. Белки-репрессоры, связанные с последовательностью оператора, физически препятствуют ферменту РНК-полимеразы, предотвращая транскрипцию.[29][30] Рибопереключатели являются еще одной важной регуляторной последовательностью, обычно присутствующей в прокариотических UTR. Эти последовательности переключаются между альтернативными вторичными структурами в РНК в зависимости от концентрации ключевых метаболиты. Вторичные структуры затем либо блокируют, либо выявляют важные участки последовательности, такие как RBS. Интроны крайне редки у прокариот и поэтому не играют значительной роли в регуляции прокариотических генов.[31]
Рекомендации
![]() Эта статья была адаптирована из следующего источника под CC BY 4.0 лицензия (2017 ) (отчеты рецензента ): «Структура эукариотических и прокариотических генов», WikiJournal of Медицина, 4 (1), 2017, Дои:10.15347 / WJM / 2017.002, ISSN 2002-4436, Викиданные Q28867140
Эта статья была адаптирована из следующего источника под CC BY 4.0 лицензия (2017 ) (отчеты рецензента ): «Структура эукариотических и прокариотических генов», WikiJournal of Медицина, 4 (1), 2017, Дои:10.15347 / WJM / 2017.002, ISSN 2002-4436, Викиданные Q28867140
- ^ Альбертс, Брюс; Джонсон, Александр; Льюис, Джулиан; Рафф, Мартин; Робертс, Кейт; Уолтер, Питер (2002). «Как работают генетические переключатели». Молекулярная биология клетки (4-е изд.).
- ^ а б c Поляк, Корнелия; Мейерсон, Мэтью (2003). «Обзор: структура гена». Онкология (6 изд.). BC Decker.
- ^ Вернер, Финн; Громанн, Дина (2011). «Эволюция мультисубъединичных РНК-полимераз в трех областях жизни». Обзоры природы Микробиология. 9 (2): 85–98. Дои:10.1038 / nrmicro2507. ISSN 1740-1526. PMID 21233849.
- ^ Козак, Мэрилин (1999). «Инициирование трансляции у прокариот и эукариот». Ген. 234 (2): 187–208. Дои:10.1016 / S0378-1119 (99) 00210-3. ISSN 0378-1119. PMID 10395892.
- ^ а б c d Struhl, Кевин (1999). «Принципиально разная логика регуляции генов у эукариот и прокариот». Клетка. 98 (1): 1–4. Дои:10.1016 / S0092-8674 (00) 80599-1. ISSN 0092-8674. PMID 10412974.
- ^ Альбертс Б., Джонсон А., Льюис Дж, Рафф М., Робертс К., Уолтер П. (2002). Молекулярная биология клетки (Четвертое изд.). Нью-Йорк: Наука о гирляндах. ISBN 978-0-8153-3218-3.
- ^ Лу, Г. (2004). «Vector NTI, сбалансированный комплексный комплекс для анализа последовательностей». Брифинги по биоинформатике. 5 (4): 378–88. Дои:10.1093 / bib / 5.4.378. ISSN 1467-5463. PMID 15606974.
- ^ Вайпер-Бержерон, Надин; Скерянц, Илона С. (2009). Транскрипция и контроль экспрессии генов. Humana Press. С. 33–49. Дои:10.1007/978-1-59745-440-7_2. ISBN 978-1-59745-440-7.
- ^ Томас, Мэри С .; Чан, Ченг-Мин (2008). «Общая транскрипционная машина и общие кофакторы». Критические обзоры в биохимии и молекулярной биологии. 41 (3): 105–78. CiteSeerX 10.1.1.376.5724. Дои:10.1080/10409230600648736. ISSN 1040-9238. PMID 16858867.
- ^ Ювен-Гершон, Тамар; Сюй, Жер-Юань; Тайзен, Джошуа WM; Кадонага, Джеймс Т (2008). «Основной промотор РНК-полимеразы II - путь к транскрипции». Текущее мнение в области клеточной биологии. 20 (3): 253–59. Дои:10.1016 / j.ceb.2008.03.003. ISSN 0955-0674. ЧВК 2586601. PMID 18436437.
- ^ а б Maston, Glenn A .; Эванс, Сара К .; Грин, Майкл Р. (2006). «Элементы регуляции транскрипции в геноме человека». Ежегодный обзор геномики и генетики человека. 7 (1): 29–59. Дои:10.1146 / annurev.genom.7.080505.115623. ISSN 1527-8204. PMID 16719718. S2CID 12346247.
- ^ Pennacchio, L.A .; Bickmore, W .; Дин, А .; Нобрега, М. А .; Бежерано, Г. (2013). «Усилители: пять важных вопросов». Природа Обзоры Генетика. 14 (4): 288–95. Дои:10.1038 / nrg3458. ЧВК 4445073. PMID 23503198.
- ^ Maston, G.A .; Evans, S.K .; Грин, М. Р. (2006). «Элементы регуляции транскрипции в геноме человека». Ежегодный обзор геномики и генетики человека. 7: 29–59. Дои:10.1146 / annurev.genom.7.080505.115623. PMID 16719718. S2CID 12346247.
- ^ Огборн, Стивен; Анталис, Тони М. (1998). «Транскрипционный контроль и роль сайленсеров в регуляции транскрипции у эукариот». Биохимический журнал. 331 (1): 1–14. Дои:10.1042 / bj3310001. ISSN 0264-6021. ЧВК 1219314. PMID 9512455.
- ^ Buchler, N.E .; Gerland, U .; Хва, Т. (2003). «О схемах комбинаторной логики транскрипции». Труды Национальной академии наук. 100 (9): 5136–41. Bibcode:2003ПНАС..100.5136Б. Дои:10.1073 / pnas.0930314100. ISSN 0027-8424. ЧВК 404558. PMID 12702751.
- ^ Каземян, М .; Pham, H .; Wolfe, S.A .; Бродский, М. Х .; Синха, С. (11 июля 2013 г.). «Широко распространенные доказательства кооперативного связывания ДНК факторами транскрипции в развитии дрозофилы». Исследования нуклеиновых кислот. 41 (17): 8237–52. Дои:10.1093 / nar / gkt598. ЧВК 3783179. PMID 23847101.
- ^ а б Шафи, Томас; Лоу, Рохан (2017). «Структура эукариотических и прокариотических генов». WikiJournal of Медицина. 4 (1). Дои:10.15347 / wjm / 2017.002. ISSN 2002-4436.
- ^ а б Гуханийоги, Джайита; Брюэр, Гэри (2001). «Регулирование стабильности мРНК в клетках млекопитающих». Ген. 265 (1–2): 11–23. Дои:10.1016 / S0378-1119 (01) 00350-X. ISSN 0378-1119. PMID 11255003.
- ^ Кюнер, Джейсон Н .; Пирсон, Эрика Л .; Мур, Клэр (2011). «Разоблачение средств достижения цели: прекращение транскрипции РНК-полимеразы II». Обзоры природы Молекулярная клеточная биология. 12 (5): 283–94. Дои:10.1038 / nrm3098. ISSN 1471-0072. ЧВК 6995273. PMID 21487437.
- ^ Маттик, Дж. С. (2006). «Некодирующая РНК». Молекулярная генетика человека. 15 (90001): R17 – R29. Дои:10.1093 / hmg / ddl046. ISSN 0964-6906. PMID 16651366.
- ^ Палаццо, Александр Ф .; Ли, Элиза С. (2015). «Некодирующая РНК: что функционально, а что нежелательно?». Границы генетики. 6: 2. Дои:10.3389 / fgene.2015.00002. ISSN 1664-8021. ЧВК 4306305. PMID 25674102.
- ^ Матера, А. Грегори; Ван, Цефэн (2014). «Один день из жизни сплайсосомы». Обзоры природы Молекулярная клеточная биология. 15 (2): 108–21. Дои:10.1038 / nrm3742. ISSN 1471-0072. ЧВК 4060434. PMID 24452469.
- ^ а б Salgado, H .; Moreno-Hagelsieb, G .; Smith, T .; Колладо-Видес, Дж. (2000). «Опероны кишечной палочки: геномный анализ и прогнозы». Труды Национальной академии наук. 97 (12): 6652–57. Bibcode:2000PNAS ... 97.6652S. Дои:10.1073 / pnas.110147297. ЧВК 18690. PMID 10823905.
- ^ Джейкоб, Ф .; Моно, Дж. (1961-06-01). «Генетические механизмы регуляции синтеза белков». Журнал молекулярной биологии. 3 (3): 318–56. Дои:10.1016 / с0022-2836 (61) 80072-7. ISSN 0022-2836. PMID 13718526.
- ^ Тиан, Тиан; Салис, Ховард М. (2015). «Прогностическая биофизическая модель трансляционного связывания для координации и контроля экспрессии белка в бактериальных оперонах». Исследования нуклеиновых кислот. 43 (14): 7137–51. Дои:10.1093 / нар / gkv635. ISSN 0305-1048. ЧВК 4538824. PMID 26117546.
- ^ Шюмперли, Даниэль; Маккенни, Кейт; Собески, Донна А .; Розенберг, Мартин (1982). «Трансляционная связь на интерцистронной границе галактозного оперона Escherichia coli». Клетка. 30 (3): 865–71. Дои:10.1016/0092-8674(82)90291-4. ISSN 0092-8674. PMID 6754091.
- ^ Левин-Карп, Айелет; Баренхольц, Ури; Барейя, Тасним; Даяги, Михал; Zelcbuch, Lior; Антоновский, Нив; Нур, Элад; Майло, Рон (2013). «Количественная оценка трансляционного связывания в синтетических оперонах E. coli с использованием модуляции RBS и флуоресцентных репортеров». Синтетическая биология ACS. 2 (6): 327–36. Дои:10.1021 / sb400002n. ISSN 2161-5063. PMID 23654261. S2CID 63692.
- ^ Льюис, Митчелл (июнь 2005 г.). «Лак репрессор». Comptes Rendus Biologies. 328 (6): 521–48. Дои:10.1016 / j.crvi.2005.04.004. PMID 15950160.
- ^ МакКлюр, В. Р. (1985). «Механизм и контроль инициации транскрипции у прокариот». Ежегодный обзор биохимии. 54 (1): 171–204. Дои:10.1146 / annurev.bi.54.070185.001131. ISSN 0066-4154. PMID 3896120.
- ^ Белл, Чарльз Э; Льюис, Митчелл (2001). «Репрессор Lac: второе поколение структурных и функциональных исследований». Текущее мнение в структурной биологии. 11 (1): 19–25. Дои:10.1016 / S0959-440X (00) 00180-9. ISSN 0959-440X. PMID 11179887.
- ^ Родригес-Треллес, Франсиско; Таррио, Роза; Айяла, Франсиско Дж. (2006). «Происхождение и эволюция сплайсосомных интронов». Ежегодный обзор генетики. 40 (1): 47–76. Дои:10.1146 / annurev.genet.40.110405.090625. ISSN 0066-4197. PMID 17094737.
внешняя ссылка
- GSDS - Сервер отображения генной структуры