Три основных непереведенных региона - Three prime untranslated region
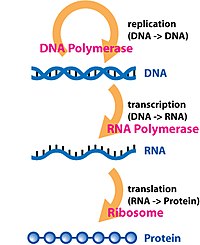

В молекулярная генетика, то три основных непереведенных региона (3'-UTR) - это раздел информационная РНК (мРНК), которая следует сразу за перевод завершающий кодон. 3'-UTR часто содержит регуляторные области, которые посттранскрипционное влияние экспрессия гена.
В течение экспрессия гена, молекула мРНК записано от ДНК последовательность и позже переведено в белок. Некоторые участки молекулы мРНК не транслируются в белок, включая Крышка 5 футов, 5 'непереведенный регион, 3 'нетранслируемая область и поли (А) хвост. Регуляторные регионы в 3'-нетранслируемой области могут влиять на полиаденилирование, эффективность трансляции, локализация и стабильность мРНК.[1][2] 3'-UTR содержит как сайты связывания для регуляторных белков, так и микроРНК (миРНК). Связываясь со специфическими сайтами в 3'-UTR, miRNA могут снижать экспрессию генов различных мРНК, либо ингибируя трансляцию, либо напрямую вызывая деградацию транскрипта. 3'-UTR также имеет глушитель регионы, которые связаны с репрессор белки и будут ингибировать экспрессию мРНК.
Многие 3'-UTR также содержат Элементы с высоким содержанием Австралии (ARE). Белки связывают ARE, чтобы локализованно влиять на стабильность или скорость распада транскриптов или влиять на инициацию трансляции. Кроме того, 3'-UTR содержит последовательность AAUAAA, которая управляет добавлением нескольких сотен остатков аденина, называемых поли (А) хвост до конца транскрипта мРНК. Поли (A) связывающий белок (PABP) связывается с этим хвостом, внося вклад в регуляцию трансляции, стабильности и экспорта мРНК. Например, PABP, связанный с поли (A) хвостом, взаимодействует с белками, связанными с 5'-концом транскрипта, вызывая циркуляризацию мРНК, которая способствует трансляции.
3'-UTR может также содержать последовательности, которые привлекают белки для связывания мРНК с цитоскелет, перевезти его в или из ядро клетки, или выполнить другие типы локализации. В дополнение к последовательностям в пределах 3'-UTR, физические характеристики области, включая ее длину и вторичная структура, способствовать регулированию перевода. Эти разнообразные механизмы регуляции генов гарантируют, что правильные гены экспрессируются в правильных клетках в соответствующее время.
Физические характеристики
3'-UTR мРНК выполняет множество регуляторных функций, которые контролируются физическими характеристиками региона. Одной из таких характеристик является длина 3'-UTR, которая в млекопитающее геном имеет значительные вариации. Эта область транскрипта мРНК может варьироваться от 60 нуклеотиды до примерно 4000.[3] В среднем длина 3'-UTR у человека составляет примерно 800 нуклеотидов, в то время как средняя длина 5'-UTR составляет всего около 200 нуклеотидов.[4] Длина 3'-UTR важна, поскольку более длинные 3'-UTR связаны с более низкими уровнями экспрессии гена. Одно из возможных объяснений этого феномена состоит в том, что более длинные области имеют более высокую вероятность обладания большим количеством сайтов связывания miRNA, которые обладают способностью ингибировать трансляцию. Помимо длины, нуклеотидный состав также значительно различается между 5'- и 3'-UTR. Значение G + C процент 5'-UTR у теплокровных позвоночных составляет около 60% по сравнению только с 45% для 3'-UTR. Это важно, поскольку наблюдалась обратная корреляция между G + C% 5 'и 3'-UTR и их соответствующими длинами. UTR, которые бедны GC, обычно длиннее, чем UTR, расположенные в геномных областях, богатых GC.[4]
Последовательности в 3'-UTR также обладают способностью деградировать или стабилизировать транскрипт мРНК. Модификации, контролирующие стабильность транскрипта, позволяют быстро контролировать экспрессию гена без изменения скорости трансляции. Одна группа элементов в 3'-UTR, которые могут помочь дестабилизировать транскрипт мРНК, - это Элементы с высоким содержанием Австралии (ARE). Эти элементы имеют размер от 50 до 150 пар оснований и обычно содержат несколько копий пентануклеотида AUUUA. Ранние исследования показали, что ARE могут различаться по последовательности и делиться на три основных класса, которые различаются количеством и расположением мотивов.[1] Другой набор элементов, который присутствует как в 5 ', так и в 3'-UTR, - это железные ответные элементы (IRE). IRE представляет собой структуру стержень-петля в нетранслируемых областях мРНК, которые кодируют белки, участвующие в метаболизме клеточного железа. Транскрипт мРНК, содержащий этот элемент, либо разрушается, либо стабилизируется в зависимости от связывания конкретных белков и концентраций внутриклеточного железа.[3]
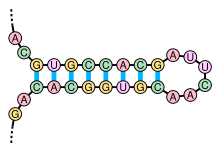
3'-UTR также содержит последовательности, которые сигнализируют о добавлении, которое необходимо сделать, либо к самому транскрипту, либо к продукту трансляции. Например, в 3'-UTR присутствуют два разных сигнала полиаденилирования, которые сигнализируют о добавлении поли (А) хвоста. Эти сигналы инициируют синтез поли (А) хвоста определенной длины, составляющей около 250 пар оснований.[1] Используемый первичный сигнал - это ядерное полиаденилирование signal (PAS) с последовательностью AAUAAA, расположенной ближе к концу 3'-UTR.[3] Однако на раннем этапе развития цитоплазматическое полиаденилирование может происходить вместо этого и регулировать активацию трансляции материнских мРНК. Элемент, который управляет этим процессом, называется CPE, богатый AU и также расположенный в 3'-UTR. CPE обычно имеет структуру UUUUUUAU и обычно находится в пределах 100 пар оснований от ядерного PAS.[3] Другое специфическое добавление, о котором сигнализирует 3'-UTR, - это включение селеноцистеина в кодоны UGA мРНК, кодирующих селенопротеины. Обычно кодон UGA кодирует остановку трансляции, но в этом случае сохраняется стебель-петля структура называется последовательность вставки селеноцистеина (SECIS) причины для введения селеноцистеина вместо этого.[4]
Роль в экспрессии генов
3'-нетранслируемая область играет решающую роль в экспрессии генов, влияя на локализацию, стабильность, экспорт и эффективность трансляции мРНК. Он содержит различные последовательности, которые участвуют в экспрессии генов, включая элементы ответа микроРНК (MRE), AU-богатые элементы (ARE) и поли (A) хвост. Кроме того, структурные характеристики 3'-UTR, а также использование им альтернативного полиаденилирования играют роль в экспрессии генов.

Элементы ответа микроРНК
3'-UTR часто содержит элементы ответа микроРНК (MRE), которые представляют собой последовательности, с которыми связываются миРНК. miRNA - это короткие некодирующие молекулы РНК, способные связываться с транскриптами мРНК и регулировать их экспрессию. Один механизм miRNA включает частичное базовая пара 5'-затравочной последовательности миРНК к MRE в 3'-UTR мРНК; это связывание затем вызывает репрессию трансляции.
Элементы с высоким содержанием Австралии
Помимо содержания MRE, 3'-UTR также часто содержит Элементы, богатые Австралийским Союзом (ARE), которые имеют длину от 50 до 150 п.н. и обычно включают множество копий последовательности AUUUA. Связывающие белки ARE (ARE-BP) связываются с элементами, богатыми AU, способом, который зависит от типа ткани, типа клетки, времени, клеточной локализации и окружающей среды. В ответ на различные внутриклеточные и внеклеточные сигналы ARE-BP могут способствовать распаду мРНК, влиять на стабильность мРНК или активировать трансляцию. Этот механизм регуляции генов участвует в росте клеток, клеточная дифференциация, адаптация к внешним раздражителям. Следовательно, он действует на кодирование транскриптов. цитокины, факторы роста, опухолевые супрессоры, протоонкогены, циклины, ферменты, факторы транскрипции, рецепторы, и мембранные белки.[1]
Поли (А) хвост

Поли (A) хвост содержит сайты связывания для поли (A) связывающих белков (PABP). Эти белки взаимодействуют с другими факторами, влияя на экспорт, стабильность, распад и трансляцию мРНК. PABP, связанные с поли (A) хвостом, могут также взаимодействовать с белками, такими как факторы инициации трансляции, которые связаны с 5'-кэпом мРНК. Это взаимодействие вызывает циркуляризацию транскрипта, что впоследствии способствует инициации трансляции. Кроме того, он обеспечивает эффективный перевод за счет повторного использования рибосомы.[1][2] В то время как присутствие поли (A) -хвоста обычно способствует запуску трансляции, его отсутствие или удаление часто приводит к опосредованной экзонуклеазой деградации мРНК. Само полиаденилирование регулируется последовательностями в 3'-UTR транскрипта. Эти последовательности включают цитоплазматические элементы полиаденилирования (CPE), которые представляют собой богатые уридином последовательности, которые вносят вклад как в активацию, так и в репрессию полиаденилирования. CPE-связывающий белок (CPEB) связывается с CPE в сочетании с множеством других белков, чтобы вызвать различные ответы.[2]
Структурные характеристики
Хотя последовательность, составляющая 3'-UTR, вносит большой вклад в экспрессию гена, структурные характеристики 3'-UTR также играют большую роль. В общем, более длинные 3'-UTR соответствуют более низким скоростям экспрессии, поскольку они часто содержат больше miRNA и сайтов связывания белков, которые участвуют в ингибировании трансляции.[1][2][5] Человек транскрипты обладают 3'-UTR, которые в среднем вдвое длиннее 3'-UTR других млекопитающих. Эта тенденция отражает высокий уровень сложности регуляции генов человека. Помимо длины, вторичная структура 3'-нетранслируемой области также выполняет регуляторные функции. Белковые факторы могут способствовать или нарушать сворачивание области в различные вторичные структуры. Наиболее распространенной структурой является стержень-петля, которая обеспечивает каркас для РНК-связывающих белков и некодирующих РНК, влияющих на экспрессию транскрипта.[1]

Альтернативное полиаденилирование
Другой механизм, затрагивающий структуру 3'-UTR, называется альтернативным полиаденилированием (APA), которое приводит к образованию мРНК. изоформы которые отличаются только своими 3'-UTR. Этот механизм особенно полезен для сложных организмы поскольку он обеспечивает средства экспрессии одного и того же белка, но в разных количествах и в разных местах. Он используется примерно половиной генов человека. APA может быть результатом наличия нескольких сайтов полиаденилирования или взаимоисключающих концевых экзоны. Поскольку он может влиять на присутствие белков и сайтов связывания miRNA, APA может вызывать дифференциальную экспрессию транскриптов мРНК, влияя на их стабильность, экспорт в цитоплазму и эффективность трансляции.[1][5][6]
Методы исследования
Ученые используют ряд методов для изучения сложных структур и функций 3 ′ UTR. Даже если показано, что данная 3'-UTR в мРНК присутствует в ткани, необходимо определить эффекты локализации, функционального периода полужизни, трансляционной эффективности и транс-действующих элементов, чтобы понять полную функциональность 3'-UTR. .[7] Вычислительные подходы, в первую очередь с помощью анализа последовательностей, показали наличие ARE примерно в 5-8% человеческих 3'-UTR и присутствие одной или нескольких мишеней miRNA в 60% или более человеческих 3'-UTR. Программное обеспечение может быстро сравнивать миллионы последовательностей одновременно, чтобы найти сходство между различными 3'-UTR в геноме. Экспериментальные подходы использовались для определения последовательностей, которые ассоциируются со специфическими РНК-связывающими белками; в частности, недавние улучшения в последовательность действий и методы перекрестного связывания позволили точно картировать сайты связывания белков в транскрипте.[8] Индуцированные сайт-специфические мутации, например те, которые влияют на кодон терминации, сигнал полиаденилирования или вторичную структуру 3'-UTR, могут показать, как мутированные области могут вызывать нарушение регуляции трансляции и заболевание.[9] Эти типы методов для всего транскрипта должны помочь нам понять известные цис-элементы и транс-регуляторные факторы в 3'-UTR.
Болезнь

Мутации 3'-UTR могут иметь очень серьезные последствия, потому что одно изменение может отвечать за измененную экспрессию многих генов. Транскрипционно мутация может влиять только на аллель и гены, которые физически связаны. Однако, поскольку белки, связывающие 3'-UTR, также участвуют в процессинге и ядерном экспорте мРНК, мутация также может влиять на другие неродственные гены.[9] Нарушение регуляции ARE-связывающих белков (AUBP) из-за мутаций в AU-богатых регионах может привести к заболеваниям, включая туморогенез (рак), злокачественные заболевания кроветворения, лейкемогенез и задержка развития / расстройства аутистического спектра.[10][11][12] Увеличенное количество тринуклеотидных (CTG) повторов в 3’-UTR протеинкиназа миотонической дистрофии (DMPK) ген вызывает миотоническая дистрофия.[7] Вставка 3-килобазным ретранслятором последовательностей тандемных повторов в 3'-UTR белка фукутина связана с врожденной мышечной дистрофией Фукуямы.[7] Элементы в 3'-UTR также были связаны с человеческими острый миелоидный лейкоз, альфа-талассемия, нейробластома, Кератинопатия, Аниридия, Синдром IPEX, и врожденные пороки сердца.[9] Несколько выявленных заболеваний, опосредованных UTR, лишь намекают на бесчисленные связи, которые еще предстоит обнаружить.
Дальнейшее развитие
Несмотря на наше текущее понимание 3'-UTR, они все еще остаются относительной загадкой. Поскольку мРНК обычно содержат несколько перекрывающихся элементов управления, часто бывает трудно определить идентичность и функцию каждого элемента 3'-UTR, не говоря уже о регуляторных факторах, которые могут связываться с этими сайтами. Кроме того, каждая 3'-UTR содержит множество альтернативных AU-богатых элементов и сигналов полиаденилирования. Эти цис- и транс-действующие элементы, наряду с miRNA, предлагают практически безграничный диапазон возможностей контроля в пределах одной мРНК.[7] Будущие исследования за счет более широкого использования основанного на глубоком секвенировании профилирование рибосом раскроет больше тонкостей регулирования, а также новые элементы управления и AUBP.[1] Кроме того, окончательная судьба стенограммы зависит от преобразование сигнала пути, в котором он участвует, поэтому дальнейшие исследования в этой области выглядят многообещающими.
Смотрите также
Рекомендации
- ^ а б c d е ж грамм час я Барретт, Люси У .; Флетчер, Сью; Уилтон, Стив Д. (27 апреля 2012 г.). «Регулирование экспрессии эукариотических генов с помощью нетранслируемых участков генов и других некодирующих элементов». Клеточные и молекулярные науки о жизни. 69 (21): 3613–3634. Дои:10.1007 / s00018-012-0990-9. ЧВК 3474909. PMID 22538991.
- ^ а б c d Пишон, Ксавьер; А. Уилсон, Линдси; Стоунли, Марк; Бастид, Амандин; Король, Елена; Сомерс, Джоанна; Э. Уиллис, Энн (1 июля 2012 г.). «Взаимодействие РНК-связывающий белок / элемент РНК и контроль трансляции». Современная наука о белках и пептидах. 13 (4): 294–304. Дои:10.2174/138920312801619475. ЧВК 3431537. PMID 22708490.
- ^ а б c d Хескет, Джон (23 сентября 2005 г.). 3'UTR и правила. Энциклопедия наук о жизни. Дои:10.1038 / npg.els.0005011. ISBN 978-0470016176.
- ^ а б c Миньоне, Флавио; Грациано Песоле (15 августа 2011 г.). Нетранслируемые области мРНК (UTR). eLS. Дои:10.1002 / 9780470015902.a0005009.pub2. ISBN 978-0470016176.
- ^ а б Ди Джаммартино, Дафне Кампильи; Нисида, Кенсей; Мэнли, Джеймс Л. (2011). «Механизмы и последствия альтернативного полиаденилирования». Молекулярная клетка. 43 (6): 853–866. Дои:10.1016 / j.molcel.2011.08.017. ЧВК 3194005. PMID 21925375.
- ^ Праудфут, Н. Дж. (2011). «Конец сообщения: poly (A) сигналы тогда и сейчас». Гены и развитие. 25 (17): 1770–1782. Дои:10.1101 / gad.17268411. ЧВК 3175714. PMID 21896654.
- ^ а б c d Коннэ, Беатрис; Штутц, Андре; Вассалли, Жан-Доминик (1 июня 2000 г.). «3'-нетранслируемая область информационной РНК: молекулярная« горячая точка »патологии?». Природа Медицина. 6 (6): 637–641. Дои:10.1038/76211. PMID 10835679.
- ^ Zhao, W .; Благев, Д .; Pollack, J. L .; Эрле, Д. Дж. (4 мая 2011 г.). «На пути к систематическому пониманию 3 'нетранслируемых областей мРНК». Труды Американского торакального общества. 8 (2): 163–166. Дои:10.1513 / патс.201007-054МС. ЧВК 3131834. PMID 21543795.
- ^ а б c Чаттерджи, Сангита; Пал, Джаянта К. (1 мая 2009 г.). «Роль 5'- и 3'-нетранслируемых участков мРНК в заболеваниях человека». Биология клетки. 101 (5): 251–262. Дои:10.1042 / BC20080104. PMID 19275763.
- ^ Baou, M .; Norton, J.D .; Мерфи, Дж. Дж. (13 сентября 2011 г.). «AU-богатые РНК-связывающие белки в гемопоэзе и лейкемогенезе». Кровь. 118 (22): 5732–5740. Дои:10.1182 / кровь-2011-07-347237. PMID 21917750.
- ^ Хабар, Халид С.А. (22 мая 2010 г.). «Посттранскрипционный контроль при хроническом воспалении и раке: акцент на элементы, богатые AU». Клеточные и молекулярные науки о жизни. 67 (17): 2937–2955. Дои:10.1007 / s00018-010-0383-х. ЧВК 2921490. PMID 20495997.
- ^ Зуль, Джошуа А. (24 ноября 2015 г.). «Вариант 3'-нетранслируемой области в FMR1 устраняет трансляцию FMRP, зависящую от нейрональной активности, путем нарушения связывания РНК-связывающего белка HuR». Труды Национальной академии наук США. 112 (47): E6553–61. Дои:10.1073 / pnas.1514260112. ЧВК 4664359. PMID 26554012.
дальнейшее чтение
- Мазумдер Б., Сешадри В., Фокс П.Л. (2003). «Управление трансляцией с помощью 3'-UTR: цели определяют средства». Trends Biochem. Наука. 28 (2): 91–8. Дои:10.1016 / S0968-0004 (03) 00002-1. PMID 12575997.
внешняя ссылка
- Краткое введение в регуляторные элементы мРНК
- UTResource Анализ 3 ′ UTR
- UTRome.org 3 'UTR у нематод
- Медицинская тематическая рубрика: 3 ′ Непереведенные области
