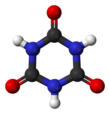
Циануровая кислота - Cyanuric acid
 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 1,3,5-триазинан-2,4,6-трион[1] | |||
| Другие имена 1,3,5-Триазин-2,4,6 (1ЧАС,3ЧАС,5ЧАС) -трион[1] 1,3,5-триазинетриол s-Триазинетриол s-Триазинетрион Трикарбимид Изоциануровая кислота Псевдоциануровая кислота | |||
| Идентификаторы | |||
3D модель (JSmol ) |
| ||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.290 | ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Характеристики | |||
| C3ЧАС3N3О3 | |||
| Молярная масса | 129,07 г / моль | ||
| Внешность | белый кристаллический порошок | ||
| Плотность | 1,75 г / см3 | ||
| Температура плавления | 320–360 ° C (608–680 ° F; 593–633 K) разлагается | ||
| 0,27 г / 100 мл (25 ° C) | |||
| -61.5·10−6 см3/ моль | |||
| Опасности | |||
| Паспорт безопасности | ICSC 1313 | ||
| Родственные соединения | |||
Связанный триазины | Циануровый фторид Цианур хлорид Циануров бромид | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Циануровая кислота или же 1,3,5-триазин-2,4,6-триол это химическое соединение с формула (CNOH)3. Как и многие промышленно полезные химические вещества, этот триазин имеет много синонимов. Это белое твердое вещество без запаха используется в качестве прекурсора или компонента отбеливает, дезинфицирующие средства и гербициды. В 1997 году мировое производство составило 160 миллионов килограммов.[2]
Свойства и синтез
Характеристики
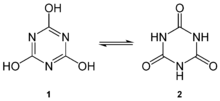
Циануровую кислоту можно рассматривать как циклическую тример неуловимых видов циановая кислота, HOCN. Кольцо может легко превращаться между двумя структуры через кето-енольная таутомерия. Таутомер триола, который может иметь ароматный персонаж,[3] преобладает в растворе. В гидроксил (-OH) группы предполагают фенольный персонаж. Депротонирование основанием дает серию цианурата соли:
- [C (O) NH]3 ⇌ [C (O) NH]2[ПРОТИВ]− + H+ (pKа = 6.88)[4]
- [C (O) NH]2[ПРОТИВ]− ⇌ [C (O) NH] [C (O) N]22− + H+ (pKа = 11.40)
- [C (O) NH] [C (O) N]22− ⇌ [C (O) N]33− + H+ (pKа = 13.5)
Циануровая кислота отличается сильным взаимодействием с меламин, образуя нерастворимые цианурат меламина. Это взаимодействие блокирует циануровую кислоту в три-кетотаутомере.
Синтез
Циануровая кислота (CYA) была впервые синтезирована Фридрих Вёлер в 1829 г. путем термического разложения мочевина и мочевая кислота.[5] Текущий промышленный маршрут к CYA влечет за собой термическое разложение мочевины, с выделением аммиака. Преобразование начинается примерно при 175 ° C:[2]
- 3 ч2N-CO-NH2 → [C (O) NH]3 + 3 NH3
CYA кристаллизуется из воды в виде дигидрата.
Циануровую кислоту можно получить гидролизом сырого или отработанного меламина с последующей кристаллизацией. Кислотные отходы заводов, производящих эти материалы, содержат циануровую кислоту и иногда растворенные аминозамещенные триазины, а именно: Ammeline, аммелид, и меламин. В одном методе сульфат аммония раствор нагревают до «кипения» и обрабатывают стехиометрическим количеством меламина, в результате чего присутствующая циануровая кислота осаждается в виде комплекс меламин-циануровая кислота. Различные потоки отходов, содержащие циануровую кислоту и аминозамещенные триазины, могут быть объединены для утилизации, и в неблагоприятных условиях в потоках отходов может присутствовать нерастворенная циануровая кислота.[6][7]
Промежуточные продукты и примеси
Промежуточные звенья дегидратации включают как изоциановая кислота, биурет, и триурет:
- ЧАС2N-CO-NH2 → HNCO + NH3
- ЧАС2N-CO-NH2 + HNCO → H2N-CO-NH-CO-NH2
- ЧАС2N-CO-NH-CO-NH2 + HNCO → H2N-CO-NH-CO-NH-CO-NH2
Одна примесь в производстве CYA - это аммелид, особенно если температура реакции превышает 190 ° C: 3 H2N-CO-NH-CO-NH2 → [C (O)]2(CNH2) (NH)2N + 2 NH3 + H2O Первое появление аммеламида происходит до 225 ° C и, как предполагается, также происходит при разложении биурета, но образуется медленнее, чем у CYA.
Меламин, [C (NH2) N]3, образование происходит между 325 и 350 ° C и только в очень малых количествах.[8]
Приложения
Циануровая кислота используется в качестве стабилизатора хлора в бассейны. Он связывается со свободным хлором и медленно высвобождает его, увеличивая время, необходимое для истощения каждой дозы дезинфицирующего средства.
В противоопухолевый лекарственного средства тероксирон, образуется в результате реакции циануровой кислоты с 3 эквивалентами эпихлоргидрин.[9]
Прекурсоры хлорированных циануратов
Циануровая кислота в основном используется как предшественник к N-хлорированные цианураты, которые используются для дезинфекции воды. Дихлорпроизводное получают прямым хлорированием:
- [C (O) NH]3 + 2 кл2 + 2 NaOH → [C (O) NCl]2[C (O) NH]
Этот вид обычно превращается в его натриевую соль, дихлор-s-триазинетрион натрия. Дальнейшее хлорирование дает трихлоризоциануровая кислота, [C (O) NCl]3. Эти N-хлорсоединения служат дезинфицирующими средствами и альгицидами для воды в плавательных бассейнах.[2] Он стабилизирует хлор в бассейне и предотвращает быстрое поглощение хлора солнечным светом.
Прекурсоры сшивающих агентов
Благодаря своей трехфункциональности CYA является предшественником сшивающих агентов, особенно для полиуретан смолы и полиизоцианурат термореактивные пластмассы.
Анализ
Проверка концентрации циануровой кислоты обычно проводится с помощью турбидометрического теста, в котором для осаждения циануровой кислоты используется реагент меламин. Относительная мутность прореагировавшего образца определяет концентрацию CYA. Упоминается в 1957 году.[10]Этот тест работает, потому что меламин соединяется с циануровой кислотой в воде, образуя тонкий, нерастворимый, белый осадок (цианурат меламина), который заставляет воду мутнеть пропорционально количеству циануровой кислоты в ней. Совсем недавно был разработан чувствительный метод анализа циануровой кислоты в моче.[11]
Корма для животных
FDA допускает присутствие определенного количества циануровой кислоты в некоторых небелковый азот (NPN) добавки, используемые в кормах для животных и питьевой воде.[12] Циануровая кислота использовалась как NPN. Например, Арчер Дэниэлс Мидленд производит добавку NPN для крупного рогатого скота, которая содержит биурет, триурет, циануровую кислоту и мочевина.[13]
Отзывы о кормах для домашних животных 2007 года
Циануровая кислота участвует в Отзывы о кормах для домашних животных 2007 года, загрязнение и отзыв многих марок кормов для кошек и собак с марта 2007 года. Исследования показали, что циануровая кислота, составляющая мочу, вместе с меламином образует плохо растворимые кристаллы, которые могут вызывать почечная недостаточность (см. раздел Анализ выше).
Безопасность
Циануровая кислота классифицируется как «практически нетоксичная».[2] Средняя летальная доза при пероральном приеме 50% (LD50 ) составляет 7700 мг / кг у крыс.[14]
Однако, когда циануровая кислота присутствует вместе с меламин (которое само по себе является еще одним малотоксичным веществом), оно образует нерастворимый и довольно нефротоксичный сложный,[15] как показано на собаках и кошках во время Загрязнение кормов для домашних животных 2007 г. и у детей во время Китайский молочный скандал в 2008 году случаи.
Естественное явление
Неочищенная медная соль кислоты с формулой Cu (C3N3О3ЧАС2)2(NH3)2, в настоящее время является единственным известным минералом изоцианурат, называемым Иоанневмит. Его нашли в месторождении гуано в Чили. Это очень редко.[16]
Рекомендации
- ^ а б Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга). Кембридж: Королевское химическое общество. 2014. с. 733. Дои:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ а б c d Клаус Хутмахер, Дитер Мост «Циануровая кислота и циануровхлорид» Энциклопедия промышленной химии Ульмана 2005, Wiley-VCH, Weinheim, doi 10.1002 / 14356007.a08 191
- ^ Перес-Манрикес, Лилиана; Кабрера, Армандо; Сансорес, Луис Энрике; Сальседо, Роберто (7 сентября 2010 г.). «Ароматичность циануровой кислоты». Журнал молекулярного моделирования. 17 (6): 1311–1315. Дои:10.1007 / s00894-010-0825-2. ЧВК 3102184. PMID 20820829.

- ^ "Константы диссоциации органических кислот и оснований" Справочник CRC по химии и физике, Интернет-версия 2005 г. (85-е изд.)
- ^ Вёлер, Ф. (1829) "Ueber die Zersetzung des Harnstoffs und der Harnsäure durch höhere Temperatur", (О разложении мочевины и мочевой кислоты при более высокой температуре), Annalen der Physik und Chemie, 2-я серия, 15 : 619-630.
- ^ «Процесс получения чистой циануровой кислоты». 14 июля 1981 г.. Получено 2007-12-10.
- ^ «Процесс термического гидролиза под высоким давлением для разложения триазинов в кислых отходах». 22 марта 1977 г.. Получено 2007-12-10.
- ^ Шабер, Питер М. и др. «Изучение реакции термического разложения мочевины (пиролиза) и важность для производства циануровой кислоты», Американская лаборатория, август 1999: 13-21. «Архивная копия» (PDF). Архивировано из оригинал (PDF) на 2007-09-28. Получено 2007-05-08.CS1 maint: заархивированная копия как заголовок (связь)
- ^ М. Будновски, Angew. Chem., 7, 827 (1968).
- ^ «Тест на мутность Merck». Merck. 6 июня 2003 г. Архивировано с оригинал 1 июля 2007 г.. Получено 2007-05-06. (мертвая ссылка 8 апреля 2018 г.)
- ^ Панувет П., Уэйд Е.Л., Нгуен СП, Монтесано Массачусетс, Нидхэм Л.Л., Барр Д.Б. Количественное определение остатка циануровой кислоты в моче человека с использованием тандемной масс-спектрометрии с высокоэффективной жидкостной хроматографией. J Chromatogr B Analyt Technol Biomed Life Sci 2010 878 (28): 2916-2922.
- ^ «21ЦФР573.220 Биурет кормовой». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 1 апреля 2006 г.. Получено 2007-05-06.
- ^ «Roughage Buster Plus: ингредиенты». Арчер Дэниэлс Мидленд. Архивировано из оригинал на 2007-02-12. Получено 2007-05-06.
- ^ Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США, «Промежуточная оценка безопасности / риска меламина и аналогов; доступность», В архиве 16 декабря 2007 г. Wayback Machine Федеральный регистр: 30 мая 2007 г. (том 72, номер 103). Проверено 27 сентября 2008 г.
- ^ «Взаимодействие меламина и циануровой кислоты может сыграть определенную роль в болезни и смерти от припоминания корма для домашних животных» В архиве 18 мая 2007 г. Wayback Machine, Американская ветеринарная медицинская ассоциация (AVMA), пресс-релиз, 1 мая 2007 г. Проверено 27 сентября 2008 г.
- ^ Миндат, http://www.mindat.org/min-42755.html
внешняя ссылка
- Международная карта химической безопасности 1313
- Страница загрязнения кормов для домашних животных Орегонской ветеринарной медицинской ассоциации (OVMA) - Новости и события обновляются регулярно