Тетразол - Tetrazole
| |||
| Идентификаторы | |||
|---|---|---|---|
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.477 | ||
PubChem CID | |||
| |||
| |||
| Характеристики | |||
| CH2N4 | |||
| Молярная масса | 70,05 г / моль | ||
| Плотность | 1,477 г / мл | ||
| Температура плавления | От 157 до 158 ° C (от 315 до 316 ° F; от 430 до 431 K)[2] | ||
| Точка кипения | 220 ± 23 ° С (428 ± 41 ° F, 493 ± 23 К) | ||
| Кислотность (пKа) | 4.90 [1] | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Тетразолы являются классом синтетический органический гетероциклическое соединение, состоящий из 5-членного кольца из четырех азот атомы и один углерод атом. Название тетразол также относится к исходному соединению с формулой CH2N4, из которых можно составить три изомера.
Структура и склеивание
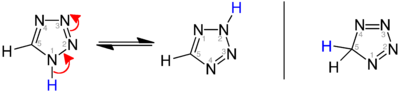
Существуют три изомера исходного тетразола, различающиеся положением двойных связей: 1ЧАС-, 2ЧАС-, и 5ЧАС-тетразол. 1ЧАС- и 2ЧАС- изомеры таутомеры, причем равновесие лежит на стороне 1ЧАС-тетразол в твердой фазе.[3][4][5] В газовой фазе 2ЧАС-тетразол доминирует.[4][6][7] Эти изомеры можно рассматривать как ароматный, с 6 π-электронами, а 5ЧАС-изомер неароматический.
Синтез
1ЧАС-Тетразол впервые был получен по реакции безводного гидразойная кислота и цианистый водород под давлением. Обработка органических нитрилы с азид натрия в присутствии йод или на кремнеземной основе бисульфат натрия как разнородный катализатор дает возможность выгодного синтеза 5-замещенного 1ЧАС-тетразолы. Другой метод - дезаминирование 5-аминотетразол, которые могут быть коммерчески получены или получены в свою очередь из аминогуанидин.[8][9]
2-арил-2H-тетразолы синтезируются [3 + 2] циклоприсоединение реакция между арилом диазоний и триметилсилилдиазометан.[10]
Использует
Есть несколько фармацевтических агентов, которые представляют собой тетразолы. Тетразолы могут действовать как биоизостеры за карбоксилатные группы потому что они имеют одинаковую pKa и депротонируются при физиологическом pH. Ангиотензин Блокаторы рецепторов II - такие как лозартан и кандесартан, часто представляют собой тетразолы. Хорошо известным тетразолом является бромид диметилтиазолилдифенилтетразолия (МТТ). Этот тетразол используется в МТТ анализ количественно оценить дыхательная активность живых клеток культура, хотя обычно убивает клетки в процессе. Некоторые тетразолы также можно использовать в анализах ДНК.[11] Исследования показывают, что VT-1161 и VT-1129 являются потенциальными мощными противогрибковыми препаратами, поскольку они нарушают ферментативную функцию грибов, но не ферменты человека.[12][13]
Некоторый тетразол производные с высокой энергией были исследованы как высокая производительность взрывчатка в качестве замены TNT а также для использования в высокой производительности твердое ракетное топливо составы.[14][15] К ним относятся азидотетразолат соли азотистых оснований.
Другие тетразолы используются из-за их взрывоопасных или горючих свойств, таких как сам тетразол и 5-аминотетразол, которые иногда используются как компонент газовые генераторы в автомобиль подушки безопасности. Энергетические материалы на основе тетразола производят высокотемпературные, нетоксичные продукты реакции, такие как вода и газообразный азот,[16] и имеют высокую скорость горения и относительную стабильность,[17] все это желательные свойства. Энергия делокализации в тетразоле составляет 209 кДж / моль.
1ЧАС-Тетразол и 5- (бензилтио) -1ЧАС-тетразол (БТТ) широко используются в качестве кислотных активаторов реакции сочетания в синтез олигонуклеотидов.[18]
Родственные гетероциклы
- Триазолы, аналоги с тремя атомами азота
- Пентазол, аналог с пятью атомами азота (строго говоря, неорганический гомоцикл, а не гетероцикл)
- Оксатетразол
- Тиатетразол
Рекомендации
- ^ Сатчелл, Жаклин Ф .; Смит, Брайан Дж. (2002). «Расчет водных констант диссоциации 1,2,4-триазола и тетразола: сравнение моделей сольватации». Phys. Chem. Chem. Phys. 4 (18): 4314–4318. Bibcode:2002PCCP .... 4.4314S. Дои:10.1039 / b203118c.
- ^ Михина, Джозеф С .; Хербст, Роберт М. (1950). «Реакция нитрилов с гидразойной кислотой: синтез монозамещенных тетразолов». J. Org. Chem. 15 (5): 1082–1092. Дои:10.1021 / jo01151a027.
- ^ Goddard, R .; Heinemann, O .; Крюгер, К. (1997-05-15). «α-1H-1,2,3,4-Тетразол». Acta Crystallographica Раздел C. 53 (5): 590–592. Дои:10.1107 / S0108270197000772. ISSN 0108-2701.
- ^ а б Киселев, Виталий Г .; Чеблаков, Павел Б .; Грицан, Нина П. (10.03.2011). «Таутомерия и термическое разложение тетразола: высокоуровневое исследование ab Initio». Журнал физической химии A. 115 (9): 1743–1753. Дои:10.1021 / jp112374t. ISSN 1089-5639.
- ^ Разынская, А .; Tempczyk, A .; Малински, Э .; Szafranek, J .; Грзонка, З .; Германн, П .: в J. Chem. Soc. Perkin Trans. 2 1983, 379.
- ^ Вонг, Мин Ва; Леунг-Тоунг, Регис; Вентруп, Курт (1993-03-01). «Таутомерное равновесие и водородные сдвиги тетразола в газовой фазе и в растворе». Журнал Американского химического общества. 115 (6): 2465–2472. Дои:10.1021 / ja00059a048. ISSN 0002-7863.
- ^ Ражиньская, Анна; Темпчик, Анна; Малински, Эдмунд; Шафранек, Януш; Грзонка, Збигнев; Германн, Питер (1983-01-01). «Применение масс-спектрометрии для изучения прототропных равновесий в 5-замещенных тетразолах в газовой фазе; экспериментальные данные и теоретические соображения». Журнал химического общества, Perkin Transactions 2 (3): 379–383. Дои:10.1039 / P29830000379. ISSN 1364-5471.
- ^ Генри, Рональд А .; Финнеган, Уильям Г. (1954-01-01). «Улучшенная процедура дезаминирования 5-аминотетразола». Журнал Американского химического общества. 76 (1): 290–291. Дои:10.1021 / ja01630a086. ISSN 0002-7863.
- ^ Курцер, Ф .; Годфри, Л. Э. А. (1963). «Синтезы гетероциклических соединений из аминогуанидина». Angewandte Chemie International Edition на английском языке. 2 (8): 459–476. Дои:10.1002 / anie.196304591. ISSN 1521-3773.
- ^ Патуре, Реми; Каменецкая, Теодор М. (06.04.2016). «Синтез 2-арил-2H-тетразолов посредством реакции региоселективного [3 + 2] циклоприсоединения». Буквы Тетраэдра. 57 (14): 1597–1599. Дои:10.1016 / j.tetlet.2016.02.102. ЧВК 4810784. PMID 27041776.
- ^ С. Бернер; К. Мюлеггер и Х. Селигер (11 февраля 1989 г.). «Исследования роли тетразола в активации фосфорамидитов». Нуклеиновые кислоты Res. 17 (3): 853–864. Дои:10.1093 / nar / 17.3.853. ЧВК 331708. PMID 2922273.
- ^ Warrilow, A.G.S .; Халл, К.М.; Паркер, Дж. Э .; Гарви, Э. П .; Hoekstra, W. J .; Мур, W. R .; Schotzinger, R.J .; Келли, Д. Э .; Келли, С. Л. (декабрь 2014 г.). «Клинический кандидат VT-1161 является сильнодействующим ингибитором Candida albicans CYP51, но не может связывать фермент человека». Противомикробные препараты и химиотерапия. 58 (12): 7121–7127. Дои:10.1128 / AAC.03707-14. ЧВК 4249504. PMID 25224009.
- ^ Локхарт, Шон Р .; Фотергилл, Аннетт В .; Икбал, Наурин; Болден, Кэрол Б.; Гроссман, Нина Т .; Гарви, Эдвард П .; Бренд, Стивен Р .; Hoekstra, Уильям Дж .; Schotzinger, Роберт Дж .; Оттингер, Элизабет; Паттерсон, Томас Ф .; Видерхольд, Натан П. (апрель 2016 г.). «Исследуемый грибковый ингибитор Cyp51 VT-1129 демонстрирует сильную активность против Cryptococcus neoformans и Cryptococcus gattii». Противомикробные препараты и химиотерапия. 60 (4): 2528–2531. Дои:10.1128 / AAC.02770-15. ЧВК 4808209. PMID 26787697.
- ^ «Более экологичные взрывчатые вещества многообещающи». Мир химии. 2 октября 2008 г.
- ^ Нико Фишер, Константин Карагиосов, Томас М. Клапётке и Йорг Штирсторфер (апрель 2010 г.). «Новые энергетические материалы, содержащие тетразолы и нитрамины - синтез, характеристика и свойства». Zeitschrift für Anorganische und Allgemeine Chemie. 636 (5): 735–749. Дои:10.1002 / zaac.200900521.CS1 maint: несколько имен: список авторов (связь)
- ^ Торе Бринк, Томас М. Клапётке и Йорг Штирсторфер (2014). «Энергетические N-оксиды тетразола». Энергетические N-оксиды тетразола. Зеленые энергетические материалы. С. 133–178. Дои:10.1002 / 9781118676448.ch06. ISBN 9781118676448.
- ^ Николас Пикиел и Майкл Р. Захария (2012). «Разложение энергетических материалов на основе аминотетразола в условиях высокой скорости нагрева». J. Phys. Chem. А. 116 (6): 1519–1526. Bibcode:2012JPCA..116.1519P. Дои:10.1021 / jp203957t. PMID 22214278.
- ^ Ся Вэй (6 мая 2013 г.). «Активаторы связывания для синтеза олигонуклеотидов через фосфорамидитный подход». Тетраэдр. 69 (18): 3615–3637. Дои:10.1016 / j.tet.2013.03.001.