Псевдоуридин - Pseudouridine
 | |
| Имена | |
|---|---|
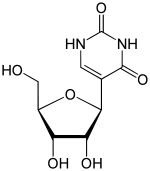
| Название ИЮПАК 5-[(2S,3р,4S,5р) -3,4-дигидрокси-5- (гидроксиметил) оксолан-2-ил] -1ЧАС-пиримидин-2,4-дион | |
| Предпочтительное название IUPAC 5- (β-D-рибофуранозил) пиримидин-2,4 (1ЧАС,3ЧАС) -диона | |
| Другие имена пси-уридин, 5-рибосилурацил, бета-D-псевдоуридин, 5- (бета-D-рибофуранозил) урацил | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C9ЧАС12N2О6 | |
| Молярная масса | 244,20 г / моль |
| Внешность | Белый гранулированный порошок |
| Хорошо растворим в воде. | |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Псевдоуридин (сокращенно греческой буквой psi- или буквой Q)[1] является изомер из нуклеозид уридин в которой урацил присоединяется через углерод-углерод вместо азот-углерод гликозидная связь. (В этой конфигурации урацил иногда называют «псевдурацилом».) Псевдоуридин является наиболее распространенным Модификация РНК в сотовой РНК. После транскрипция и после синтеза РНК может быть модифицирована более чем 100 химически различными модификациями. Они потенциально могут регулировать экспрессию РНК посттранскрипционно, в дополнение к четырем стандартным нуклеотидам, и играют различные роли в клетке, включая трансляцию, локализацию и стабилизацию РНК. Псевдоуридин, будучи одним из них, представляет собой C5-гликозидный изомер уридина, который содержит связь C-C между C1 рибоза сахар и C5 из урацил, а не обычная связь C1-N1, обнаруженная в уридине. Связь C-C дает ему большую свободу вращения и конформационную гибкость.[2] Кроме того, псевдоуридин имеет дополнительный донор водородной связи в положении N1. Псевдоуридин, также известный как 5-рибосилурацил, является повсеместным, но загадочным компонентом структурных РНК (переносных, рибосомных, малых ядер (мяРНК) и малых ядрышек). Недавно это также было обнаружено в кодирующей РНК. Будучи самым многочисленным, он обнаружен во всех трех филогенетических областях жизни и был обнаружен первым. Этот нуклеотид считается «пятым нуклеотидом». На его долю приходится 4% нуклеотидов в дрожжи тРНК. Эта модификация основания способна стабилизировать РНК и улучшить укладку оснований за счет образования дополнительных водородных связей с водой через ее дополнительную иминогруппу. В группе 11 псевдоуридинов. кишечная палочка рРНК, 30 в цитоплазматической рРНК дрожжей и единственная модификация в митохондриальной 21S рРНК и около 100 псевдоуридинов в человеческой рРНК, что указывает на то, что степень псевдоуридилирования увеличивается со сложностью организма. Псевдоуридин в рРНК и тРНК, как было показано, тонко настраивают и стабилизируют региональную структуру и помогают поддерживать свои функции в декодировании мРНК, сборке, обработке и трансляции рибосом.[2][3][4] Псевдоуридин в мяРНК было показано, что усиливает сплайсосомный Взаимодействие РНК-пре-мРНК для облегчения регуляции сплайсинга.[5]
Эффекты и модификации на различных РНК
тРНК

Псевдоуридин = Ψ
Ψ повсеместно встречается в этом классе РНК и способствует распространению тРНК структурные мотивы. Одним из таких структурных мотивов является петля ствола TΨC, которая включает Ψ55. Ψ обычно находится в стебле D, стебле и петле антикодона тРНК из каждого домена. В каждом структурном мотиве уникальные физико-химические свойства Ψ стабилизируют структуры, которые были бы невозможны со стандартным U.[2]
Во время трансляции Ψ модулирует взаимодействия молекул тРНК с рРНК и мРНК. Ψ и другие модифицированные нуклеотиды влияют на локальную структуру доменов тРНК, в которых они находятся, не влияя на общую складку РНК. В «стебле-петле» антикодона (ASL) Ψ кажется критическим для правильного связывания тРНК с рибосомой. Ψ стабилизирует динамическую структуру ASL и способствует более сильному связыванию с 30S рибосомой. Стабилизированная форма ASL помогает поддерживать правильный антикодон -кодон пары во время перевода. Эта стабильность может повысить точность трансляции за счет снижения скорости образования пептидной связи и предоставления большего времени для отклонения неправильных пар кодон-антикодон. Несмотря на роль в стабилизации локальной структуры, псевдоуридилирование тРНК не является существенным для жизнеспособности клеток и обычно не требуется для аминоацилирование.[2]
мРНК
Ψ также встречается в мРНК которые являются матрицей для синтеза белка. Ψ остатки в мРНК могут влиять на специфичность кодирования стоп-кодонов UAA, UGA и UAG. В этих стоп-кодонах модификация U → Ψ и мутация U → C способствуют бессмысленному подавлению.[6]
рРНК
Ψ встречается в больших и малых рибосомальный субъединицы всех сфер жизни и их органеллы. В рибосоме Ψ остатки группируются в доменах II, IV и V и стабилизируют взаимодействия РНК-РНК и / или РНК-белок. Стабильность, обеспечиваемая Ψ, может помочь рРНК сворачивание и сборка рибосом. Ψ также может влиять на стабильность локальных структур, что влияет на скорость и точность декодирования и корректуры во время перевода.[2]
мяРНК
Ψ встречается в основных сплайсосомный мяРНК эукариот. Ψ остатки мяРНК часто филогенетически консервативны, но имеют некоторые вариации в зависимости от таксонов и организмов. Остатки в мяРНК обычно расположены в областях, которые участвуют во взаимодействиях РНК-РНК и / или РНК-белок, участвующих в сборке и функции сплайсосомы. Ψ остатки в мяРНК способствуют правильной укладке и сборке сплайсосомы, что важно для процессинга пре-мРНК.[2]
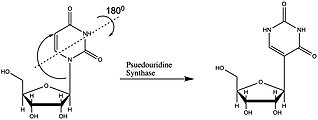
Белки псевдоуридинсинтазы
Псевдоуридин - это модификации РНК, которые производятся посттранскрипция, поэтому после образования РНК. Белки, которые производят эту модификацию, называются псевдоуридинсинтазами или PUS. Белки PUS встречаются во всех сферах жизни. Большинство исследований было проведено в отношении того, как белок PUS модифицирует тРНК, поэтому механизм с участием мяРНК и мРНК четко не определен. Белки PUS могут различаться по специфичности РНК, структуре и изомеризация механизмы. Различные структуры PUS делятся на 4 семейства. Семейства разделяют активную последовательность и важные структурные мотивы.[1]
TruA
Домен TruA модифицирует множество различных участков тРНК, мяРНК и мРНК. В этом семействе до сих пор обсуждают механизм изомеризации уридина.[4][7]

PUS 1 расположен в ядре и модифицирует тРНК в разных местах: U44 мяРНК U2 и U28 мяРНК U6. Исследования показали, что экспрессия PUS 1 увеличивается во время стресса окружающей среды и важна для регуляции сплайсинга РНК. Кроме того, PUS 1 необходим для взятия тРНК, образующейся в ядре, и отправки их в цитоплазму.[4]
PUS 2 очень похож на PUS 1, но расположен в митохондриях и модифицирует только U27 и U28 мито-тРНК. Этот белок модифицирует митохондриальную тРНК, которая имеет меньшее количество модификаций псевдоуридина по сравнению с другими тРНК. В отличие от большинства белков, локализованных в митохондриях, PUS 2 не имеет сигнала нацеливания на митохондрии или MTS.[4]
PUS 3 является гомологом PUS 1, но модифицирует разные места тРНК (U38 / 39) в цитоплазме и митохондриях. Этот белок является наиболее консервативным из семейства TruA. Уменьшение модификаций, производимых PUS 3, было обнаружено, когда структура тРНК неправильно свернута. Наряду с тРНК, белок нацелен на нкРНК и мРНК, все еще необходимы дальнейшие исследования в отношении важности этой модификации. PUS 3 вместе с PUS 1 модифицируют рецептор стероидного активатора у человека.[4]
TruB
Семейство TruB содержит только PUS 4, расположенный в митохондриях и ядрах. Модификация PUS 4 сильно консервативна и расположена в U55 в локте тРНК. В человеческой форме PUS 4 фактически отсутствует связывающий домен, называемый PUA или псевдоуридинсинтаза, и археозин транс-гликозилаза. PUS 4 имеет специфичность последовательности для части Т-петли тРНК. Предварительные данные о модификации мРНК PUS4, но для подтверждения необходимы дополнительные исследования. Также связывается со специфическим вирусом мозаики брома, который представляет собой РНК-вирус, поражающий растения.[4][8]
TruD
TruD способен модифицировать множество РНК, и неясно, как эти различные субстраты РНК распознаются. PUS 7 модифицирует U2 snRNA в положении 35, и эта модификация будет усиливаться, когда клетки находятся в сильном шоке. Другая модификация - цитоплазматическая тРНК в положении 13 и положении 35 в пре-тРНК.Тюр. PUS 7 модифицирует почти специфичность, не зависит от типа РНК, поскольку мРНК показывает псевдоуридилированную PUS 7. Распознайте это как последовательность РНК, UGUAR со вторым U, являющимся нуклеотидом, который будет модифицирован. Псевдоуридилирование мРНК PUS 7 увеличивается во время теплового шока, поскольку белок перемещается из ядра в цитоплазму. Считается, что эта модификация увеличивает стабильность мРНК во время теплового шока до того, как РНК попадет в ядро или митохондрии, но необходимы дополнительные исследования.[4][7]
RluA
Домен RluA этих белков может идентифицировать субстрат через связывание другого белка с субстратом, а затем особые связи с доменом RluA.[1][7]
PUS 5 недостаточно изучена и расположена псевдоуридинсинтаза и, как и Pus 2, не имеет последовательности, направленной на митохондриальный сигнал. Белок модифицирует U2819 митохондриальной 21S рРНК. Также подозревается, что Pus 5 модифицирует некоторые уридины в мРНК, но снова необходимы дополнительные данные для подтверждения.
PUS 6 есть один, который изменяет только U31 цитоплазматической и митохондриальной тРНК. Также известно, что гной 6 модифицирует мРНК.[4]
PUS 8 также известный как Rib2 модифицирует цитоплазматическую тРНК в положении U32. На С-конце находится DRAP-дезаминазный домен, связанный с биосинтезом рибофлавина. RluA и DRAP или домен дезаминазы, относящийся к рибофлавинсинтаза выполняют полностью отдельные функции в белке, и неизвестно, взаимодействуют ли они друг с другом. PUS 8 необходим дрожжам, но предполагается, что он связан с синтезом рибофлавина, а не с модификацией псевдоуридина.[4]
PUS 9 и PUS 8 катализируют то же положение в митохондриальной тРНК вместо цитоплазматической. Это единственный белок PUS, который содержит митохондриальный сигнальный домен нацеливания на N-конце. Исследования предполагают, что PUS 9 может изменять мРНК, что означает меньшую субстратную специфичность.[4]
Методы секвенирования генома псевдоуридина
Псевдоуридин можно идентифицировать множеством различных методов. Распространенным методом выявления модификаций РНК и ДНК является жидкостная хроматография с масс-спектрометрией или ЖХ-МС. Масс-спектрометрии разделяет молекулы по массе и заряду, при этом уридин и псевдроуидин имеют одинаковую массу, но разные заряды. Жидкостная хроматография работает по времени удерживания, которое связано с выходом из колонки.[9] В химическом способе идентификации псевдоуридина используется соединение под названием CMC или N-циклогексил-N'-β- (4-метилморфолиниум) этилкарбодиимид, которое специфически маркирует и отличает уридин от псевдоуридина. КМЦ связывается с псевдоуридином и уридином, но крепче удерживается с псевдурдином из-за третьего азота, способного образовывать водородную связь. КМЦ, связанную с псевдоуридином, затем можно визуализировать, пометив сигнальную молекулу. Этот метод все еще разрабатывается, чтобы обеспечить высокую пропускную способность.[10]
Медицинское значение псевдоуридина
Псевдоуридин оказывает тонкое, но значительное влияние на соседний сахарно-фосфатный остов, а также усиливает укладку оснований. Эти эффекты могут лежать в основе биологической роли большинства, но, возможно, не всех остатков псевдоуридина в РНК. Некоторые генетические мутанты, лишенные специфических остатков псевдоуридина в тРНК или рРНК, проявляют трудности с трансляцией, демонстрируют медленные темпы роста и неспособны эффективно конкурировать со штаммами дикого типа в смешанной культуре. Модификации псевдоуридина также участвуют в заболеваниях человека, таких как митохондриальная миопатия и сидеробластная анемия (MLASA) и врожденный дискератоз.[4] Врожденный дискератоз и Hoyeraal-Hreidarsson два редких наследственных синдрома, вызванных мутациями в DKC1, ген, кодирующий дискерин псевдоуридинсинтазы. Псевдоуридины были признаны регуляторами латентных вирусных процессов у вируса иммунодефицита человека (ВИЧ ) инфекции.[11] Псевдоуридилирование также связано с патогенезом наследуемого по материнской линии диабета и глухоты (MIDD). В частности, точечная мутация в митохондриальной тРНК, по-видимому, предотвращает псевдоуридилирование одного нуклеотида, тем самым изменяя третичную структуру тРНК. Это может привести к более высокой нестабильности тРНК, вызывая дефицит митохондриальной трансляции и дыхания.[11]
Смотрите также
Рекомендации
- ^ а б c Хамма, Томоко; Ферре-Д'Амаре, Адриан Р. (ноябрь 2006 г.). «Псевдоуридинсинтазы». Химия и биология. 13 (11): 1125–1135. Дои:10.1016 / j.chembiol.2006.09.009. ISSN 1074-5521. PMID 17113994.
- ^ а б c d е ж Грей, Майкл Шаретт, Майкл У. (01.05.2000). «Псевдоуридин в РНК: что, где, как и почему». IUBMB Life. 49 (5): 341–351. Дои:10.1080/152165400410182. ISSN 1521-6543. PMID 10902565.
- ^ Ге, Цзюньху; Ю, И-Тао (апрель 2013 г.). «Псевдоуридилирование РНК: новый взгляд на старую модификацию». Тенденции в биохимических науках. 38 (4): 210–218. Дои:10.1016 / j.tibs.2013.01.002. ISSN 0968-0004. ЧВК 3608706. PMID 23391857.
- ^ а б c d е ж грамм час я j k Ринтала-Демпси, Энн С.; Коте, Юте (03.01.2017). "Автономные эукариотические псевдоуридинсинтазы - ферменты, модифицирующие РНК, и новые регуляторы экспрессии генов?". РНК Биология. 14 (9): 1185–1196. Дои:10.1080/15476286.2016.1276150. ISSN 1547-6286. ЧВК 5699540. PMID 28045575.
- ^ Ву, Гуовэй; Радван, Мохамед К .; Сяо, Му; Адачи, Хиронори; Вентилятор, Джейсон; Ю, И-Тао (2016-06-07). «Путь TheTORsignaling регулирует вызванное голоданием псевдоуридилирование дрожжевой U2 snRNA». РНК. 22 (8): 1146–1152. Дои:10.1261 / rna.056796.116. ISSN 1355-8382. ЧВК 4931107. PMID 27268497.
- ^ Адачи, Хиронори; De Zoysa, Meemanage D .; Ю, И-Тао (март 2019). «Посттранскрипционное псевдоуридилирование в мРНК, а также в некоторых основных типах некодирующих РНК». Biochimica et Biophysica Acta (BBA) - механизмы регуляции генов. 1862 (3): 230–239. Дои:10.1016 / j.bbagrm.2018.11.002. ISSN 1874-9399. ЧВК 6401265. PMID 30414851.
- ^ а б c Penzo, M .; Guerrieri, A.N .; Zacchini, F .; Treré, D .; Монтанаро, Л. (2017-11-01). «Псевдоуридилирование РНК в физиологии и медицине: к лучшему и к худшему». Гены. 8 (11): 301. Дои:10.3390 / гены8110301. ISSN 2073-4425. ЧВК 5704214. PMID 29104216.
- ^ Кеффер-Уилкс, Лаура Кэрол; Вирареддигари, Говардхан Редди; Коте, Юте (14 ноября 2016 г.). «Фермент модификации РНК TruB является шапероном тРНК». Труды Национальной академии наук. 113 (50): 14306–14311. Дои:10.1073 / pnas.1607512113. ISSN 0027-8424. ЧВК 5167154. PMID 27849601.
- ^ Xu, J .; Gu, A. Y .; Thumati, N.R .; Вонг JMY (2017-09-05). «Количественная оценка уровней псевдоуридина в пулах клеточной РНК с помощью модифицированного анализа HPLC-UV». Гены. 8 (9): 219. Дои:10.3390 / genes8090219. ISSN 2073-4425. ЧВК 5615352. PMID 28872587.
- ^ Калсотра, Ауинаш (02.11.2016). «Оценка факультета 1000 для картирования транскриптомов показывает широко распространенное динамически регулируемое псевдоуридилирование нкРНК и мРНК». Дои:10.3410 / ф.718875945.793524920. Цитировать журнал требует
| журнал =(помощь) - ^ а б Чжао, Ян; Кариджолич, Джон; Glaunsinger, Britt; Чжоу, Цян (октябрь 2016 г.). «Псевдоуридилирование 7 SK sn РНК способствует образованию 7 SK sn RNP для подавления транскрипции ВИЧ-1 и выхода из латентного периода». Отчеты EMBO. 17 (10): 1441–1451. Дои:10.15252 / набр.201642682. ISSN 1469-221X. ЧВК 5048380. PMID 27558685.
