Правило Кашаса - Kashas rule
Правило Каши это принцип в фотохимия из электронно возбужденный молекулы. Правило гласит, что испускание фотона (флуоресценция или же фосфоресценция ) происходит с заметным выходом только из низшего возбужденного состояния данного множественность. Назван в честь американского спектроскописта. Майкл Каша, который предложил его в 1950 году.[1][2]
Описание и объяснение
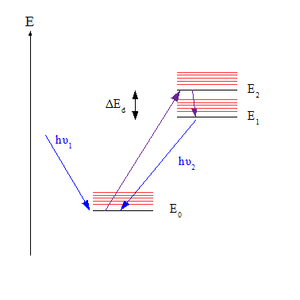
Правило важно для понимания спектр излучения возбужденной молекулы. После поглощения фотона молекула в своем электронном основное состояние (обозначено S0, предполагая синглетное состояние ) может - в зависимости от фотона длина волны - быть возбужденным до любого из набора высших электронных состояний (обозначенных Sп куда п> 0). Однако по правилу Каши, фотонное излучение (называется флуоресценцией в случае S состояние) ожидается с заметным выходом только из низшего возбужденного состояния, S1. Поскольку ожидается, что только одно состояние дает излучение, эквивалентное утверждение правила состоит в том, что длина волны излучения не зависит от длины волны возбуждения.[3]
Правило можно объяснить тем, что Факторы Франка – Кондона за вибронные переходы. Для данной пары уровней энергии, различающихся как колебательными, так и электронными квантовое число фактор Франка – Кондона выражает степень перекрытия их колебательных волновые функции. Чем больше перекрытие, тем быстрее молекула может перейти с более высокого уровня на более низкий. Перекрытие между парами наиболее велико, когда два вибрационных уровня близки по энергии; это имеет место, когда бесшумный уровней электронных состояний, связанных переходом (где колебательное квантовое число v равен нулю) близки. В большинстве молекул безколебательные уровни возбужденных состояний все расположены близко друг к другу, поэтому молекулы в верхних состояниях быстро достигают нижнего возбужденного состояния, S1, прежде чем они успеют флуоресцировать. Однако энергетический разрыв между S1 и S0 больше, поэтому здесь возникает флуоресценция, поскольку теперь она кинетически конкурирует с внутренняя конверсия (IC).[4][5]
Исключения из правила Каша возникают, когда между возбужденными состояниями существуют большие энергетические промежутки. Примером является азулен: классическое объяснение состоит в том, что S1 и S2 состояния расположены достаточно далеко друг от друга, поэтому флуоресценция наблюдается в основном от S2.[4][5] Однако недавние исследования показали, что это может быть не так, и что флуоресценция наблюдается от S2 из-за перехода в N-мерная потенциальная поверхность, обеспечивающая очень быстрое внутреннее преобразование из S1 к S0.[нужна цитата ]
Правило Вавилова
Следствием правила Каши является Вавилов правило, в котором говорится, что квантовый выход люминесценции обычно не зависит от длины волны возбуждения.[4][6] Это можно понять как следствие тенденции - подразумеваемой правилом Каша - для молекул в верхних состояниях безызлучательно релаксировать в нижнее возбужденное состояние. Опять же есть исключения: например бензол пар.[4]
Смотрите также
- Стоксов сдвиг, разность частот поглощения и излучения, связанная с правилом Каша.[7]
Рекомендации
- ^ Характеристика электронных переходов в сложных молекулах.. Каша, М. Обсуждения общества Фарадея, 1950, 9: с.14-19.
- ^ ИЮПАК. Правило Каши - Сборник химической терминологии, 2-е изд. («Золотая книга»). Составлено McNaught, A.D. и Wilkinson, A. Blackwell Scientific Publications, Oxford, 1997.
- ^ «Необычная аутофлуоресценция, характерная для культивированных клеток красного дождя». Луис Дж. И Кумар А.С. Представлено в SPIE Конференция 7097, август 2008 г.
- ^ а б c d Фотохимия органических соединений: от концепции к практике. Клан, П. и Вирц, Дж. Вили-Блэквелл, 2009. с.40. ISBN 1-4051-6173-6.
- ^ а б Химия и свет. Суппан, П. Королевское химическое общество, 1994. стр.56. ISBN 0-85186-814-2.
- ^ ИЮПАК. Правило Каша – Вавилова - Сборник химической терминологии, 2-е изд. («Золотая книга»). Составлено McNaught, A.D. и Wilkinson, A. Blackwell Scientific Publications, Oxford, 1997.
- ^ Координационная химия Gispert, J.R. Wiley-VCH, 2008. стр. 483. ISBN 3-527-31802-X.






