Дитиол - Dithiol
А дитиол это тип сероорганическое соединение с двумя тиол функциональные группы. Их свойства в целом аналогичны свойствам монотиолов с точки зрения растворимости, запаха и летучести. Их можно классифицировать по относительному расположению двух тиоловых групп на органическом скелете.
- Структура некоторых дитиолов
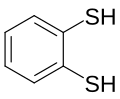
1,2-Benzenedithiol, исходный ароматический дитиол

Препарат мезо-2,3-димеркаптоянтарная кислота

Димеркапрол («Британский антилевизит»), ранний антидот от отравления мышьяком.
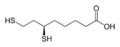
Дигидролипоевая кислота, витамин
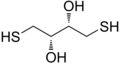
Дитиотреитол, реагент в биохимии белков
Геминальные дитиолы
Геминальные дитиолы имеют формулу RR'C (SH)2. Они получены из альдегидов и кетонов под действием сероводород. Их стабильность контрастирует с редкостью геминальных диолов. Примеры включают метанедитиол, 1,1-этандитиол и 1,1-циклогександитиол. При нагревании гем-дитиолы часто выделяют сероводород, что приводит к переходному процессу. тиокетон или тиал, которые обычно конвертируются в олигомеры.[1]
1,2-дитиолы
Соединения, содержащие тиольные группы на соседних углеродных центрах, являются обычными. 1,2-этандитиол реагирует с альдегидами и кетонами с образованием 1,3-дитиоланов:
- (HS)2C2ЧАС4 + RCHO → RCHS2C2ЧАС4 + H2О
Некоторые дитиолы используются в хелатотерапия, то есть удаление ядов тяжелых металлов.[2] Примеры включают димеркаптопропансульфат (DMPS), димеркапрол («БАЛ») и мезо-2,3-димеркаптоянтарная кислота.
Энедитиолы
Энедитиолы, за исключением ароматических примеров, встречаются редко. Родительский ароматический пример: бензоледитиол. Дитиол 1,3-дитиол-2-тион-4,5-дитиолат2- также известно.
1,3-дитиолы
1,3-пропанедитиол является родительским элементом этой серии. Он используется как реагент в органической химии, так как образует 1,3-дитиан при лечении кетонами и альдегиды. Будучи производной альдегидов, метиленовая C-H группа является достаточно кислой, чтобы ее можно было депротонировать, а образующийся анион можно было C-алкилировать. Процесс является основой умполунг явление.[3]
Подобно 1,2-этандитиолу, пропандитиол образует комплексы с металлами:
Встречающийся в природе 1,3-дитиол - это дигидролипоевая кислота.
1,3-дитиолы окисляются с образованием 1,2-дитиоланы.
1,4-дитиолы
Обычный 1,4-дитиол - это дитиотреитол (ДТТ), ХСЧ2СН (ОН) СН (ОН) СН2SH, иногда называют Cleland реагент для уменьшить белок дисульфидные связи. Окисление DTT приводит к стабильной шестичленной гетероциклический кольцо с внутренним дисульфидная связь.

использованная литература
- ^ Cairns, T. L .; Evans, G.L .; Larchar, A. W .; McKusick, B.C. (1952). «драгоценные камни-дитиолы». Журнал Американского химического общества. 74: 3982–9. Дои:10.1021 / ja01136a004.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Руни, Джеймс П.К. (2007). «Роль тиолов, дитиолов, факторов питания и взаимодействующих лигандов в токсикологии ртути». Токсикология. 234 (3): 145–156. Дои:10.1016 / j.tox.2007.02.016. PMID 17408840.
- ^ Conrow, R.E .; Ле Уэру, Ю. (2004). «1,3-Пропандиол». В Л. Пакетте (ред.). Энциклопедия реагентов для органического синтеза. J. Wiley & Sons, Нью-Йорк. Дои:10.1002 / 047084289X. Cite имеет пустой неизвестный параметр:
|1=(Помогите)




