Карборан - Carborane
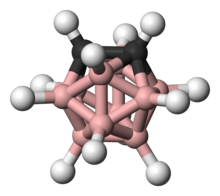
Карбораны электронно-делокализованные (неклассически связанные) кластеры, состоящие из бор, углерод и водород атомы, которые также могут содержать другие металлические и неметаллические элементы в каркасе кластера.[1] Как и многие другие гидриды бора эти кластеры многогранники или фрагменты многогранников, и аналогично классифицируются как клозо-, нидо-, арахно-, гифо-, и т. д. в зависимости от того, представляют ли они полный (близко-) многогранник, или многогранник без одного (нидо-), два (арахно-), три (дефо-) или более вершин. Карбораны являются ярким примером гетеробораны.
Карбораны имеют от 5 до 14 атомов в каркасе клетки (15, если включены атомы металла), но большинство из них имеют два атома углерода каркаса; из них самая известная серия - это серия близко-C2BпЧАСп + 2 системы, в которых n = от 3 до 12. Однако были получены карбораны, содержащие от 1 до 6 каркасных атомов углерода, а также ряд карборановых моно- и дианионов. Икосаэдрический CB11ЧАС12− анион - сильная кислота, а его полихлорированное производное H (CHB11Cl11) это суперкислотный.
В икосаэдр нейтральный по заряду близко -карбораны, 1,2-, 1,7- и 1,12-C2B10ЧАС12 (соответственно орто-, мета-, и параграф-карборан в неофициальной номенклатуре) особенно стабильны и коммерчески доступны.[2] Эти богатые бором кластеры обладают уникальными органометик свойства с химической реакционной способностью, соответствующей классическим органическим молекулам, но структурно подобны неорганическим и металлоорганическим соединениям на основе металлов[3]
C2B10ЧАС12 изомеры вместе с другими карборановыми кластерами и металлакарборанами (см. ниже) используются в широком диапазоне применений, включая термостойкие полимеры, извлечение радиоактивных металлов из ядерных отходов, катализ, новые электроактивные материалы и медицинские приложения. Как и другие электронно-делокализованные полиэдрические кластеры, электронная структура этих кластерных соединений может быть описана Правила Уэйда – Минго.[4]
Как отмечалось выше, карбораны тесно связаны с гидридами бора (бораны ), и, таким образом, структурно сильно отличаются от углеводородов из-за того факта, что атомы углерода имеют на один валентный электрон больше, чем атомы бора (примечательной особенностью карборанов является то, что углеродные атомы каркаса часто напрямую связаны с целыми 6 или даже более того, соседние атомы, в отличие от углеводородов). Карбораны и бораны имеют трехмерную геометрию каркаса (кластера), чтобы облегчить их электронно-делокализованную неклассическую связь, тогда как углеводороды обычно представляют собой цепи или кольца; например, B4ЧАС10 имеет арахно геометрия клетки, а изомеры бутана п- и iso-C4ЧАС10, с электронами на 4 больше, чем B4ЧАС10, принимают линейные или разветвленные цепные структуры. Примеры нидо и арахно- карбораны включают 2,3-С2B4ЧАС8 и 1,3-С2B7ЧАС13, соответственно. Могут существовать геометрические изомеры карборанов, что требует использования числовых префиксов в названии соединения; это иллюстрируется 1,2-, 1,7- и 1,2-C2B10ЧАС12 упомянутые ранее икосаэдрические кластеры.[примечание 1][заметка 2][заметка 3]
Подготовка
Карбораны были получены многими различными способами, наиболее распространенным из которых является добавление алкинильных реагентов к кластерам гидрида бора с образованием дикарбоновых карборанов. Например, высокотемпературная реакция пентаборана (9) с ацетиленом образует несколько клозо-карборанов, а также другие продукты:
- нидо-B5ЧАС9 + C2ЧАС2 близко-1,5-С2B3ЧАС5, близко-1,6-С2B4ЧАС6, 2,4-С2B5ЧАС7
Когда реакцию проводят при более низких температурах, получают карборан с открытой клеткой:
- нидо-B5ЧАС9 + C2ЧАС2 нидо-2,4-С2B4ЧАС8
Другие процедуры генерируют карбораны, содержащие три или четыре каркасных атома углерода (ссылки [1], [4], [5])
Производные монокарбы
Мононуклеозкарбораны представляют собой кластеры с BпC. клетки. 12-вершинная производная изучена лучше всего, но известно несколько.
Обычно их получают путем добавления одноуглеродных реагентов к кластерам гидрида бора. Одноуглеродные реагенты включают цианид, изоцианиды, и формальдегид. Например, монокарбадодекаборат ([CB11ЧАС12]−) производится из декаборан и формальдегид с последующим добавлением боран диметилсульфид.[8][9]
Грозди дикарба
Дикарббораны могут быть получены из гидридов бора с использованием алкинов в качестве источника двух углеродных центров. В добавок к близко-C2BпЧАСп + 2 серии, упомянутой выше, известно несколько видов дикарбонов в открытых клетках, включая нидо-C2B3ЧАС7 (изоструктурный и изоэлектронный с B5ЧАС9) и арахно-C2B7ЧАС13.
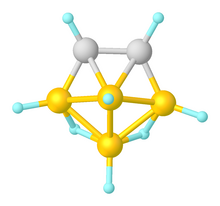
Синтезы икосаэдра близко-дикарбадодекаборана производные (R2C2B10ЧАС10) используют алкины в качестве R2C2 источник и декаборан (B10ЧАС14) для питания B10 единица.
Кластеры трикарба, тетракарба, пентакарба и гексакарба
Карбораны, содержащие более двух атомов углерода в каркасе скелета, полученные различными способами, включают производные нидо-C3B3ЧАС7, нидо-C3B8ЧАС11, нидо-C4B2ЧАС6, нидо-C4B4ЧАС8, нидо-C5BH6+, и арахно-ЧАС6C6B6Et6 (ссылка [1]).
Изомерия
Многие дикарббораны существуют в виде изомеров, которые различаются относительным расположением углеродных центров. В дополнение к трем ранее упомянутым икосаэдрам C2B10ЧАС12 соединений, изомерия также обнаруживается в некоторых более мелких близко-карборановые системы, например, 1,2- и 1,6-C2B4ЧАС6, 2,3- и 2,4-С2B5ЧАС7, 1,2- и 1,6-С2B6ЧАС8, и 2,3- и 2,4-С2B5ЧАС7, а также в карборанах открытого типа, таких как 2,3- и 2,4-C2B4ЧАС8 и 1,2 и 1,3-C2B9ЧАС13.
В общем, изомеры, содержащие несмежные атомы углерода каркаса, более термически стабильны, чем изомеры с соседними атомами углерода, так что нагрев имеет тенденцию вызывать взаимное разделение атомов углерода в каркасе. Это иллюстрируется термической изомеризацией 1,2- в 1,6-C2B4ЧАС6 и от 1,2- до 1,7-С2B10ЧАС12. Формирование 1,12-C2B10ЧАС12 (параграф-карборан) изомер требует гораздо более высоких температур (около 600 ° C), сопровождаемых некоторым разложением (ссылки [1], [4] и [5]).
Реакции
Карбораны претерпевают самые разные реакции. Депротонирование близко-dicarbadodecaboranes с использованием литийорганический реагенты дает дилитиопроизводные.[11]
- C2B10ЧАС12 + 2 БуЛи → Ли2C2B10ЧАС10 + 2 BuH
Эти дилитиированные соединения реагируют с различными электрофилами, например хлорфосфины, хлорсиланы и сера.[12]
Вызванное основанием разложение карборанов дает анионные нидопроизводные, которые можно использовать в качестве лиганды для переходных металлов, генерирующих металлакарбораны, которые представляют собой карбораны, содержащие один или несколько атомов переходного металла или металла основной группы в каркасе клетки, обнаруженные в 1965 году.[13] Основная часть работ по металлакарборанам была сосредоточена на 12-вершинном МК.2B9 И м2C2B8 кластеры и 7-вершинные МК2B4 И м2C2B3 (трехэтажный[14] и многодековый сэндвич[15]) кластеров, но также были приготовлены металлокарбораны с 6-15 вершинами,[16] как и кластеры с различным числом атомов углерода, бора и металлов (см. ссылки [1], [4 [, и [5]). Диборолил-металлические комплексы с MC3B2 И м2C3B2 клетки, представляющие другой тип металлакарборана, также были тщательно изучены [17]
Исследование
Комплексы дикарболлида были оценены для многих приложений в течение многих лет, но коммерческое применение редко. Бис (дикарболлид) [Co (C2B9ЧАС11)2]− использовался как осадитель для удаления 137CS+ от радиоактивных отходов.[18]
Были изучены медицинские применения карборанов.[19][20] С-функционализированные карбораны представляют собой источник бора для борная нейтронозахватная терапия.[21]
Некоторые комплексы металлов проявляют каталитические свойства.[22]
Соединение H (CHB11Cl11) это суперкислотный, образуя выделяемую соль с протонированный бензол, С6ЧАС+
7.[23] Он протонирует фуллерен, С60.[24]
Смотрите также
Примечания
- ^ Для общих обзоров химии карборана см. «Химия элементов», стр. 181–189.[5] и "Advanced Inorganic Chemistry, Sixth Edition, pp. 131-174".[6]
- ^ Недавнее всестороннее исследование этой области с ежегодным обновлением ссылок можно найти в Carboranes 3rd Ed.[1]
- ^ Электронно-делокализованная связь в боранах и карборанах подробно обсуждается в Гидриды бора[7]
Рекомендации
- ^ а б Граймс, Р. Н., Карбораны 3-е изд., Эльзевир, Амстердам и Нью-Йорк (2016) ISBN 9780128018941
- ^ Джеммис, Э. (1982). «Контроль перекрытия и стабильность полиэдрических молекул. Клозо-карбораны». Журнал Американского химического общества. 104 (25): 7017–7020. Дои:10.1021 / ja00389a021.
- ^ Спокойный, А. М. (2013). «Новые лигандные платформы с богатыми бором кластерами в качестве органометических заместителей». Чистая и прикладная химия. 85 (5): 903–919. Дои:10.1351 / PAC-CON-13-01-13. ЧВК 3845684. PMID 24311823.
- ^ Правила Уэйда-Мингоса впервые были сформулированы Кеннет Уэйд в 1971 г. и расширен на Майкл Мингос в 1972 г .:
* Уэйд, Кеннет (1971). «Структурное значение количества скелетных связывающих электронных пар в карборанах, высших боранах и анионах борана, а также различных соединениях кластера карбонила переходных металлов». J. Chem. Soc. D. 1971: 792–793. Дои:10.1039 / C29710000792.
* Мингос, Д. М. П. (1972). «Общая теория кластерных и кольцевых соединений основной группы и переходных элементов». Природа Физические науки. 236: 99–102. Дои:10.1038 / Physci236099a0.
Иногда их называют просто «правилами Уэйда».
* Уэлч, Алан Дж. (2013). «Значение и влияние правил Уэйда». Chem. Commun. 49: 3615–3616. Дои:10.1039 / C3CC00069A. - ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Расширенная неорганическая химия, шестое издание, Ф. А. Коттон, Г. Уилкинсон, К. А. Мурильо и М. Бохманн, Wiley Interscience, 1999, глава 5 (Р. Н. Граймс).
- ^ Липскомб В.Н. Гидриды бора. Бенджамин, Нью-Йорк (1963) |
- ^ У. Х. Нот (1967). «1-Б9ЧАС9CH− и B11ЧАС11CH−". Варенье. Chem. Soc. 89: 1274–1275. Дои:10.1021 / ja00981a048.
- ^ Tanaka, N .; Shoji, Y .; Фукусима, Т. (2016). «Удобный путь к монокарба-клозо-додекаборатным анионам». Металлоорганические соединения. 35: 2022–2025. Дои:10.1021 / acs.organomet.6b00309.CS1 maint: использует параметр авторов (связь)
- ^ Г.С. Поули (1966). «Дальнейшее улучшение некоторых твердых соединений бора». Acta Crystallogr. 20: 631–638. Дои:10.1107 / S0365110X66001531.
- ^ Попеску, А.-Р .; Musteti, A.D .; Феррер-Угальде, А .; Виньяс, С .; Núñez, R .; Тейксидор, Ф. (2012). "Влияние эфирного растворителя на литийорганические соединения: случай карбораниллития". Химия - Европейский журнал. 18: 3174–3184. Дои:10.1002 / chem.201102626.CS1 maint: использует параметр авторов (связь)
- ^ Джин, Г.-Х. (2004). «Успехи химии металлоорганических комплексов с 1,2-дихалькогенолато-о-карборановыми лигандами». Coord. Chem. Rev. 248: 587–602. Дои:10.1016 / j.ccr.2004.01.002.
- ^ Хоторн, М. Ф .; Янг, Д. С .; Wegner, P.A.J. Am. Chem. Soc. 1965, 87, 1818
- ^ Beer, D.C .; Миллер, В. Р .; Sneddon, L.G .; Grimes, R.N .; Мэтью, М .; Palenik, G. J. J. Am. Chem. Soc. 1973, 95, 3046
- ^ Ван, X .; Sabat, M .; Grimes, R. N. J. Am. Chem. Soc. 1995, 117, 12227
- ^ Deng, L .; Се, З. (2007). «Достижения в химии карборанов и металлов - Бах, Б .; Не, Ю.; Прицков, Х .; Зиберт, У. Дж. Органомет. Хим. 2004, 689, 429 лакарборанов с более чем 12 вершинами». Coord. Chem. Rev. 251: 2452–2476. Дои:10.1016 / j.ccr.2007.02.009.CS1 maint: использует параметр авторов (связь)
- ^ Бах, Б .; Nie, Y .; Pritzkow, H .; Siebert, W. J. Organomet. Chem. 2004, 689, 429
- ^ Dash, B.P .; Satapathy, R .; Swain, B.R .; Mahanta, C.S .; Jena, B. B .; Хосман, Н. С. (2017). «Бис (дикарболлид) анион кобальта и его производные». J. Organomet. Chem. 849–850: 170–194. Дои:10.1016 / j.jorganchem.2017.04.006.CS1 maint: использует параметр авторов (связь)
- ^ Issa, F .; Kassiou, M .; Рендина, Л. М. (2011). «Бор в открытии лекарств: карбораны как уникальные фармакофоры в биологически активных соединениях». Chem. Rev. 111: 5701–5722. Дои:10.1021 / cr2000866.CS1 maint: использует параметр авторов (связь)
- ^ Стокманн, Филипп; Гоцци, Марта; Kuhnert, Роберт; Sárosi, Menyhárt B .; Эй-Хокинс, Эвамари (2019). «Новые ключи от старых замков: карборансодержащие препараты как платформы для механизированной терапии». Обзоры химического общества. 48: 3497–3512. Дои:10.1039 / C9CS00197B.

- ^ Soloway, A.H .; Tjarks, W .; Barnum, B.A .; Rong, F.-G .; Barth, R. F .; Codogni, I.M .; Уилсон, Дж. Г. (1998). "Химия нейтронно-захватной терапии". Химические обзоры. 98 (4): 1515–1562. Дои:10.1021 / cr941195u. PMID 11848941.
- ^ Crowther, D. J .; Baenziger, N.C .; Джордан, Р. Ф. (1991). «Химия дикарболлидов металлов группы 4. Синтез, структура и реакционная способность электрофильных алкильных комплексов (Cp *) (C2B9ЧАС11) M (R), M = Hf, Zr ". Журнал Американского химического общества. 113 (4): 1455–1457. Дои:10.1021 / ja00004a080.
- ^ Olah, G. A .; Пракаш, Г. К. С .; Sommer, J .; Мольнар, А. (2009). Суперкислотная химия (2-е изд.). Вайли. п.41. ISBN 978-0-471-59668-4.
- ^ Рид Кристофер А (2013). «Мифы о протоне. Природа H+ в конденсированных средах ». Соотв. Chem. Res. 46 (11): 2567–2575. Дои:10.1021 / ar400064q. ЧВК 3833890. PMID 23875729.


