Бензил - Benzil
 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Дифенилэтандион | |
| Систематическое название ИЮПАК 1,2-дифенилэтан-1,2-дион | |
| Другие имена Дифенилэтан-1,2-дион Бензил Дибензоил Бибензоил Дифенилглиоксаль | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 608047 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.004.689 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C14ЧАС10О2 | |
| Молярная масса | 210.232 г · моль−1 |
| Внешность | желтый кристаллический порошок |
| Плотность | 1,23 г / см3твердые (1,255 г / см3, рентгеновский снимок) |
| Температура плавления | От 94,0 до 96,0 ° С; От 201,2 до 204,8 ° F; От 367,1 до 369,2 К |
| Точка кипения | От 346,0 до 348,0 ° С; От 654,8 до 658,4 ° F; От 619,1 до 621,1 К |
| нерастворимый | |
| Растворимость в этиловый спирт | растворимый |
| Растворимость в диэтиловый эфир | растворимый |
| Растворимость в бензол | растворимый |
| -118.6·10−6 см3/ моль | |
| Структура | |
| P31,221[1] | |
| 3.8 D[2] | |
| Опасности | |
| Главный опасности | Раздражающий |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| H315, H319, H335 | |
| P261, P264, P271, P280, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P403 + 233, P405, P501 | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Связанный дикетоны | биацетил |
Родственные соединения | бензофенон глиоксаль бибензил |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
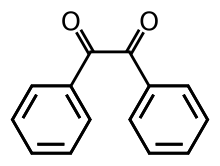
Бензил (систематически известный как 1,2-дифенилэтан-1,2-дион) является органическое соединение с формулой (C6ЧАС5CO )2, обычно сокращенно (Ph CO)2. Это желтое твердое вещество - одно из самых распространенных дикетоны. Его основное использование - как фотоинициатор в химия полимеров.[3]
Структура
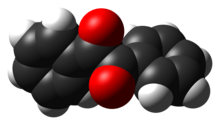
Наиболее примечательной структурной особенностью соединения является его длинная углерод-углеродная связь из 1,54 Å, что указывает на отсутствие пи-связи между двумя карбонильными центрами. Центры PhCO плоские, но пара бензоильных групп скручена относительно друг друга с двугранный угол 117 °.[4] Менее затрудненный аналоги (глиоксаль, биацетил, Щавелевая кислота производные), (RCO)2 группа принимает плоскую антиконформацию.
Приложения
Больше всего бензил используется в свободных радикалах. лечение из полимер сети. Ультрафиолетовый радиация разлагает бензил, образуя свободные радикалы в материале, способствуя образованию перекрестные ссылки. Бензил - мощный ингибитор человеческого карбоксилэстеразы, ферменты, участвующие в гидролизе сложных карбоновых эфиров и многих клинически используемых лекарств.[5]
Бензил является относительно плохим фотоинициатором и используется редко. Он поглощает на длине волны 260 нм. Он подвергается фотообесцвечивание, что позволяет свету для полимеризации проникать в более глубокие слои материала при более длительном воздействии.[6]
Реакции
Benzil - стандартный строительный блок в органический синтез. Конденсируется с аминами с образованием дикетимин лиганды. Классический органическая реакция бензила - это перегруппировка бензиловой кислоты, в котором основание катализирует превращение бензила в бензиловую кислоту. Эта реактивность используется при приготовлении препарата. фенитоин. Бензил также реагирует с 1,3-дифенилацетон в альдольная конденсация давать тетрафенилциклопентадиенон.
Подготовка
Бензил готовится из бензоин, например с ацетат меди (II):[7]
- PhC (O) CH (OH) Ph + 2 Cu2+ → PhC (O) C (O) Ph + 2 H+ + 2 Cu+
Другие подходящие окислители, такие как азотная кислота (HNO3) используются регулярно.
Хлорид железа (III) (FeCl3) можно использовать в качестве недорогого катализатора этого химического превращения.[8]
Рекомендации
- ^ Acta Crystallogr. B43 398 (1987)
- ^ Spectrochim. Acta A60 (8-9) 1805 (2004)
- ^ Хардо Сигель, Манфред Эггерсдорфер «Кетоны» в Энциклопедии промышленной химии Ульманна Wiley-VCH, 2002, Wiley-VCH, Weinheim. Дои:10.1002 / 14356007.a15_077
- ^ Куанг. Шен, Кольбьорн. Hagen "Газофазная молекулярная структура и конформация бензила, как определено электронной дифракцией" J. Phys. Chem., 1987, 91 (6), стр 1357–1360. Дои:10.1021 / j100290a017.
- ^ Вадкинс. Р. М. и др. "Идентификация и характеристика новых аналогов бензила (дифенилэтан-1,2-диона) как ингибиторов карбоксилэстераз млекопитающих. J. Med. Chem., 2005 48 стр. 2906-15.
- ^ Артур Грин, У. (22 апреля 2010 г.). Промышленные фотоинициаторы: техническое руководство. ISBN 9781439827468.
- ^ Depreux, P .; Bethegnies, G .; Марсинкаль-Лефевр, А. (1988). «Синтез бензила из бензоина с ацетатом меди (II)». Журнал химического образования. 65 (6): 553. Bibcode:1988JChEd..65..553D. Дои:10.1021 / ed065p553.
- ^ Би, Сяосинь; Ву, Линтао; Ян, Чаогуо; Цзин, Сяоби; Чжу, Хунсян (2011). «Синтез бензилов в одной емкости из альдегидов путем димеризации бензоина, катализируемой Nhc, в безметалловых условиях в воде». Журнал Чилийского химического общества. 56 (2): 663. Дои:10.4067 / S0717-97072011000200008.

