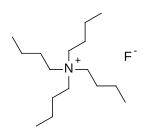
Фторид тетра-н-бутиламмония - Tetra-n-butylammonium fluoride
 | |
| Имена | |
|---|---|
| Название ИЮПАК Тетра-п-фторид бутиламмония | |
| Другие имена Фторид тетрабутиламмония; TBAF; п-Bu4NF | |
| Идентификаторы | |
| |
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.006.417 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| (C4ЧАС9)4NF | |
| Молярная масса | 261,46 г / моль |
| Температура плавления | От 58 до 60 ° C (от 136 до 140 ° F, от 331 до 333 K) (тригидрат) |
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Тетра-п-фторид бутиламмония, обычно сокращенно TBAF и п-Bu4NF, это четвертичная аммониевая соль с химической формулой (CH3CH2CH2CH2)4N+F−. Он коммерчески доступен в виде белого твердого тригидрата и в виде раствора в тетрагидрофуран. TBAF используется как источник фторид ион в органических растворителях.[1]
Подготовка и свойства
TBAF можно подготовить, пройдя плавиковая кислота через ионообменная смола, с последующим бромид тетрабутиламмония. После испарения воды TBAF можно собрать в виде масла с количественным выходом.[1]
Подготовка безводный образцов представляет интерес как основность фторид увеличивается более чем на 20 пK единиц при переходе от водных к апротонный растворитель.[нужна цитата ] Однако нагрев образцов гидратированного материала до 77 ° C в вакууме вызывает разложение до дифторид водорода соль.[2] Точно так же образцы, высушенные при 40 ° C в высоком вакууме, все еще содержат 0,1-0,3 мол.% Воды и около 10% дифторида.[3] Вместо этого безводный TBAF был получен реакцией гексафторбензол и цианид тетрабутиламмония. Растворы соли в ацетонитрил и диметилсульфоксид стабильны.[4]
Реакции и использование
Поскольку фторид ион такой сильный водородная связь акцептор, его соли имеют тенденцию к гидратации и ограничены растворимость в органических растворителях. В качестве источника фторид-ионов TBAF решает эту проблему, хотя природа фторида неясна, поскольку образцы TBAF почти всегда гидратированы, что приводит к образованию бифторида (HF2−) гидроксид (OH−), а также фторид. Многие приложения допускают использование гетерогенных или плохо определенных источников фтора.
В качестве источника фторида в органических растворителях TBAF используется для удаления силиловый эфир защитные группы. Он также используется как катализатор межфазного переноса и как мягкий основание. В качестве агента для снятия защиты TBAF в DMSO будет превращать O-силилированные еноляты в карбонилы. Со связями C-Si TBAF дает карбанионы, которые могут захватываться электрофилами или подвергаться протонолизу.[1][5]
Рекомендации
- ^ а б c Ли, Хуэй-Инь; Солнце, Хаорань; ДиМаньо, Стивен Г. (2007). «Фторид тетрабутиламмония». В пакете, Лео А. (ред.). Энциклопедия реагентов для органического синтеза. Джон Вили и сыновья. Дои:10.1002 / 9780470842898.rt015.pub2.
- ^ Рамеш К. Шарма; Джеймс Л. Фрай (1983). «Неустойчивость безводных фторидов тетра-н-алкиламмония». Журнал органической химии. 48 (12): 2112–4. Дои:10.1021 / jo00160a041.
- ^ Д. Филлип Кокс; Яцек Терпинский; Витольд Лавринович (1984). "'Безводный фторид тетрабутиламмония: мягкий, но очень эффективный источник нуклеофильного фторид-иона ». Журнал органической химии. 49 (17): 3216–9. Дои:10.1021 / jo00191a035.
- ^ Хаоран Сан и Стивен Дж. ДиМаньо (2005). «Безводный фторид тетрабутиламмония». Журнал Американского химического общества. 127 (7): 2050–1. Дои:10.1021 / ja0440497. PMID 15713075.
- ^ Нина Гоммерманн и Пауль Кнохель "N, N-Дибензил-N- [1-циклогексил-3- (триметилсилил) -2-пропинил] амин из циклогексанкарбальдегида, триметилсилилацетилена и дибензиламина" Org. Synth. 2007, 84, 1. Дои:10.15227 / orgsyn.084.0001
дальнейшее чтение
- К. Хироя; Р. Жука; М. Камеда; А. Ясухара и Т. Сакамото (2001). «Реакции циклизации производных 2-алкинилбензилового спирта и 2-алкинилбензиламина, промотированные фторидом тетрабутиламмония». Тетраэдр. 57 (48): 9697–710. Дои:10.1016 / S0040-4020 (01) 00991-7..
