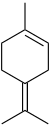
Терпинен - Terpinene
| |||
| |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК α: 4-метил-1- (1-метилэтил) -1,3-циклогексадиен β: 4-метилен-1- (1-метилэтил) циклогексен γ: 4-метил-1- (1-метилэтил) -1,4-циклогексадиен δ: 1-метил-4- (пропан-2-илиден) циклогекс-1-ен | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.440 | ||
| UNII |
| ||
| |||
| |||
| Характеристики | |||
| C10ЧАС16 | |||
| Молярная масса | 136.238 г · моль−1 | ||
| Плотность | α: 0,8375 г / см3 β: 0,838 г / см3 γ: 0,853 г / см3 | ||
| Температура плавления | α: 60-61 ° С | ||
| Точка кипения | α: 173,5–174,8 ° С β: 173-174 ° С γ: 183 ° С | ||
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
В терпинены группа изомерный углеводороды, которые классифицируются как монотерпены. Каждый из них имеет одинаковую молекулярную формулу и углеродный каркас, но они различаются положением двойных углерод-углеродных связей. α-терпинен был выделен из кардамон и майоран масла и из других природных источников. β-Терпинен не имеет известного природного источника, но был получен из сабинен. γ-терпинен и δ-терпинен (также известный как терпинолен) были выделены из различных растительных источников. Все они представляют собой бесцветные жидкости с запахом скипидара.[1]
Производство и использование
α-Терпинен получают в промышленности путем катализируемой кислотой перегруппировки α-пинен. Он обладает парфюмерными и вкусовыми свойствами, но в основном используется для придания приятного запаха промышленным жидкостям. Гидрирование дает насыщенную производную п-метан.[1]
Биосинтез α-терпинена

Биосинтез α-терпинена и других терпеноидов происходит через мевалонатный путь потому что его исходный реагент, диметилаллил пирофосфат (DMAPP), происходит от мевалоновая кислота.
Геранилпирофосфат (GPP) образуется в результате реакции резонансно-стабильного аллильного катиона, образованного в результате потери пирофосфатной группы из DMAPP, и изопентенилпирофосфат (IPP), и последующая потеря протона. Затем GPP теряет пирофосфатную группу с образованием резонансно-стабильного геранильного катиона. Повторное введение пирофосфатной группы в катион дает изомер GPP, известный как линалил пирофосфат (LPP). LPP затем образует резонансно-стабильный катион, теряя свою пирофосфатную группу. Циклизация затем завершается благодаря этой более благоприятной стереохимии катиона LPP, теперь образуя терпинильный катион. Наконец, сдвиг 1,2-гидрида через Перегруппировка Вагнера-Меервейна образует катион терпинен-4-ила. Именно потеря водорода из этого катиона приводит к образованию α-терпинена.
Растения, производящие терпинен
Рекомендации
- ^ а б М. Эггерсдорфер (2005). «Терпены». Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH. Дои:10.1002 / 14356007.a26_205. ISBN 3527306730.CS1 maint: использует параметр авторов (связь)
- ^ Дьюик, П. М. (2009). Лекарственные натуральные продукты: биосинтетический подход. Соединенное Королевство: John Wiley & Sons. стр.187 –197.
- ^ Ли, Ронг; Цзы-Тао Цзян (2004). «Химический состав эфирного масла Cuminium cyminum L. из Китая». Журнал вкусов и ароматов. 19 (4): 311–313. Дои:10.1002 / ffj.1302.
- ^ Ван, Лу; Ван, З; Чжан, Х; Ли, Х; Чжан, Х; и другие. (2009). «Ультразвуковая распылительная экстракция в сочетании с однокапельной микроэкстракцией и газовой хроматографией-масс-спектрометрией для анализа эфирного масла в Цюминий циминум Л. ". Analytica Chimica Acta. 647 (1): 72–77. Дои:10.1016 / j.aca.2009.05.030. PMID 19576388.
- ^ Iacobellis, Nicola S .; Lo Cantore, P; Capasso, F; Senatore, F; и другие. (2005). «Антибактериальная активность эфирных масел Cuminium cyminum L. и Carum carvi L.». Журнал сельскохозяйственной и пищевой химии. 53 (1): 57–61. Дои:10.1021 / jf0487351. PMID 15631509.
- ^ Хиллиг, Карл В. (октябрь 2004 г.). «Хемотаксономический анализ терпеноидных вариаций в каннабисе». Биохимическая систематика и экология. 32 (10): 875–891. Дои:10.1016 / j.bse.2004.04.004. ISSN 0305-1978.
- ^ Шахвар, Мухаммад Хурам; Эль-Гораб, Ахмед Хасан; Анджум, Факир Мухаммад; Батт, Масуд Садик; Хуссейн, Шахзад; Надим, Мухаммад (01.07.2012). «Характеристика семян и листьев кориандра (Coriandrum sativum L.): летучие и нелетучие экстракты». Международный журнал свойств пищевых продуктов. 15 (4): 736–747. Дои:10.1080/10942912.2010.500068. ISSN 1094-2912.