Диалкилбиарилфосфиновые лиганды - Dialkylbiaryl phosphine ligands
В органический и металлоорганическая химия, лиганды диалкилбиарилфосфина (или диалкилбиарилфосфина) находятся фосфор -содержащие опорные лиганды которые используются для регулирования химической активности палладий и другие переходный металл катализаторы на основе. Впервые они были описаны Стивен Л. Бухвальд в 1998 г. для заявок в реакции сочетания, катализируемые палладием с образованием углерод-азотных и углерод-углеродных связей.[1] До их разработки использование фосфиновых лигандов первого или второго поколения для катализируемого палладием перекрестного связывания с образованием связи C-N (например, трис (о-толил) фосфин и БИНАП соответственно) требовали суровых условий, а масштабы трансформации были сильно ограничены. Реакции кросс-сочетания Сузуки-Мияуры и Негиши обычно проводили с Pd (PPh3)4 в качестве катализатора и в основном ограничивались арилбромидами и иодидами при повышенных температурах, в то время как широко доступные арилхлориды не вступали в реакцию. Для устранения этих ограничений была необходима разработка новых классов лигандов.
Со времени этого первоначального отчета группами Бухвальда и Хартвига, среди других лабораторий, была проделана обширная работа по разработке стерически затрудненных и богатых электронами фосфиновых лигандов, позволяющих катализировать широкий спектр реакций, включая Аминирование Бухвальда-Хартвига и этерификация реакции, Кросс-сцепление Negishi, и Кросс-муфта Suzuki-Miyaura.[2] В частности, группа Бухвальда сосредоточилась на разработке диалкилбиарилфосфиновых лигандов, в то время как группа Хартвига исследовала бисфосфиноферроценовые и триалкилфосфиновые лиганды. Благодаря открытию группой Бухвальда и широкому развитию диалкилбиарилфосфиновых лигандов, они также неофициально известны как «лиганды Бухвальда».[3]
Диалкилбиарилфосфиновые лиганды оказались очень успешными для этих применений в перекрестном связывании, что позволило реализовать большие возможности для этих превращений. Более того, производные BrettPhos (см. Ниже) уникально способны достигать катализируемого палладием связывания арил (псевдо) галогенидов с множеством сложных нуклеофилов, включая фторид, трифторметил источники, нитрит (для синтеза нитроарена) и цианат (для синтеза мочевины через изоцианаты). В дополнение к этим процессам их использование также было расширено до превращений, катализируемых золото, серебро, медь, родий, и рутений, среди других переходных металлов.[4] Сегодня эти лиганды широко используются как в академических кругах, так и в промышленности.
Общие особенности
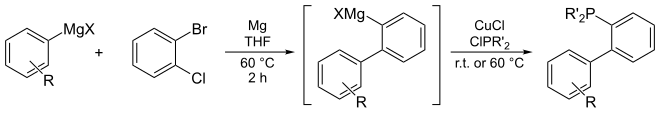
Все лиганды Бухвальда представляют собой устойчивые на воздухе кристаллические вещества. Многие из них можно купить на рынке или синтезировать всего за несколько шагов из недорогих исходных материалов. Протоколы с одним горшком были разработаны для синтеза этих лигандов и используются в весах> 10 кг.[5][6]

Их повышенная каталитическая активность по сравнению с другими лигандами в реакции сочетания, катализируемые палладием были объяснены их электронным богатством, стерическим объемом и некоторыми особенностями структуры. В частности, циклогексил, т-бутильные и адамантильные группы на фосфоре используются для этой цели в качестве объемных электронодонорных заместителей. Нижнее кольцо бифенильной системы, орто к группе фосфино, также является ключевой структурной особенностью. Многочисленные кристаллографические исследования показали, что он ведет себя как гемилабильный лиганд и, как полагают, играет роль в стабилизации высокореактивного, формально 12-электронного LPd(0) промежуточное звено во время каталитического цикла. Недавно разработанные лиганды обычно используют 2,6-замещение в нижнем кольце для предотвращения разложения катализатора посредством Pd-опосредованного C-H активация этих позиций. Обширные эксперименты группы Бухвальда показали, что дальнейшие незначительные изменения в структуре этих лигандов могут резко изменить их каталитическую активность в реакциях кросс-сочетания с различными субстратами. Это привело к появлению множества лигандов, приспособленных для определенных трансформаций.[7] Обеспечивая средства создания постулируемого каталитически активного LPd(0) видов в мягких условиях (комнатная температура или ниже во многих случаях), разработка нескольких поколений активированных основанием, циклопалладированных предварительных катализаторов еще больше расширила применимость лигандов и упростила их использование.[8][3]
Некоторые из наиболее известных и продаваемых на рынке диалкилбиарилфосфиновых лигандов и их применения описаны ниже в приблизительном порядке дат их открытия. Их имена часто происходят от имени или инициала сотрудника группы Бухвальда, который открыл лиганд, или (в трех случаях) после кошек Бухвальда, если у первооткрывателя уже был лиганд, ранее названный в его / ее честь.
DavePhos
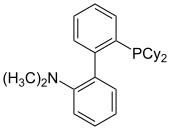
DavePhos является первым описанным диалкилбиарилфосфиновым лигандом и первоначально использовался в мягких катализируемых Pd реакциях кросс-сочетания Сузуки-Мияуры, а также аминированиях Бухвальда-Хартвига.[9] Этот лиганд дополнительно использовался для катализа широкого спектра реакций, включая арилирование кетонов.[10] и сложные эфиры,[11] борилирование арилхлоридов,[12] и арилирование индолов.[13]
Синтезировано много дополнительных модифицированных версий DavePhos. Было показано, что tBuDavePhos является еще более реактивным вариантом DavePhos при взаимодействии Сузуки-Мияуры арилбромидов и хлоридов при комнатной температуре.[14] Бифенильный эквивалент (PhDavePhos) также доступен в качестве альтернативного катализатора в соединениях Suzuki-Miyaura.
JohnPhos
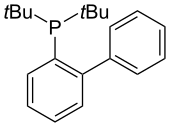
Названный в честь Джон П. Вулф JohnPhos был первоначально использован в 1999 году в катализируемых палладием реакциях Сузуки-Мияуры с арилбромидами и хлоридами.[15] Это позволяет взаимодействовать затрудненным субстратам при комнатной температуре с чрезвычайно низкой загрузкой катализатора. С тех пор этот лиганд использовался во многих реакциях, включая аминирование широкого спектра арилгалогенидов и трифлатов.[16][17] а также арилирование тиофенов.[18]
Несколько модифицированных версий этого лиганда, включая PhJohnPhos и CyJohnPhos, также были исследованы на предмет их использования в Pd-катализируемых перекрестных связях.
MePhos

Впервые сообщалось в 1999 г., что MePhos оказался в равной степени компетентным лигандом в катализируемом Pd Suzuki-Miyaura, как и в случае DavePhos и JohnPhos.[19] Он также может образовывать активный катализатор при образовании арилкетонов.[20] Варианты этого лиганда, включая тBuMePhos также имеется в продаже.
Сотрудники Amgen обнаружили, что перекрестное связывание Suzuki на поздней стадии (на пути к новому ингибитору киназы p38 MAP) лучше всего катализируется Pd2(dba)3Каталитическая система MePhos. Эту реакцию проводили в масштабе килограммов, и не требовалось специальной обработки по удалению палладия, поскольку избыток имидазола, присутствующий на конечной стадии амидного сочетания, координировался с Pd и давал удаляемый побочный продукт.[21]

XPhos
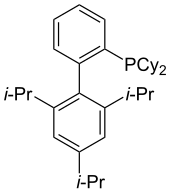
XPhos впервые был использован в 2003 году для общего аминирования и амидирования аренсульфонатов и арилгалогенидов.[22] XPhos также использовался в катализируемом Pd борилировании арил- и гетероарилхлоридов.[23]
Также сообщалось о модифицированных версиях XPhos. Более затрудненные tBuXPhos и Me4tButylXPhos использовались в образовании диариловых эфиров.[24] Включение сульфонатной группы в положение 4 позволяет использовать этот лиганд для Муфты Sonogashira в водных двухфазных растворителях.[25]
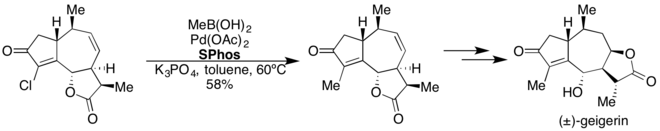
SPhos

SPhos впервые сообщалось в 2004 году как чрезвычайно компетентный лиганд в катализе реакций сочетания Сузуки-Мияура.[26] Этот лиганд обеспечивает перекрестное связывание гетероарильных, богатых электронами и бедных электронами арильных и винилбороновых кислот с различными арил- и гетероарилгалогенидами в мягких условиях реакции. SPhos также использовался в катализируемом Pd борилировании арил- и гетероарилхлоридов.[27]
Было показано, что 3-сульфонатные варианты этого лиганда (sSPhos) катализируют сочетания Сузуки-Мияура в водной среде.[28] Одним из примеров применения SPhos в академических кругах было его использование в 8-ступенчатом общем синтезе (±) -гейгерина.[29]
РуФос

Впервые о RuPhos было сообщено в 2004 году как о части высокореакционной каталитической системы для катализируемого палладием соединения Негиши цинкоорганических соединений с арилгалогенидами.[30] Эти лиганды позволяют как сильно затрудненным субстратам, так и субстратам с широким спектром функциональных групп подвергаться этой реакции. Было также показано, что этот лиганд эффективен при катализе таких реакций, как трифторметилирование арилхлоридов.[31] и аминирования арилгалогенидов.[32]
BrettPhos
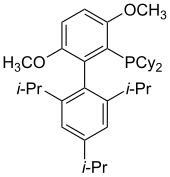
BrettPhos впервые был представлен в 2008 году для катализируемого Pd аминирования арилмезилатов и арилгалогенидов.[33] Этот лиганд способствует связыванию слабых нуклеофилов с арилгалогенидами. Примечательно, что этот лиганд обладает высокой селективностью к моноарилированию первичных аминов с минимальным образованием диарилированного продукта. BrettPhos также хемоселективен в отношении первичных аминов по сравнению с вторичными аминами. Другие применения BrettPhos в катализе включают трифторметилирование арилхлоридов,[34] образование арилтрифторметилсульфидов,[35] и кросс-муфты Suzuki-Miyaura.[36]
Несколько модифицированных версий BrettPhos также коммерчески доступны. Было показано, что tBuBrettPhos является надежным лигандом при каталитическом превращении арилтрифлатов и арилбромидов в арилфториды.[37] а также синтез ароматических нитросоединений.[38] Чрезвычайно громоздкий AdBrettPhos можно использовать при амидировании пятичленных гетероциклических галогенидов, содержащих несколько гетероатомов (таких как галоимидазолы и галогенпиразолы).[39]
CPhos

CPhos был использован в качестве высокоактивного лиганда в катализируемом Pd связывании по Негиши вторичных алкилцинковых реагентов с арилгалогенидами.[40]
Альфос
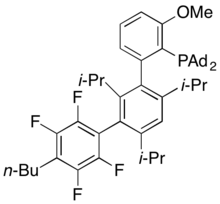
AlPhos - один из новейших коммерчески доступных диалкилбиарилфосфиновых лигандов.[41] Сообщалось в 2015 году, что этот лиганд позволяет осуществлять мягкое катализируемое Pd фторирование арил- и гетероарилтрифлатов.[42]
Смотрите также
Рекомендации
- ^ Старый, Дэвид У .; Вулф, Джон П .; Бухвальд, Стивен Л. (сентябрь 1998 г.). «Высокоактивный катализатор для реакций поперечного взаимодействия, катализируемых палладием: муфты Сузуки при комнатной температуре и аминирование неактивированных арилхлоридов». Журнал Американского химического общества. 120 (37): 9722–9723. Дои:10.1021 / ja982250 +.
- ^ Surry, Дэвид С .; Бухвальд, Стивен Л. (2011). «Диалкилбиарилфосфины в Pd-катализируемом аминировании: руководство пользователя». Chem. Наука. 2 (1): 27–50. Дои:10.1039 / C0SC00331J. ISSN 2041-6539. ЧВК 3306613. PMID 22432049.
- ^ а б Bruno, N.C .; Бухвальд, С. Л. (2014). Палладиевые предкатализаторы для реакций поперечной связи (PDF). Strem Chemiker.
- ^ Surry, Дэвид С .; Бухвальд, Стивен Л. (11 августа 2008 г.). "Биарилфосфановые лиганды в аминировании, катализируемом палладием". Angewandte Chemie International Edition. 47 (34): 6338–6361. Дои:10.1002 / anie.200800497. ISSN 1521-3773. ЧВК 3517088. PMID 18663711.
- ^ Мартин, Рубен; Бухвальд, Стивен Л. (18 ноября 2008 г.). «Катализируемые палладием реакции Сузуки-Мияура перекрестного связывания с использованием диалкилбиарилфосфиновых лигандов». Отчеты о химических исследованиях. 41 (11): 1461–1473. Дои:10.1021 / ar800036s. ISSN 0001-4842. ЧВК 2645945. PMID 18620434.
- ^ Кэй, Стивен; Фокс, Джозеф М .; Хикс, Фредерик А .; Бухвальд, Стивен Л. (31 декабря 2001 г.). «Использование каталитических количеств CuCl и других улучшений на пути бензина к фосфиновым лигандам на основе бифенила». Расширенный синтез и катализ. 343 (8): 789–794. Дои:10.1002 / 1615-4169 (20011231) 343: 8 <789 :: AID-ADSC789> 3.0.CO; 2-A. ISSN 1615-4169.
- ^ Мартин, Рубен; Бухвальд, Стивен Л. (18 ноября 2008 г.). «Катализируемые палладием реакции Сузуки-Мияура перекрестного связывания с использованием диалкилбиарилфосфиновых лигандов». Отчеты о химических исследованиях. 41 (11): 1461–1473. Дои:10.1021 / ar800036s. ISSN 0001-4842. ЧВК 2645945. PMID 18620434.
- ^ Бискоу, Марк Р .; Fors, Brett P .; Бухвальд, Стивен Л. (2008-05-01). «Новый класс легко активируемых предкатализаторов палладия для простых реакций кросс-связывания C − N и низкотемпературного окислительного добавления арилхлоридов». Журнал Американского химического общества. 130 (21): 6686–6687. Дои:10.1021 / ja801137k. ЧВК 2587037. PMID 18447360.
- ^ Старый, Дэвид У .; Вулф, Джон П .; Бухвальд, Стивен Л. (сентябрь 1998 г.). «Высокоактивный катализатор для реакций поперечного взаимодействия, катализируемых палладием: муфты Сузуки при комнатной температуре и аминирование неактивированных арилхлоридов». Журнал Американского химического общества. 120 (37): 9722–9723. Дои:10.1021 / ja982250 +.
- ^ Фокс, Джозеф М .; Хуан, Сяохуа; Чиффи, Андре; Бухвальд, Стивен Л. (1 февраля 2000 г.). «Высокоактивные и селективные катализаторы образования α-арилкетонов». Журнал Американского химического общества. 122 (7): 1360–1370. Дои:10.1021 / ja993912d. ISSN 0002-7863.
- ^ Moradi, Wahed A .; Бухвальд, Стивен Л. (2001). «Катализируемое палладием α-арилирование сложных эфиров». Журнал Американского химического общества. 123 (33): 7996–8002. Дои:10.1021 / ja010797 +. ISSN 0002-7863. PMID 11506555.
- ^ Биллингсли, Кельвин Л .; Бардер, Тимоти Э .; Бухвальд, Стивен Л. (9 июля 2007 г.). "Катализированное палладием борилирование арилхлоридов: область применения, применения и вычислительные исследования". Angewandte Chemie International Edition. 46 (28): 5359–5363. Дои:10.1002 / anie.200701551. ISSN 1521-3773. PMID 17562550.
- ^ Старый, Дэвид У .; Harris, Michele C .; Бухвальд, Стивен Л. (1 мая 2000 г.). «Эффективное N-арилирование индолов, катализируемое палладием». Органические буквы. 2 (10): 1403–1406. Дои:10.1021 / ol005728z. ISSN 1523-7060. PMID 10814458.
- ^ Вулф, Джон П .; Певец, Роберт А .; Ян, Брайант Х .; Бухвальд, Стивен Л. (1 октября 1999 г.). «Высокоактивные палладиевые катализаторы для реакций сцепления Suzuki». Журнал Американского химического общества. 121 (41): 9550–9561. Дои:10.1021 / ja992130h. ISSN 0002-7863.
- ^ Вулф, Джон П .; Певец, Роберт А .; Ян, Брайант Х .; Бухвальд, Стивен Л. (1 октября 1999 г.). «Высокоактивные палладиевые катализаторы для реакций сцепления Suzuki». Журнал Американского химического общества. 121 (41): 9550–9561. Дои:10.1021 / ja992130h. ISSN 0002-7863.
- ^ Вулф, Джон П .; Томори, Хироши; Sadighi, Joseph P .; Инь, Цзинцзюнь; Бухвальд, Стивен Л. (1 февраля 2000 г.). «Простая и эффективная система катализаторов для катализируемого палладием аминирования арилхлоридов, бромидов и трифлатов» (PDF). Журнал органической химии. 65 (4): 1158–1174. Дои:10.1021 / jo991699y. ISSN 0022-3263. PMID 10814067.
- ^ Surry, Дэвид С .; Бухвальд, Стивен Л. (11 августа 2008 г.). "Биарилфосфановые лиганды в аминировании, катализируемом палладием". Angewandte Chemie International Edition. 47 (34): 6338–6361. Дои:10.1002 / anie.200800497. ISSN 1521-3773. ЧВК 3517088. PMID 18663711.
- ^ Окадзава, Тору; Сато, Тэцуя; Миура, Масахиро; Номура, Масакацу (1 мая 2002 г.). «Катализируемое палладием множественное арилирование тиофенов». Журнал Американского химического общества. 124 (19): 5286–5287. Дои:10.1021 / ja0259279. ISSN 0002-7863.
- ^ Вулф, Джон П .; Певец, Роберт А .; Ян, Брайант Х .; Бухвальд, Стивен Л. (1 октября 1999 г.). «Высокоактивные палладиевые катализаторы для реакций сцепления Suzuki». Журнал Американского химического общества. 121 (41): 9550–9561. Дои:10.1021 / ja992130h. ISSN 0002-7863.
- ^ Фокс, Джозеф М .; Хуан, Сяохуа; Чиффи, Андре; Бухвальд, Стивен Л. (1 февраля 2000 г.). «Высокоактивные и селективные катализаторы образования α-арилкетонов». Журнал Американского химического общества. 122 (7): 1360–1370. Дои:10.1021 / ja993912d. ISSN 0002-7863.
- ^ Тиль, Оливер; Ахматович, Михал; Милберн, Роберт (11 июня 2012 г.). «Исследование и разработка процессов для гетероциклических ингибиторов киназы p38 MAP». Synlett. 23 (11): 1564–1574. Дои:10.1055 / с-0031-1290425.
- ^ Хуан, Сяохуа; Андерсон, Кевин В .; Зим, Данило; Цзян, Лэй; Клапарс, Артис; Бухвальд, Стивен Л. (1 июня 2003 г.). «Расширение процессов образования связи C-N, катализируемых Pd: первое амидирование арилсульфонатов, водное аминирование и комплементарность реакциям, катализируемым медью». Журнал Американского химического общества. 125 (22): 6653–6655. Дои:10.1021 / ja035483w. ISSN 0002-7863. PMID 12769573.
- ^ Биллингсли, Кельвин Л .; Бардер, Тимоти Э .; Бухвальд, Стивен Л. (9 июля 2007 г.). "Катализированное палладием борилирование арилхлоридов: область применения, применения и вычислительные исследования". Angewandte Chemie International Edition. 46 (28): 5359–5363. Дои:10.1002 / anie.200701551. ISSN 1521-3773. PMID 17562550.
- ^ Бургос, Карлос Х .; Бардер, Тимоти Э .; Хуан, Сяохуа; Бухвальд, Стивен Л. (26 июня 2006 г.). «Существенно улучшенный метод Pd-катализируемого связывания фенолов с арилгалогенидами: понимание эффектов лиганда». Angewandte Chemie International Edition. 45 (26): 4321–4326. Дои:10.1002 / anie.200601253. ISSN 1521-3773. PMID 16733839.
- ^ Андерсон, Кевин В .; Бухвальд, Стивен Л. (26 сентября 2005 г.). «Общие катализаторы для реакций связывания Сузуки – Мияуры и Соногашира арилхлоридов и для связывания сложных комбинаций субстратов в воде». Angewandte Chemie International Edition. 44 (38): 6173–6177. Дои:10.1002 / anie.200502017. ISSN 1521-3773. PMID 16097019.
- ^ Уокер, Шон Д .; Бардер, Тимоти Э .; Мартинелли, Джозеф Р .; Бухвальд, Стивен Л. (26 марта 2004 г.). «Рационально разработанный универсальный катализатор для процессов взаимодействия Сузуки – Мияура». Angewandte Chemie International Edition. 43 (14): 1871–1876. Дои:10.1002 / anie.200353615. ISSN 1521-3773. PMID 15054800.
- ^ Биллингсли, Кельвин Л .; Бардер, Тимоти Э .; Бухвальд, Стивен Л. (9 июля 2007 г.). "Катализированное палладием борилирование арилхлоридов: область применения, применения и вычислительные исследования". Angewandte Chemie International Edition. 46 (28): 5359–5363. Дои:10.1002 / anie.200701551. ISSN 1521-3773. PMID 17562550.
- ^ Андерсон, Кевин В .; Бухвальд, Стивен Л. (26 сентября 2005 г.). «Общие катализаторы для реакций связывания Сузуки – Мияуры и Соногашира арилхлоридов и для связывания сложных комбинаций субстратов в воде». Angewandte Chemie International Edition. 44 (38): 6173–6177. Дои:10.1002 / anie.200502017. ISSN 1521-3773. PMID 16097019.
- ^ Карре, Себастьян; Депрес, Жан-Пьер (10 сентября 2007 г.). «Доступ к гвайанолидам: высокоэффективный стереоконтролируемый полный синтез (±) -Гейгерина». Angewandte Chemie International Edition. 46 (36): 6870–6873. Дои:10.1002 / anie.200702031. ISSN 1521-3773. PMID 17676568.
- ^ Милн, Жаклин Э .; Бухвальд, Стивен Л. (1 октября 2004 г.). «Чрезвычайно активный катализатор реакции перекрестной связи Негиши». Журнал Американского химического общества. 126 (40): 13028–13032. Дои:10.1021 / ja0474493. ISSN 0002-7863. PMID 15469301.
- ^ Чо, Ын Джин; Senecal, Todd D .; Кинзель, Том; Чжан, Юн; Уотсон, Дональд А .; Бухвальд, Стивен Л. (25 июня 2010 г.). «Катализируемое палладием трифторметилирование арилхлоридов». Наука. 328 (5986): 1679–1681. Bibcode:2010Sci ... 328.1679C. Дои:10.1126 / science.1190524. ISSN 0036-8075. ЧВК 3005208. PMID 20576888.
- ^ Чарльз, Марк Д .; Шульц, Филипп; Бухвальд, Стивен Л. (1 сентября 2005 г.). «Эффективное Pd-катализируемое аминирование гетероарилгалогенидов». Органические буквы. 7 (18): 3965–3968. Дои:10.1021 / ol0514754. ISSN 1523-7060. PMID 16119943.
- ^ Fors, Brett P .; Уотсон, Дональд А .; Бискоу, Марк Р .; Бухвальд, Стивен Л. (15 октября 2008 г.). «Высокоактивный катализатор для реакций аминирования, катализируемых Pd: реакции перекрестного связывания с использованием арилмезилатов и высокоселективного моноарилирования первичных аминов с использованием арилхлоридов». Журнал Американского химического общества. 130 (41): 13552–13554. Дои:10.1021 / ja8055358. ISSN 0002-7863. ЧВК 2748321. PMID 18798626.
- ^ Чо, Ын Джин; Senecal, Todd D .; Кинзель, Том; Чжан, Юн; Уотсон, Дональд А .; Бухвальд, Стивен Л. (25 июня 2010 г.). «Катализируемое палладием трифторметилирование арилхлоридов». Наука. 328 (5986): 1679–1681. Bibcode:2010Sci ... 328.1679C. Дои:10.1126 / science.1190524. ISSN 0036-8075. ЧВК 3005208. PMID 20576888.
- ^ Теверовский, Георгий; Surry, Дэвид С .; Бухвальд, Стивен Л. (1 августа 2011 г.). «Катализируемый Pd синтез соединений Ar-SCF3 в мягких условиях». Angewandte Chemie International Edition. 50 (32): 7312–7314. Дои:10.1002 / anie.201102543. ISSN 1521-3773. ЧВК 3395331. PMID 21692157.
- ^ Бхайана, Бриджеш; Fors, Brett P .; Бухвальд, Стивен Л. (3 сентября 2009 г.). «Универсальная каталитическая система для реакций кросс-связывания Сузуки-Мияура C (sp2) -тозилатов и мезилатов». Органические буквы. 11 (17): 3954–3957. Дои:10.1021 / ol9015892. ISSN 1523-7060. ЧВК 2759755. PMID 19663467.
- ^ Уотсон, Дональд А .; Су, Минцзюань; Теверовский, Георгий; Чжан, Юн; Гарсия-Фортанет, Хорхе; Кинзель, Том; Бухвальд, Стивен Л. (25 сентября 2009 г.). «Образование ArF из LPdAr (F): Каталитическое превращение арилтрифлатов в арилфториды». Наука. 325 (5948): 1661–1664. Bibcode:2009Sci ... 325.1661W. Дои:10.1126 / science.1178239. ISSN 0036-8075. ЧВК 3038120. PMID 19679769.
- ^ Fors, Brett P .; Бухвальд, Стивен Л. (16 сентября 2009 г.). «Катализируемое палладием превращение арилхлоридов, трифлатов и нонафлатов в нитроароматические соединения». Журнал Американского химического общества. 131 (36): 12898–12899. Дои:10.1021 / ja905768k. ISSN 0002-7863. ЧВК 2773681. PMID 19737014.
- ^ Су, Минцзюань; Бухвальд, Стивен Л. (7 мая 2012 г.). «Объемный биарилфосфиновый лиганд позволяет проводить катализируемое палладием амидирование пятичленных гетероциклов в качестве электрофилов». Angewandte Chemie International Edition. 51 (19): 4710–4713. Дои:10.1002 / anie.201201244. ISSN 1521-3773. ЧВК 3407381. PMID 22473747.
- ^ Хан, Чонг; Бухвальд, Стивен Л. (10 июня 2009 г.). «Сочетание Негиши вторичных галогенидов алкилцинка с арилбромидами и хлоридами». Журнал Американского химического общества. 131 (22): 7532–7533. Дои:10.1021 / ja902046m. ISSN 0002-7863. ЧВК 2746668. PMID 19441851.
- ^ «AlPhos и [(AlPhosPd) 2 • COD] для фторирования, катализируемого палладием». Сигма-Олдрич. Получено 2018-08-17.
- ^ Sather, Aaron C .; Ли, Хон Гын; Де ла Роса, Валентина Ю .; Ян, Ян; Мюллер, Питер; Бухвальд, Стивен Л. (21 октября 2015 г.). «Фторированный лиганд делает возможным региоселективное Pd-катализируемое фторирование арилтрифлатов и бромидов при комнатной температуре». Журнал Американского химического общества. 137 (41): 13433–13438. Дои:10.1021 / jacs.5b09308. ISSN 0002-7863. ЧВК 4721526. PMID 26413908.
