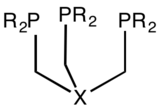
Триподальный лиганд - Tripodal ligand

Триподальные лиганды находятся три- и тетрадентатный лиганды с C3 симметрия. Они популярны в исследованиях в области координационная химия и гомогенный катализ. Поскольку лиганды полидентатны, они не легко диссоциируют от металлического центра.
Координационная химия
При использовании в координационные комплексы с октаэдрическая молекулярная геометрия то трезубец лиганды треноги занимают одну сторону, что приводит к фиксированному лица (или же фак) геометрия. В тетрадентатный триподные лиганды занимают четыре смежных сайта, оставляя два СНГ позиции доступны на восьмигранном металлическом центре. Связавшись с четырех- и пятикоординатными металлическими центрами, эти лиганды накладывают C3 симметрия, которая может привести к необычным лигандное поле шаблоны разделения. Триподальные лиганды часто способны координировать насыщение ионов металлов более низкими координационные номера.
Одним из триподальных лигандов коммерческого значения является нитрилотриацетат, N (CH2CO2−)3 потому что он дешево производится и имеет высокое сродство к ионам двухвалентных металлов. Другие триаминные лиганды включают: трен (N (CH2CH2NH2)3) и цис-1,3,5-триаминоциклогексан.[1] Определенный трифосфины например RC (CH2PPh2)3 также являются триподными. В рукава триподных лигандов были включены многие виды донорных групп, включая амидо (Р2N−),[2] и N-гетероциклические карбены.
- Примеры триподных лигандов

Трис (2-пиридилметил) амин, тетрадентный триодальный лиганд, популярный в биоинорганическая химия.[5]
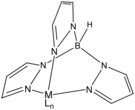
Структура металлического комплекса триспиразолилборат, анионный тридентатный триподный лиганд, поскольку он имитирует три имидазольных лиганда.[6]

NTA является коммерчески важным триподальным лигандом. Его три группы карбоновых кислот подвергаются депротонированию при образовании комплекса.
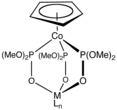
В Kläui лиганд, дианионный металлорганический лиганд.
Рекомендации
- ^ Эйми Дж. Гэмбл, Джейсон М. Линам, Роберт Дж. Тэтчер, Пол Х. Уолтон, Адриан К. Уитвуд (2013). «Цис-1,3,5-триаминоциклогексан в качестве лиганда, блокирующего лиганд для рутения (II)». Неорг. Chem. 52: 4517–4527. Дои:10.1021 / ic302819j.CS1 maint: использует параметр авторов (связь)
- ^ Веркаде, Дж. Г. (1993). «Атраны: новые примеры с неожиданными свойствами». Соотв. Chem. Res. 26: 483. Дои:10.1021 / ar00033a005.
- ^ Шварценбах, Герольд; Бюрги, Ханс-Бит; Дженсен, Уильям П .; Лоуренс, Джеффри А .; Мёнстед, Лене; Сарджесон, Алан М. (1983). «Кислотное расщепление комплексов никеля (Ii), содержащих цис, цис-1,3,5-циклогексантриамин (TACH), кристаллическая структура [Ni (tach) (H2O)3](НЕТ3)2, и взаимосвязь между структурой и реакционной способностью никель-полиаминовых комплексов ». Неорганическая химия. 22 (26): 4029–4038. Дои:10.1021 / ic00168a042.
- ^ Саума, К. Т., Петерс, Дж. К. (2011). «M-E и M = E комплексы железа и кобальта, которые подчеркивают тройную симметрию (E = O, N, NR)». Coord. Chem. Rev. 255: 920. Дои:10.1016 / j.ccr.2011.01.009.CS1 maint: несколько имен: список авторов (связь)
- ^ Блэкман, А. Г. (2008). «Триподальные тетрааминовые лиганды, содержащие три пиридиновых звена: другие полипиридильные лиганды». Евро. J. Inorg. Chem.: 2633. Дои:10.1002 / ejic.200800115.
- ^ Паркин, Г. (2000). «Биоинорганическая химия цинка: синтетические аналоги ферментов цинка, содержащие триподальные лиганды». Химические коммуникации: 1971-1985. Дои:10.1039 / B004816J.