Ротигаптид - Rotigaptide
 | |
| Имена | |
|---|---|
| Название ИЮПАК N-Ацетил-D-тирозил-D-пролил- (4S) -4-гидрокси-D-пролилглицил-D-аланилглицинамид | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭМБЛ | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C28ЧАС39N7О9 | |
| Молярная масса | 617.660 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ротигаптид (ЗП-123) - это лекарственный препарат, который проходит клинические испытания для лечения сердечные аритмии - конкретно мерцательная аритмия. Это пептид аналог, который, как было показано, увеличивает щелевой переход межклеточная проводимость в клетки сердечной мышцы.[1] Щелевые соединения - это белковые каналы, которые отвечают за проведение электрических импульсов между клетками сердца для поддержания нормального ритма. Модуляция щелевого соединения - многообещающий и новый механизм действия для лечения сердечно-сосудистых заболеваний.[1] Его пептидная последовательность - Ac-D-Tyr-D-Pro-D-Hyp-Gly-D-Ala-Gly-NH2.
Показания
Ротигаптид изучается на предмет его антиаритмических эффектов, особенно для лечения фибрилляции предсердий.[2] Мерцательная аритмия - нерегулярный и часто учащенный сердечный ритм. Нерегулярный ритм возникает из-за аномальных электрических импульсов в сердце. Неравномерность может быть постоянной или прерывистой. При фибрилляции предсердий несколько импульсов проходят через предсердия одновременно. Вместо скоординированного сокращения, сокращения предсердий нерегулярные, дезорганизованные и очень быстрые.[2] Эти нерегулярные импульсы достигают AV узел в быстрой последовательности, но не все из них проходят через AV-узел. Следовательно, желудочки сокращаются в нерегулярном ритме медленнее. В результате учащенное, нерегулярное сердцебиение вызывает нерегулярный пульс, а иногда и ощущение трепетания в груди.
Механизм действия
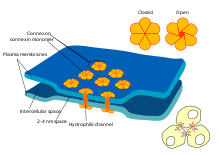
Точный механизм действия ротигаптида полностью не изучен. Однако считается, что ротигаптид оказывает свое влияние на кардиомиоцит щелевые соединения через фосфорилирование События. Каждый щелевой переход состоит из серии коннексоны в непосредственной близости друг от друга. Каждый коннексон состоит из 6 функциональных блоков (коннексины ), которые соединяются вместе, образуя канал между соседними ячейками.[3] Ротигаптид действует на коннексины, предпочтительно, на коннексин 43 (Сх43).[4] Было показано, что лечение ротигаптидом активирует различные протеинкиназа C (PKC) изоформы, вызывающие фосфорилирование Сх43, что способствует правильному функционированию коннексона.[5] Это позволяет более гладкой проводимости проходить через миоциты для распространения синхронного сокращения.[6] Было показано, что это снижает частоту фибрилляции предсердий.[2]
Ограничения
Потенциальным ограничением для этого препарата является то, что животных, используемых для исследований, чаще всего анестезируют изофлуран, который, как было показано, является частичным разобщителем щелевых соединений и, таким образом, сводит на нет эффекты ротигаптида.[7] Однако этот эффект может быть лишь незначительным, так как одно исследование показало, что низкая доза изофлурана сохранялась непрерывно на протяжении всего исследования, что указывает на то, что доза была недостаточно высокой для отсоединения ротигаптида. Поэтому маловероятно, что изофлуран играет роль в представленных результатах.[2]
Рекомендации
- ^ а б Широшита-Такешита А., Сакабе М., Хауган К., Хэннан Дж., Наттель С. (2007). Зависящие от модели эффекты антиаритмического пептида ротигаптида (ZP123), усиливающего проводимость щелевого соединения, на экспериментальную фибрилляцию предсердий у собак. Тираж. 115: 310- 318.
- ^ а б c d Герра Дж, Эверетт Т., Ли К., Уилсон Э, Ольгин Дж (2006). Влияние модификатора щелевого соединения ротигаптида (ZP123) на предсердную проводимость и уязвимость к фибрилляции предсердий. Тираж. 114: 110-118.
- ^ Verheule S, van Kempen MJ, te Welscher PH, Kwak BR, Jongsma HJ (1997). Характеристика каналов щелевого соединения в миокарде предсердий и желудочков взрослых кроликов. Циркуляционные исследования. 80(5): 673-681.
- ^ Хеннан К., Свилло Р., Морган Дж., Кейт Дж., Шауб Р., Смит Р., Фельдман Х, Хауган К., Кантровиц Дж., Ван П., Абу-Каре А., Бутера Дж., Ларсен Б., Крэндалл Д. (2006). Ротигаптид (ZP123) предотвращает спонтанные желудочковые аритмии и уменьшает размер инфаркта во время ишемии / реперфузии миокарда у собак с открытой грудью. JPET. 317: 236– 243.
- ^ Axelsen L, Stahlhut M, Mohammed S, Due Larsen B, Nielsen M, Holstein-Rathlou NH, Søren Andersen, Jensen O, Hennan J, Kjølbye A (2006). Идентификация регулируемых ишемией сайтов фосфорилирования в коннексине 43: возможная мишень для аналога антиаритмического пептида ротигаптида (ZP123). Журнал молекулярной и клеточной кардиологии. 40: 790-798.
- ^ Кларк Т., Томас Д., Петерсен Дж, Эванс В., Мартин П. (2006). Антиаритмический пептид ротигаптид (ZP123) увеличивает межклеточную коммуникацию щелевых соединений в сердечных миоцитах и клетках HeLa, экспрессирующих коннексин 43. Британский журнал фармакологии. 147: 486–495.
- ^ Мантц Дж., Кордье Дж., Джоум С. (1993). Влияние общих анестетиков на межклеточные коммуникации, опосредованные щелевыми контактами между астроцитами в первичной культуре. Анестезиология. 78: 892–901.
