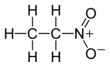
Нитроэтан - Nitroethane
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Нитроэтан | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.001.081 | ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | ООН 2842 | ||
| |||
| |||
| Характеристики | |||
| C2ЧАС5NО2 | |||
| Молярная масса | 75.067 г · моль−1 | ||
| Плотность | 1,054 г / см3 | ||
| Температура плавления | -90 ° С (-130 ° F, 183 К) | ||
| Точка кипения | От 112,0 до 116,0 ° C (от 233,6 до 240,8 ° F; от 385,1 до 389,1 K) | ||
| Слабо растворим (4,6 г / 100 мл при 20 ° C) | |||
| Давление газа | 21 мм рт. Ст. (25 ° C)[1] | ||
| Кислотность (пKа) | 16.7[2][3] | ||
| -35.4·10−6 см3/ моль | |||
| Вязкость | 0.677 Па · с при 20 ° C | ||
| Опасности | |||
| Главный опасности | Легковоспламеняющийся, вредный | ||
| Паспорт безопасности | Паспорт безопасности материалов на сайте fishersci.com | ||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасность | ||
| H226, H302, H315, H331, H341, H412 | |||
| P210, P261, P312, P301, P330, P304, P340, P312, P370, P378, P403 + 233 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 28 ° С (82 ° F, 301 К) | ||
| Пределы взрываемости | 3.4%-?[1] | ||
| Смертельная доза или концентрация (LD, LC): | |||
LC50 (средняя концентрация ) | 5000 частей на миллион (кролик, 2 часа)[4] | ||
LCLo (самый низкий опубликованный ) | 6250 частей на миллион (мышь, 2 часа)[4] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 100 частей на миллион (310 мг / м3)[1] | ||
REL (Рекомендуемые) | TWA 100 частей на миллион (310 мг / м3)[1] | ||
IDLH (Непосредственная опасность) | 1000 частей на миллион[1] | ||
| Родственные соединения | |||
Связанный нитросоединения | 2-нитропропан Нитрометан | ||
Родственные соединения | Этилнитрит Этилнитрат | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Нитроэтан является органическое соединение имеющий химическую формулу C2ЧАС5НЕТ2. Во многом похож на нитрометан, нитроэтан представляет собой маслянистую жидкость при стандартной температуре и давлении. Чистый нитроэтан бесцветен и имеет фруктовый запах.
Подготовка
Нитроэтан получают промышленным путем путем обработки пропан с азотная кислота при 350–450 ° С. Этот экзотермический В результате реакции образуются четыре промышленно значимых нитроалкана: нитрометан, нитроэтан, 1-нитропропан, и 2-нитропропан. В реакции участвуют свободные радикалы, такие как CH3CH2CH2О., возникающие при гомолизе соответствующего нитритного сложный эфир. Эти алкокси-радикалы подвержены реакциям фрагментации C — C, что объясняет образование смеси продуктов.[5]
В качестве альтернативы нитроэтан может производиться Виктор Мейер реакция галогенэтанов, таких как хлорэтан, бромэтан, или же йодэтан с нитритом серебра в диэтиловый эфир или же THF. Модификация этой реакции Корнблюма использует нитрат натрия в любом диметилсульфоксид или же диметилформамид растворитель.[6]
Использует
Через конденсации, такие как Реакция Генри, нитроэтан превращается в несколько соединений, представляющих коммерческий интерес. Конденсация с 3,4-диметоксибензальдегид дает предшественник антигипертензивный препарат, средство, медикамент метилдопа; конденсация с незамещенным бензальдегидом дает фенил-2-нитропропен. Нитроэтан конденсируется с двумя эквивалентами формальдегид дать, после гидрирование, 2-амино-2-метил-1,3-пропандиол, который, в свою очередь, конденсируется с олеиновой кислотой с образованием оксазолина, который протонируется с образованием катионного поверхностно-активное вещество.[5]
Как и некоторые другие нитрованные органические соединения, нитроэтан также используется в качестве топливная добавка и предшественник Ракетное топливо.
Нитроэтан - полезный растворитель для таких полимеров, как полистирол и особенно полезен для растворения цианоакрилат клеи. В косметике он использовался как компонент в искусственный ноготь съемник и в аэрозольных баллончиках для герметика потолка.
Нитроэтан ранее успешно использовался в качестве химического сырья (ингредиентов-прекурсоров) в лабораториях для синтеза множества веществ и потребительских товаров, например Первитин в медицине использовался широко в XIX и XX веках (особенно популярным во время Второй мировой войны союзными войсками и нацистами для повышения настроения, подавления аппетита и сна, а также повышения концентрации внимания и внимания), нитроалканы были одним из многих ингредиентов, используемых в синтезе многих фенэтиламины, включая лекарства, такие как первитин и рацемическое соединение Бензедрин.[7] анорексическое лекарство от ожирения.[8]
Токсичность
Предполагается, что нитроэтан вызывает генетические повреждения и вреден для нервная система. Типичное значение TLV / TWA составляет 100 частей на миллион. Типичное значение STEL составляет 150 частей на миллион. Причины контакта с кожей дерматит в людях. В исследованиях на животных наблюдалось, что воздействие нитроэтана вызывает слезотечение, одышка, легочные хрипы, отек, повреждение печени и почек и наркоз.[9] Дети отравились в результате случайного проглатывания жидкости для снятия искусственных ногтей.[10]
В LD50 для крыс - 1100 мг / кг.[11]
Рекомендации
- ^ а б c d е Карманный справочник NIOSH по химической опасности. "#0453". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Райх, Ганс. "Таблица Bordwell pKa:" Нитроалканы"". Химический факультет Университета Висконсина. Получено 17 января 2016.
- ^ Мэтьюз, Уолтер; и другие. (1975). «Равновесные кислотности углеродных кислот. VI. Установление абсолютной шкалы кислотностей в растворе диметилсульфоксида». Журнал Американского химического общества. 97 (24): 7006. Дои:10.1021 / ja00857a010.
- ^ а б «Нитроэтан». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ а б Шелдон Б. Маркофски «Нитросоединения, алифатические» в Энциклопедия промышленной химии Ульмана, Wiley-VCH, Weinheim, 2002. Дои:10.1002 / 14356007.a17_401.
- ^ Агравал, Джай (2007). Органическая химия взрывчатых веществ. Чичестер, Англия: John Wiley & Sons. С. 7–10. ISBN 9780470029671.
- ^ «Резюме национальной оценки лекарственных средств за 2016 год» (PDF). Управление по лекарствам. Ноябрь 2016 г.
- ^ «Резюме национальной оценки лекарственных средств за 2016 год» (PDF). Управление по лекарствам. Ноябрь 2016 г.
- ^ «Информация о химическом отборе проб нитроэтана». Получено 9 февраля 2007 г. с веб-сайта Управления по охране труда США.
- ^ Хорнфельдт CS, Рабе WH (1994). «Отравление нитроэтаном от искусственного средства для удаления ногтей». J. Toxicol. Clin. Токсикол. 32 (3): 321–4. Дои:10.3109/15563659409017967. PMID 8007041.
- ^ MSDS для нитроэтана (пересмотрен 3 октября 2005 г.), как сообщает Fisher Scientific.