Метоксиметанол - Methoxymethanol
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Метоксиметанол | |
| Другие имена Формальдегид метил гемиацеталь | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 1900186 | |
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard | 100.022.476 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Свойства | |
| C2ЧАС6О2 | |
| Молярная масса | 62.068 г · моль−1 |
| Плотность | 0.948 |
| Опасности | |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Предупреждение |
| H226, H302, H371 | |
| P210, P233, P240, P241, P242, P243, P260, P264, P270, P280, P301 + 312, P303 + 361 + 353, P309 + 311, P330, P370 + 378, P403 + 235, P405, P501 | |
| точка возгорания | 39,9 ° С (103,8 ° F, 313,0 К) |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
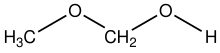
Метоксиметанол химическое соединение, которое одновременно эфир и алкоголь, а гемиформный.[1] Структурную формулу можно записать как CH3ОСН2ОЙ. Он был обнаружен в космосе.[2]
Формирование
Метоксиметанол образуется спонтанно, когда водный раствор формальдегид и метанол смешаны.[3][1] или когда формальдегид барботируют через метанол.[4]
В космосе метоксиметанол может образовываться, когда метанольные радикалы (CH2ОН или СН3O) реагировать. Это продукты радиолиза, полученные при попадании ультрафиолетового света или космических лучей на замороженный метанол.[3]
Метанол может реагировать с углекислый газ и водород при 80 ° C и некотором давлении с катализатором из рутения или кобальта, чтобы получить некоторое количество метоксиметанола.[5]
Свойства
Различные конформации молекулы - это гош-гауче (Gg), гош-гауче (Gg ') и транс-гош (Tg).[6]
использованная литература
- ^ а б Майвальд, Майкл; Фишер, Хольгер H .; Отт, Майкл; Пешла, Роджер; Кунерт, Кристиан; Крейтер, Корнелиус Г .; Маурер, Герд; Хассе, Ганс (январь 2003 г.). «Количественная ЯМР-спектроскопия сложных жидких смесей: методы и результаты химического равновесия формальдегид-вода-метанол при температурах до 383 К». Промышленные и инженерные химические исследования. 42 (2): 259–266. Дои:10.1021 / ie0203072.
- ^ McGuire, Brett A .; Shingledecker, Christopher N .; Уиллис, Эрик Р .; Burkhardt, Andrew M .; Эль-Абд, Самер; Мотиенко, Роман А .; Brogan, Crystal L .; Хантер, Тодд Р .; Маргулес, Лоран; Гийемен, Жан-Клод; Гаррод, Робин Т .; Хербст, Эрик; Ремиджан, Энтони Дж. (2017). «ALMA обнаружение межзвездного метоксиметанола (CH3OCH2OH)». Астрофизический журнал. 851 (2): L46. arXiv:1712.03256. Bibcode:2017ApJ ... 851L..46M. Дои:10.3847 / 2041-8213 / aaa0c3. S2CID 119211919.
- ^ а б Хейс, Брайан М .; Видикус Уивер, Сюзанна Л. (6 мая 2013 г.). «Теоретическая экспертиза O (1D) Реакции введения с образованием метандиола, метоксиметанола и аминометанола ». Журнал физической химии A. 117 (32): 7142–7148. Bibcode:2013JPCA..117.7142H. Дои:10.1021 / jp400753r. PMID 23646865.
- ^ Celik, Fuat E .; Лоуренс, Генри; Белл, Алексис Т. (июнь 2008 г.). «Синтез предшественников этиленгликоля из формальдегида и метилформиата, катализируемый гетерополикислотами». Журнал молекулярного катализа A: химический. 288 (1–2): 87–96. Дои:10.1016 / j.molcata.2008.03.029.
- ^ Dixneuf, Pierre H .; Суле, Жан-Франсуа (2019). Металлоорганические соединения для зеленого катализа. Springer. С. 69–70. ISBN 9783030109554.
- ^ Мотиенко Р.А. (21 июня 2016 г.). «Миллиметровая спектроскопия метоксиметанола». HDL:2142/91121. Цитировать журнал требует
| журнал =(Помогите)
