Этилсульфат - Ethyl sulfate
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Этиловый гидросульфат | |
| Другие имена Этилсульфат; Сульфовиновая кислота; Этилбисульфат; Этоксисульфоновая кислота; Этилсульфат | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.007.963 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C2ЧАС6О4S | |
| Молярная масса | 126.13 г · моль−1 |
| Плотность | 1,46 г / см³ |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
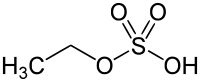
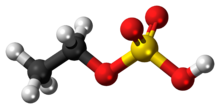
Этилсульфат (Название ИЮПАК: этилгидросульфат), также известный как сульфовиновая кислота, является органический химикат сложный используется в качестве промежуточного продукта при производстве этиловый спирт из этилен. Это этиловый сложный эфир серной кислоты.
История
Это вещество изучалось одновременно с эфир к Немецкий алхимик Август Зигмунд Фробениус в 1730 г.,[1] впоследствии Французский химики Фуркрой в 1797 г. и Гей-Люссак в 1815 г.[2][3] Швейцарский ученый Николя-Теодор де Соссюр также изучал его в 1807 году.[4] В 1827 г. химик и фармацевт Феликс-Полидор Булле (1806-1835) вместе с Жан-Батист Андре Дюма отметили роль этилсульфата в приготовлении диэтиловый эфир из серная кислота и этиловый спирт.[5][6] Дальнейшие исследования немецкого химика Эйльхард Митчерлих и шведский химик Йенс Берцелиус предположил, что серная кислота действовала как катализатор, это в конечном итоге привело к открытию сульфовиновой кислоты в качестве промежуточного продукта в процессе.[7][8] Появление электрохимия к Итальянский физик Алессандро Вольта и английский химик Хэмфри Дэви в 1800-х годах было подтверждено, что эфир и вода образовывались в результате реакции субстехиометрический количества серной кислоты на этаноле, и эта сульфовиновая кислота образовалась в качестве промежуточного продукта в реакции.[9]
Производство
Этиловый спирт был произведен в основном в процессе гидратации серной кислоты, в котором этилен реагирует с серная кислота для производства этилсульфата с последующим гидролиз,[10] но этот метод в основном заменен прямым гидратация этилена.[11]
Этилсульфат можно получить в лабораторных условиях путем реакции этиловый спирт с серная кислота при слабом кипении, при поддержании реакции ниже 140 ° C. Серную кислоту необходимо добавлять по каплям или реакционную смесь необходимо активно охлаждать, поскольку сама реакция является сильно экзотермической.
- CH3CH2ОН + Н2ТАК4 → CH3-CH2-О-ТАК3H + H2О
Если температура превышает 140 ° C, этилсульфатный продукт имеет тенденцию реагировать с остаточным исходным материалом этанола с образованием диэтиловый эфир. Если при значительном избытке серной кислоты температура превышает 170 ° C, этилсульфат распадается на этилен и серная кислота.[12][13]
Реакции
Механизм образования этилсульфата, диэтиловый эфир, и этилен основан на реакции между этанолом и серная кислота, который включает протонирование этанольного кислорода с образованием[нечеткий ] оксониевый ион.[13]
Этилсульфат накапливается в волосах после хронического употребления алкоголя, и его обнаружение можно использовать как биомаркер для употребления алкоголя.[14]
Соли
Этилсульфат может существовать в солевых формах, таких как этилсульфат натрия, этилсульфат калия и этилсульфат кальция. Соль может быть образована добавлением соответствующей карбонатной или бикарбонатной соли. Например, этилсульфат и карбонат калия образует этилсульфат калия и бикарбонат калия.[13]
- CH3-CH2-О-ТАК3H + K2CO3 → CH3-CH2-О-ТАК3K + KHCO3
Смотрите также
Рекомендации
- ^ Доктор Фробениус (1730) «Отчет о spiritus vini æthereus вместе с несколькими опробованными экспериментами», Философские труды Королевского общества (Лондона), 36 (413) : 283–289.
- ^ Фуркрой А.Ф., Воклен Л.Н. (1797) "Sur l'action de l'acide sulfique sur l'alcool et de la education de l'éther" В архиве 2016-03-19 в Wayback Machine (О действии серной кислоты на спирт и образовании эфира), Annales de Chimie, 23 : 203-215.
- ^ Гей-Люссак, Л. Дж. (1815) "Sur l'analyse de l'alcool et de l'éther sulfique et sur les produits de la fermentation" (Об анализе спирта и серного эфира и продуктов брожения), Annales de Chimie, 95 : 311-318.
- ^ Теодор де Соссюр (1807) "Воспоминание о композиции алкоголя и серного эфира", В архиве 2016-12-26 в Wayback Machine Journal de Physique, de chimie, d'histoire naturelle et des arts, 64 : 316–354.
- ^ Дюма, Дж. Б. и Булле, П. (1827) "Mémoire sur la education de l'éther sulfique", Annales de Chimie et de Physique, 36 : 294-316.
- ^ Висняк, Хайме (2010). "Феликс-Полидор Булле" (PDF). Revista CENIC Ciencias Químicas. 41 (1): 59–66. В архиве (PDF) из оригинала на 2017-08-16. Получено 2013-08-09.
- ^ Э. Мичерлих (1834). "Ueber die Aetherbildung" В архиве 2017-01-13 в Wayback Machine (Об образовании эфира), Annalen der Physik und Chemie, 31 (18) : 273-282.
- ^ Дж. Дж. Берцелиус, Årsberättelsen om framsteg i fysik och kemi [Годовой отчет о достижениях в области физики и химии], (Стокгольм, Швеция: Шведская королевская академия наук, 1835 г.). Изучив исследования Эйльхарда Мичерлиха по образованию эфира, Берцелиус придумал слово Каталис (катализ) на стр. 245 В архиве 2017-01-13 в Wayback Machine:
Оригинал: Jag skall derföre, för att beginagna en i kemien välkänd härledning, kalla den kroppars каталитиска крафт, sönderdelning genom denna kraft Каталис, likasom vi med ordet analys beteckna åtskiljandet af kroppars beståndsdelar medelst den vanliga kemiska frändskapen.
Перевод: Поэтому, используя хорошо известное химическое выражение, я буду называть [каталитические] тела [то есть вещества] каталитическая сила и разложение [других] тел этой силой катализ, так же, как мы обозначаем словом анализ разделение составных частей тел обычным химическим сродством.
- ^ «История эфира». Состав и структура эфира. В архиве с оригинала 27 декабря 2003 г.. Получено 7 сентября, 2005.
- ^ Фрэнк С. Уитмор (2012). Органическая химия. Один. Курьерская корпорация. ISBN 9780486311159.
- ^ Ландау, Ральф; Шаффель, Г. С (1971). «Последние разработки в химии этилена». Происхождение и переработка нефти. Успехи химии. 103. стр.150–157. Дои:10.1021 / ba-1971-0103.ch008. ISBN 978-0-8412-0120-0.
- ^ Юлиус Б. Коэн (1930). Практическая органическая химия (подготовка 5). Макмиллан.
- ^ а б c Фредерик Джордж Манн и Бернард Чарльз Сондерс (1960). Практическая органическая химия (препараты, взаимодействие этанола и серной кислоты). Longman Inc.
- ^ Каппель, Дельфина; Лай, Фун Инь; Ковачи, Адриан; Вермассен, Аннеми; Crunelle, Cleo L .; Нилс, Хьюго; Ван Нуйс, Александр Л. (2018). «Оценка этилсульфата в волосах как маркера потребления алкоголя с использованием жидкостной хроматографии-тандемной масс-спектрометрии». Тестирование и анализ на наркотики. 10 (10): 1566–1572. Дои:10.1002 / dta.2410. PMID 29923331.
