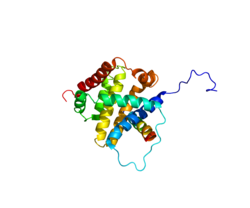
BCL2L11 - BCL2L11
Bcl-2-подобный белок 11, обычно называемый BIM, представляет собой белок что у людей кодируется BCL2L11 ген.[5][6]
Функция
Белок, кодируемый этим геном, принадлежит к BCL-2 семейство белков. Члены семейства BCL-2 образуют гетеро- или гомодимеры и действуют как анти- или про-апоптотический регуляторы, которые участвуют в широком спектре клеточной деятельности. Белок, кодируемый этим геном, содержит домен 3 гомологии Bcl-2 (BH3). Было показано, что он взаимодействует с другими членами семейства белков BCL-2, включая BCL2, BCL2L1 / BCL-X (L) и MCL1, и действовать как активатор апоптоза. Экспрессия этого гена может быть вызвана фактор роста нервов (NGF), а также фактором транскрипции вилки FKHR-L1 (FoxO3a ), что предполагает роль этого гена в апоптозе нейронов и лимфоцитов. Трансгенные исследования аналога мыши показали, что этот ген функционирует как важный инициатор апоптоза в тимоцит -отрицательный выбор. Было идентифицировано несколько альтернативно сплайсированных вариантов транскрипта этого гена.[7]
Регулирование BIM
Экспрессия и активность Bim регулируются на транскрипционном, трансляционном и посттрансляционном уровнях; скоординированная экспрессия и активность Bim формируют иммунные ответы и обеспечивают целостность тканей. Раковые клетки развивают механизмы, которые подавляют экспрессию Bim, что способствует прогрессированию опухоли и метастазированию.[8]
Взаимодействия
BCL2L11 показал способность взаимодействовать с:
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000153094 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000027381 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ а б c d е Хсу С.Ю., Линь П., Сюэ А.Дж. (ноябрь 1998 г.). «BOD (ген смерти яичников, связанный с Bcl-2) представляет собой проапоптотический белок Bcl-2, содержащий домен BH3 яичника, способный к димеризации с различными антиапоптотическими членами Bcl-2». Мол Эндокринол. 12 (9): 1432–40. Дои:10.1210 / исправление.12.9.0166. PMID 9731710.
- ^ а б c d О'Коннор Л., Штрассер А., О'Рейли Л.А., Хаусманн Дж., Адамс Дж. М., Кори С., Хуанг, округ Колумбия (февраль 1998 г.). «Bim: новый член семейства Bcl-2, способствующий апоптозу». EMBO J. 17 (2): 384–95. Дои:10.1093 / emboj / 17.2.384. ЧВК 1170389. PMID 9430630.
- ^ «Ген Энтреза: BCL2L11 BCL2-подобный 11 (посредник апоптоза)».
- ^ Сионов Р.В., Влахопулос С.А., Гранот З. (2015). «Регулирование BIM в здоровье и болезнях». Oncotarget. 6 (27): 23058–134. Дои:10.18632 / oncotarget.5492. ЧВК 4695108. PMID 26405162.
- ^ а б c Чен Л., Уиллис С.Н., Вэй А., Смит Б.Дж., Флетчер Д.И., Хайндс М.Г., Колман П.М., Дэй К.Л., Адамс Дж.М., Хуанг, округ Колумбия (февраль 2005 г.). «Дифференциальное нацеливание белков Bcl-2 для выживания с помощью их лигандов, содержащих только BH3, обеспечивает комплементарную апоптотическую функцию». Мол. Клетка. 17 (3): 393–403. Дои:10.1016 / j.molcel.2004.12.030. PMID 15694340.
- ^ Уитфилд Дж., Харада К., Барделл С., Стаддон Дж. М. (ноябрь 2003 г.). «Высокопроизводительные методы обнаружения димеризации белков семейства Bcl-2». Анальный. Биохим. 322 (2): 170–8. Дои:10.1016 / j.ab.2003.07.014. PMID 14596824.
- ^ Day CL, Puthalakath H, Skea G, Strasser A, Barsukov I, Lian LY, Huang DC, Hinds MG (февраль 2004 г.). «Локализация легких цепей 1 и 2 динеина и их проапоптотических лигандов». Biochem. J. 377 (Pt 3): 597–605. Дои:10.1042 / BJ20031251. ЧВК 1223895. PMID 14561217.
- ^ Вадламуди Р.К., Багери-Ярманд Р., Ян З., Баласентил С., Нгуен Д., Сахин А.А., ден Холландер П., Кумар Р. (июнь 2004 г.). «Легкая цепь динеина 1, субстрат, взаимодействующий с p21-активированной киназой 1, способствует злокачественным фенотипам». Раковая клетка. 5 (6): 575–85. Дои:10.1016 / j.ccr.2004.05.022. PMID 15193260.
- ^ Пэ Дж., Лео С. П., Сюй С.Ю., Сюэ А.Дж. (август 2000 г.). «MCL-1S, вариант сплайсинга антиапоптотического члена семейства BCL-2 MCL-1, кодирует проапоптотический белок, имеющий только домен BH3». J. Biol. Chem. 275 (33): 25255–61. Дои:10.1074 / jbc.M909826199. PMID 10837489.
дальнейшее чтение
- Ван К., Инь XM, Чао Д.Т. и др. (1996). «BID: новый агонист смерти, содержащий только домен BH3». Genes Dev. 10 (22): 2859–69. Дои:10.1101 / gad.10.22.2859. PMID 8918887.
- Чжа Дж., Харада Х., Ян Э. и др. (1997). «Фосфорилирование серина агониста смерти BAD в ответ на фактор выживания приводит к связыванию с 14-3-3, а не с BCL-X (L)». Клетка. 87 (4): 619–28. Дои:10.1016 / S0092-8674 (00) 81382-3. PMID 8929531. S2CID 860908.
- Хуанг, округ Колумбия, Адамс Дж. М., Кори С. (1998). «Консервативный N-концевой домен BH4 гомологов Bcl-2 необходим для ингибирования апоптоза и взаимодействия с CED-4». EMBO J. 17 (4): 1029–39. Дои:10.1093 / emboj / 17.4.1029. ЧВК 1170452. PMID 9463381.
- Puthalakath H, Huang DC, O'Reilly LA, et al. (1999). «Проапоптотическая активность Bim члена семейства Bcl-2 регулируется взаимодействием с моторным комплексом динеина». Мол. Клетка. 3 (3): 287–96. Дои:10.1016 / S1097-2765 (00) 80456-6. PMID 10198631.
- Охи Н., Токунага А., Цунода Х. и др. (1999). «Новый аденовирусный E1B19K-связывающий белок B5 ингибирует апоптоз, индуцированный Nip3, путем образования гетеродимера через С-концевую гидрофобную область». Разница в гибели клеток. 6 (4): 314–25. Дои:10.1038 / sj.cdd.4400493. PMID 10381623.
- Булье П., Меткалф Д., Хуанг Д.К. и др. (1999). «Проапоптотический Bcl-2 родственник Bim, необходимый для определенных апоптотических реакций, гомеостаза лейкоцитов и предотвращения аутоиммунитета». Наука. 286 (5445): 1735–8. Дои:10.1126 / science.286.5445.1735. PMID 10576740.
- Dijkers PF, Medema RH, Lammers JW и др. (2000). «Экспрессия проапоптотического члена семейства Bcl-2 Bim регулируется фактором транскрипции вилки FKHR-L1». Curr. Биол. 10 (19): 1201–4. Дои:10.1016 / S0960-9822 (00) 00728-4. PMID 11050388. S2CID 17945478.
- Булье П., Чжан Л.К., Хуанг Д.К. и др. (2001). «Альтернативный сплайсинг генной структуры и хромосомная локализация проапоптотического Bcl-2 относительно Bim». Мамм. Геном. 12 (2): 163–8. Дои:10.1007 / s003350010242. PMID 11210187. S2CID 7225766.
- Putcha GV, Moulder KL, Golden JP и др. (2001). «Индукция BIM, проапоптотического члена семейства BCL-2, содержащего только BH3, имеет решающее значение для апоптоза нейронов». Нейрон. 29 (3): 615–28. Дои:10.1016 / S0896-6273 (01) 00238-0. PMID 11301022. S2CID 16223140.
- Мюррей С., Халфорд С., Эбенезер Н.Д. и др. (2001). «Отнесение BCL2L11 к полосе хромосомы человека 2p13 с соматическими клетками и радиационными гибридами». Cytogenet. Cell Genet. 92 (3–4): 353. Дои:10.1159/000056930. PMID 11435715. S2CID 32790948.
- Cheng EH, Wei MC, Weiler S и др. (2001). «BCL-2, BCL-X (L) изолируют молекулы, содержащие только домен BH3, предотвращая BAX- и BAK-опосредованный митохондриальный апоптоз». Мол. Клетка. 8 (3): 705–11. Дои:10.1016 / S1097-2765 (01) 00320-3. PMID 11583631.
- Мами У, Мияшита Т., Шикама Ю. и др. (2002). «Молекулярное клонирование и характеристика шести новых изоформ Bim человека, члена проапоптотического семейства Bcl-2». FEBS Lett. 509 (1): 135–41. Дои:10.1016 / S0014-5793 (01) 03145-3. PMID 11734221. S2CID 82875886.
- Булье П., Пуртон Дж. Ф., Годфри Д. И. и др. (2002). «Только BH3-член семейства Bcl-2 Bim необходим для апоптоза аутореактивных тимоцитов». Природа. 415 (6874): 922–6. Дои:10.1038 / 415922a. PMID 11859372. S2CID 1404636.
- Марани М., Тенев Т., Хэнкок Д. и др. (2002). «Идентификация новых изоформ Bim домена BH3, которые непосредственно активируют Bax, чтобы вызвать апоптоз». Мол. Клетка. Биол. 22 (11): 3577–89. Дои:10.1128 / MCB.22.11.3577-3589.2002. ЧВК 133811. PMID 11997495.
- Лю Дж. У., Чандра Д., Тан Ш. и др. (2002). «Идентификация и характеристика Bimgamma, нового проапоптотического варианта сплайсинга BH3 Bim». Рак Res. 62 (10): 2976–81. PMID 12019181.
- Террадильос О., Монтессуит С., Хуанг, округ Колумбия, Мартину Дж. К. (2002). «Прямое добавление BimL в митохондрии не приводит к высвобождению цитохрома с». FEBS Lett. 522 (1–3): 29–34. Дои:10.1016 / S0014-5793 (02) 02871-5. PMID 12095614. S2CID 20419085.
- Сугияма Т., Симидзу С., Мацуока Ю. и др. (2002). «Активация митохондриального потенциал-зависимого анионного канала апроапоптотическим белком BH3 Bim». Онкоген. 21 (32): 4944–56. Дои:10.1038 / sj.onc.1205621. PMID 12118373.
внешняя ссылка
- BCL2L11 расположение человеческого гена в Браузер генома UCSC.
- BCL2L11 детали человеческого гена в Браузер генома UCSC.
| Эта статья о ген на хромосома 2 человека это заглушка. Вы можете помочь Википедии расширяя это. |