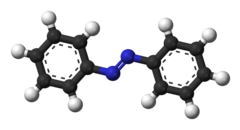
Азобензол - Azobenzene
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК (E) -Дифенилдиазен | |
| Другие имена Азобензол | |
| Идентификаторы | |
3D модель (JSmol ) | |
| 742610 | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.002.820 |
| Номер ЕС |
|
| 83610 | |
| КЕГГ | |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| |
| |
| Характеристики | |
| C12ЧАС10N2 | |
| Молярная масса | 182.226 г · моль−1 |
| Внешность | оранжево-красные кристаллы[1] |
| Плотность | 1,203 г / см3[1] |
| Температура плавления | 67,88 ° C (транс), 71,6 ° C (цис) [1] |
| Точка кипения | 300 ° С (572 ° F, 573 К)[1] |
| 6,4 мг / л (25 ° С) | |
| Кислотность (пKа) | -2.95[2] |
| -106.8·10−6 см3/ моль[3] | |
| 1,6266 (589 нм, 78 ° С)[1] | |
| Структура | |
| зр2 в N | |
| 0 D (транс-изомер) | |
| Опасности | |
| Главный опасности | токсичный |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| H302, H332, H341, H350, H373, H400, H410 | |
| P201, P202, P260, P261, P264, P270, P271, P273, P281, P301 + 312, P304 + 312, P304 + 340, P308 + 313, P312, P314, P330, P391, P405, P501 | |
| точка возгорания | 476 ° С (889 ° F, 749 К) |
| Родственные соединения | |
Родственные соединения | Нитрозобензол анилин |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Азобензол это химический соединение, состоящее из двух фенил кольца, соединенные N = N двойная связь. Это простейший пример арила. азосоединение. Термин «азобензол» или просто «азо» часто используется для обозначения широкого класса подобных соединения. Эти азосоединения рассматриваются как производные диазен (диимид),[4] и иногда их называют «диазенами». Диазены сильно поглощают свет и широко распространены. красители.
Структура и синтез
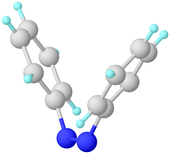
транс-Азобензол планарный. Расстояние N-N составляет 1,189 Å.[5] СНГ-Азобензол непланарен с двугранным углом C-N = N-C, равным 173,5 °. Расстояние N-N составляет 1,251 Å.[6]Азобензол впервые был описан Эйльхард Митчерлих в 1834 г.[7][8] Желтовато-красные кристаллические чешуйки азобензола были получены в 1856 г.[9] Его оригинальное приготовление похоже на современное. По методу 1856 г. нитробензол восстанавливается железными опилками в присутствии уксусная кислота. В современном синтезе цинк является восстановителем в присутствии основания.[10] Промышленное электросинтез также применяется нитробензол.[11]
Транс-изомер более стабилен примерно на 50 кДж / моль, а барьер для изомеризации в основном состоянии составляет примерно 100 кДж / моль.


Реакции
Азобензол является слабым основанием, но подвергается протонированию при одном азоте с pKа = -2,95. Он функционирует как База Льюиса, например в сторону тригалогенидов бора. Он связывается с центрами металлов с низкой валентностью, например Ni (Ph2N2) (PPh3)2 хорошо охарактеризован.[12]
Он окисляется, чтобы дать азоксибензол. Гидрирование дает дифенилгидразин.
Транс-цис-изомеризация
Азобензол (и производные) подвергаются фотоизомеризация из транс и СНГ изомеры. цис-азобензол расслабляется обратно в темноте к транс-изомеру. Такая тепловая релаксация происходит медленно при комнатной температуре. Два изомера можно переключать с помощью определенных длин волн света: ультрафиолетового света, который соответствует запрещенной зоне π-π * (S2 состояние), для преобразования транс-в-цис, и синий свет, который эквивалентен свету n-π * (S1 состояние) переход для цис-транс-изомеризации. По разным причинам СНГ изомер менее стабилен, чем транс (например, он имеет искаженную конфигурацию и менее делокализован, чем транс-конфигурация). Фотоизомеризация позволяет осуществлять обратимое хранение энергии (как фотопереключатели ).
Спектроскопическая классификация
Длины волн, при которых происходит изомеризация азобензола, зависят от конкретной структуры каждой азомолекулы, но они обычно группируются в три класса: молекулы азобензольного типа, аминоазобензолы и псевдо-молекулы.стильбены. Эти азо желтые, оранжевые и красные соответственно,[13][14] из-за тонких различий в их электронных спектрах поглощения. Соединения, подобные незамещенному азобензолу, демонстрируют низкоинтенсивное n-π * -поглощение в видимой области и гораздо более высокую интенсивность π-π * -поглощения в видимой области. ультрафиолетовый. Азосы, которые орто- или же паразамещенный с электронодонорные группы (Такие как амино ), классифицируются как аминоазобензолы и имеют тенденцию к близкому расположению[13] n-π * и π-π * полосы в видимом диапазоне. Класс псевдо-стильбенов характеризуется заменой положений 4 и 4 'двух азоколец электронодонорными и электроноакцепторными группами (то есть двумя противоположными концами ароматный система функционализирована). Добавление этого тяни-Толкай конфигурация приводит к сильно асимметричной электрон распределение, которое изменяет множество оптических свойств. В частности, сдвигается спектры поглощения из транс и СНГ изомеры, так что они эффективно перекрываются.[14] Таким образом, для этих соединений единый длина волны света в видимой области будет вызывать как прямую, так и обратную изомеризацию. Под освещением эти молекулы циклически переходят между двумя изомерными состояниями.
Фотофизика изомеризации
Фотоизомеризация азобензола происходит очень быстро и в пикосекундных временных масштабах. Скорость тепловой обратной релаксации сильно варьируется в зависимости от соединения: обычно часы для молекул азобензольного типа, минуты для аминоазобензолов и секунды для псевдостильбенов.[14]
Механизм изомеризации был предметом некоторых дискуссий, и два пути были определены как жизнеспособные: вращение о связи N-N, с разрывом двойной связи или через инверсия, с полулинейным и гибридным переходным состоянием. Было высказано предположение, что транс-к-СНГ преобразование происходит через вращение в S2 состояние, тогда как инверсия порождает СНГ-к-транс конверсия. Все еще обсуждается, какое возбужденное состояние играет прямую роль в ряде поведения фотоизомеризации. Однако последние исследования спектроскопия фемтосекундных переходов предположил, что S2 состояние подвергается внутреннему преобразованию в S1 состояние, а затем транс-к-СНГ идет изомеризация. Недавно Диау предложил другой путь изомеризации,[15] путь «согласованной инверсии», при котором оба валентных угла CNN изгибаются одновременно.
Фотоиндуцированные движения
Фотоизомеризация азобензола - это форма движения молекул под действием света.[13][16][17] Эта изомеризация также может привести к движению в больших масштабах. Например, поляризованный свет заставит молекулы изомеризоваться и расслабиться в случайных положениях. Однако те расслабленные (транс) молекулы, которые падают перпендикулярно поляризации входящего света, больше не смогут поглощать и останутся фиксированными. Таким образом, происходит статистическое обогащение хромофоров перпендикулярно поляризованному свету (ориентационное горение дырок). Поляризованное излучение сделает азо-материал анизотропный и поэтому оптически двулучепреломляющий и дихроичный. Эту фотоориентацию можно также использовать для ориентирования других материалов (особенно в жидкокристаллический системы).[18]
Рекомендации
- ^ а б c d е Хейнс, стр. 3,32
- ^ Hoefnagel, M. A .; Van Veen, A .; Вепстер, Б. М. (1969). «Протонирование азосоединений. Часть II: Структура конъюгированной кислоты транс-азобензола». Рекл. Trav. Чим. Pays-Bas. 88 (5): 562–572. Дои:10.1002 / recl.19690880507.
- ^ Хейнс, стр. 3,579
- ^ ИЮПАК, Сборник химической терминологии, 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2009 г.) "азосоединения ". Дои:10.1351 / goldbook.A00560
- ^ Harada, J .; Ogawa, K .; Томода, С. (1997). «Молекулярное движение и конформационное взаимопревращение азобензолов в кристаллах по данным рентгеновской дифракции». Acta Crystallogr. B. 53 (4): 662. Дои:10.1107 / S0108768197002772.
- ^ Мостад А. и Ремминг К. (1971). «Уточнение кристаллической структуры цис-азобензола». Acta Chem. Сканд. 25: 3561. Дои:10.3891 / acta.chem.scand.25-3561.CS1 maint: использует параметр авторов (связь)
- ^ Митчерлих, Э. (1834). "Ueber das Stickstoffbenzid". Анна. Фарм. 12 (2–3): 311–314. Bibcode:1834АнП ... 108..225М. Дои:10.1002 / jlac.18340120282.
- ^ Мерино, Эстибализ и Рибагорда Байльштейн, Мария (2012). «Управление движением молекул с помощью цис-транс-фотоизомеризации азогруппы». J. Org. Chem. 8: 1071–1090. Дои:10.3762 / bjoc.8.119. ЧВК 3458724. PMID 23019434.CS1 maint: несколько имен: список авторов (связь)
- ^ Благородный, Альфред (1856). "III. Zur Geschichte des Azobenzols und des Benzidins". Annalen der Chemie und Pharmacie. 98 (2): 253–256. Дои:10.1002 / jlac.18560980211.
- ^ Bigelow, H.E .; Робинсон, Д. Б. (1955). «Азобензол». Органический синтез. 22: 28.; Коллективный объем, 3, п. 103
- ^ Кардосо, Д. С .; Šljukić, B .; Сантос, Д. М .; Секейра, К. А. (17 июля 2017 г.). «Органический электросинтез: от лабораторной практики до промышленного применения». Исследования и разработки в области органических процессов. 21 (9): 1213–1226. Дои:10.1021 / acs.oprd.7b00004.
- ^ Федотова, Яна В .; Корнев, Александр Н .; Сушев, Вячеслав В .; Курский, Юрий А .; Муштина, Татьяна Г .; Макаренко, Наталья П .; Фукин, Георгий К .; Абакумов, Глеб А .; Захаров, Лев Н .; Рейнгольд, Арнольд Л. (2004). «Фосфиногидразины и фосфиногидразиды M (–N (R) –N (R) –PPh2) n некоторых переходных металлов и металлов основной группы: синтез и характеристика: перегруппировка лигандов Ph2P – NR – NR– в аминоиминофосфоран, RNPPh2 – NR– и родственная химия ». J. Organomet. Chem. 689 (19): 3060–3074. Дои:10.1016 / j.jorganchem.2004.06.056.
- ^ а б c Рау, Х. (1990). Рабек, Дж. Ф. (ред.). Фотохимия и фотофизика. 2. Бока-Ратон, Флорида: CRC Press. С. 119–141. ISBN 978-0-8493-4042-0.
- ^ а б c Ягер, К. Г .; Барретт, К. Дж. (2008). «Глава 17 - Азобензольные полимеры как фотомеханические и многофункциональные интеллектуальные материалы». В Шахинпур, М .; Шнайдер, Х.-Дж. (ред.). Интеллектуальные материалы. Кембридж: Королевское химическое общество. С. 426–427. Дои:10.1039/9781847558008-00424. ISBN 978-1-84755-800-8.
- ^ Diau, E. W.-G. (2004). «Новый механизм транс-цис-фотоизомеризации азобензола на поверхности S1 (n, π *)». Журнал физической химии A. 108 (6): 950–956. Bibcode:2004JPCA..108..950 Вт. Дои:10.1021 / jp031149a. S2CID 54662441.
- ^ Натансон А .; Рочон, П. (ноябрь 2002 г.). «Фотоиндуцированные движения в азосодержащих полимерах». Химические обзоры. 102 (11): 4139–4175. Дои:10.1021 / cr970155y. PMID 12428986.
- ^ Yu, Y .; Nakano, M .; Икеда, Т. (2003). «Фотомеханика: Направленное изгибание полимерной пленки светом». Природа. 425 (6954): 145. Bibcode:2003Натура.425..145л. Дои:10.1038 / 425145a. PMID 12968169.
- ^ Ичимура, К. (2000). «Фото-юстировка жидкокристаллических систем». Химические обзоры. 100 (5): 1847–1874. Дои:10.1021 / cr980079e. PMID 11777423.
Цитированные источники
- Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. п. 3.32. ISBN 1439855110.
дальнейшее чтение
- Исторический интерес: Г. С. Хартли (1937). «Цис-форма азобензола». Природа. 140 (3537): 281. Bibcode:1937Натура.140..281H. Дои:10.1038 / 140281a0.
- Torres-Zúñiga, V .; Morales-Saavedra, O.G .; Rivera, E .; Castañeda-Guzmán, R .; Bañuelos, J. G .; Ортега-Мартинес, Р. (2010). «Получение и фотофизические свойства мономерных жидкокристаллических азокрасителей, внедренных в объемный и пленочный SiO2.2-соногель очки ». Журнал золь-гель науки и технологий. 56 (1): 7–18. Дои:10.1007 / s10971-010-2265-у.
- Tazuke, S .; Kurihara, S .; Икеда, Т. (1987). «Запись усиленного изображения на жидкокристаллических носителях с помощью фотохимически инициируемого фазового перехода». Письма по химии. 16 (5): 911–914. Дои:10.1246 / cl.1987.911.
- Тамаоки, Н. (2001). «Холестерические жидкие кристаллы для цветных информационных технологий». Современные материалы. 13 (15): 1135–1147. Дои:10.1002 / 1521-4095 (200108) 13:15 <1135 :: AID-ADMA1135> 3.0.CO; 2-S.
- Pieraccini, S .; Masiero, S .; Spada, G.P .; Готтарелли, Г. (2003). «Новый аксиально-хиральный фотохимический переключатель». Химические коммуникации. 2003 (5): 598–599. Дои:10.1039 / b211421f. PMID 12669843.
- Ягер, К. Г .; Барретт, К. Дж. (2006). «Фотомеханическое моделирование поверхности в азополимерных материалах». Макромолекулы. 39 (26): 9320–9326. Bibcode:2006MaMol..39.9320Y. Дои:10.1021 / ma061733s.
- Горостиза, П .; Исаков, Э. Я. (октябрь 2008 г.). «Оптические переключатели для дистанционного и неинвазивного контроля клеточной сигнализации». Наука. 322 (5900): 395–399. Bibcode:2008Наука ... 322..395G. Дои:10.1126 / science.1166022. PMID 18927384.
- Banghart, M. R .; Волграф, М .; Траунер, Д. (декабрь 2006 г.). «Инженерные светозатворные ионные каналы». Биохимия. 45 (51): 15129–15141. CiteSeerX 10.1.1.70.6273. Дои:10.1021 / bi0618058. PMID 17176035.
